
КАТЕГОРИИ:
Архитектура-(3434)Астрономия-(809)Биология-(7483)Биотехнологии-(1457)Военное дело-(14632)Высокие технологии-(1363)География-(913)Геология-(1438)Государство-(451)Демография-(1065)Дом-(47672)Журналистика и СМИ-(912)Изобретательство-(14524)Иностранные языки-(4268)Информатика-(17799)Искусство-(1338)История-(13644)Компьютеры-(11121)Косметика-(55)Кулинария-(373)Культура-(8427)Лингвистика-(374)Литература-(1642)Маркетинг-(23702)Математика-(16968)Машиностроение-(1700)Медицина-(12668)Менеджмент-(24684)Механика-(15423)Науковедение-(506)Образование-(11852)Охрана труда-(3308)Педагогика-(5571)Полиграфия-(1312)Политика-(7869)Право-(5454)Приборостроение-(1369)Программирование-(2801)Производство-(97182)Промышленность-(8706)Психология-(18388)Религия-(3217)Связь-(10668)Сельское хозяйство-(299)Социология-(6455)Спорт-(42831)Строительство-(4793)Торговля-(5050)Транспорт-(2929)Туризм-(1568)Физика-(3942)Философия-(17015)Финансы-(26596)Химия-(22929)Экология-(12095)Экономика-(9961)Электроника-(8441)Электротехника-(4623)Энергетика-(12629)Юриспруденция-(1492)Ядерная техника-(1748)
Основные понятия кинетики цепных реакций
|
|
|
|
Первая схема цепного процесса предложена В.Нернстом в 1918 г. для описания реакции H2+Cl2=2HCl. Примерами цепных радикальных реакций являются: окисление органических веществ молекулярным кислородом, взаимодействие водорода и углеводородов с хлором и бромом, термическое разложение озона и кислородных соединений хлора, крекинг нефтепродуктов, полимеризация поликонденсация, а также ядерные реакции разложения урана или плутония в атомном реакторе.
Цепными называются химические реакции, в которых появление активной частицы вызывает большое число превращений неактивных молекул вследствие регенерации активной частицы в каждом элементарном акте этого процесса.
Активными частицами являются: атомы, обладающие неспаренными электронами, свободные радикалы, несольватированные ионы, возбужденные молекулы, то есть частицы с нескомпенсированной валентностью. Образование активных частиц связано с затратой энергии на разрыв химических связей.
Любая цепная реакция состоит из трех стадий:
1. зарождение цепи;
2. продолжение (развития) цепи;
3. обрыв цепи.
В стадии зарождения цепи (или стадии инициирования) образуются активные молекулы. Причинами этого могут быть:
· Распад молекул на свободные радикалы
· Гетерогенные условия протекания реакции (то есть за счет участия стенок сосуда)
· Инициирование извне: под действием света или ионизирующего излучения, добавление специальных веществ - инициаторов образования свободных радикалов.
Стадия продолжения цепи состоит из большого числа повторяющихся элементарных реакций взаимодействия активных частиц с исходным веществом.
 Если количество образующихся активных частиц не превосходит числа исходных, то это неразветвленная цепная реакция (НЦР).
Если количество образующихся активных частиц не превосходит числа исходных, то это неразветвленная цепная реакция (НЦР).
|
|
|
 Если количество активных частиц больше исходных – это разветвленная цепная реакция (РЦР).
Если количество активных частиц больше исходных – это разветвленная цепная реакция (РЦР).
Стадия обрыва цепи. Обрыв цепи происходит либо путем захвата свободных радикалов стенками реакционных сосудов или в результате взаимных столкновений радикалов.
Если радикал атакует молекулу продукта, замедляя цепной процесс - это ингибирование.
Неразветвленные цепные реакции (НЦР)
Неразветвленная цепная реакция включает в себя стадии зарождения, продолжения, и обрыва цепи.
Заслуга в разработке теории неразветвленных цепных реакций, по оценке Н.Н.Семенова, принадлежит школе Боденштейна (1913-1929). Классическим примером реакций этого типа является синтез HCl из водорода и хлора. Схема процесса предложена В.Нернстом, теоретический анализ кинетики реакции проведен в основном М.Боденштейном и его учениками.
Для характеристики неразветвленных цепных реакций используют понятия звено и длина цепи.
Звено цепи – это совокупность последовательных элементарных реакций продолжения цепи, которая приводит к регенерации активного центра, уже участвовавшего в реакции.
Например, для реакции C2H6+Cl2®C2H5Cl + HCl звено цепи состоит из двух элементарных реакций
C2H6+Cl·®·C2H5+HCl и ·C2H5+ Cl2®C2H5Cl+ Cl·.
Средняя длина цепи – это число полных звеньев, приходящихся в среднем на каждый активный центр, образовавшийся по реакции зарождения цепи или иначе – это количество молекул данного исходного вещества, которые вступают в реакцию в результате одного первичного элементарного акта зарождения цепи.
Скорость НЦР зависит от длины цепи, которая в реакциях может быть очень велика.
Скорость зарождения цепи обозначается w о.
Скорость процесса продолжения цепи 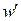
Скорость обрыва цепи 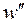
Длина цепи L определяется соотношением скорости процесса продолжения цепи 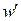 и скорости обрыва цепи
и скорости обрыва цепи 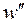
 (1)
(1)
|
|
|
Длина цепи зависит о т природы цепной реакции и условий ее протекания: концентрации и частоты реагентов, интенсивности света, температуры, материала реакционного сосуда, его размера и т.п.
Необходимым условием стационарного режима протекания неразветвленной цепной реакции является равенство скоростей зарождения и обрыва цепей
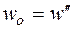 (2)
(2)
 (3)
(3)
Из анализа формулы (3) видно, что скорость НЦР зависит от скорости всех трех стадий, так как длина цепи связана с условиями продолжения цепи и обрыва цепи.
К кинетическим особенностям неразветвленной цепной реакции относятся: рост скорости под воздействием на реакционную смесь физических агентов (света и т.п.) и небольших количеств инициаторов; зависимость скорости от размеров сосуда, материала стенок и их состояния; быстрое уменьшение скорости при добавлении в реакционную смесь небольших количеств ингибиторов. Последнее обстоятельство является характерным признаком цепного механизма реакции. Если цепная реакция начинается в момент времени t = 0, то скорость ее не сразу достигнет некоторой постоянной величины 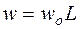 , поскольку для развития цепи необходимо время. В кинетике цепных реакций встречается понятие ингибирование реакции - это стадия, в которой радикал атакует молекулу продукта, замедляя тем самым цепной процесс.
, поскольку для развития цепи необходимо время. В кинетике цепных реакций встречается понятие ингибирование реакции - это стадия, в которой радикал атакует молекулу продукта, замедляя тем самым цепной процесс.
Дифференциальное кинетическое уравнение для скорости изменения концентрации активных центров в ходе неразветвленной цепной реакции
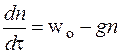 (4)
(4)
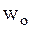 -скорость зарождения цепи; g − удельная скорость реакции обрыва цепи;
-скорость зарождения цепи; g − удельная скорость реакции обрыва цепи; -концентрация активных центров
-концентрация активных центров
Полагая, что 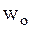 и g постоянны, интегрируем (4) в пределах от n = 0 при
и g постоянны, интегрируем (4) в пределах от n = 0 при  =0 до n при
=0 до n при  :
:
 (5)
(5)
Зависимость скорости реакции от времени:
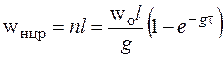 (6)
(6)
l − удельная скорость реакции продолжения цепи, ведущей к образованию продукта.
При 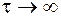
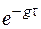 →0 и (6):
→0 и (6):
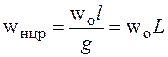 (7) стационарный режим.
(7) стационарный режим.
Разветвленные цепные реакции (РЦР)
Цепная реакция, включающая в себя стадии зарождения, продолжения, разветвления и обрыва цепи, называется разветвленной.
Примерами таких процессов являются реакции окисления кислородом фосфора, фосфина, водорода, монооксида углерода и др. Теория разветвленных цепных реакций разработана главным образом Н.Н.Семеновым и его школой, определенный вклад в ее развитие внес С.Н.Хиншельвуд. Н.Н.Семенов показал, что при общем описании закономерностей развития разветвленных цепных реакций система кинетических уравнений для активных центров может быть сведена к уравнению для активных центров одного вида.
|
|
|
Дифференциальной уравнение для скорости изменения концентрации активных центров
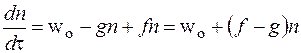 (1)
(1)
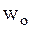 -скорость зарождения цепи
-скорость зарождения цепи
 -концентрация активных центров
-концентрация активных центров
 − скорость гибели активных центров
− скорость гибели активных центров
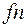 − скорость образования активных центров в результате реакций разветвления.
− скорость образования активных центров в результате реакций разветвления.
f − фактор разветвления цепи
g − фактор гибели цепи
Проинтегрируем (1) в пределах от 0 до 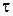 и от 0 до n.
и от 0 до n.
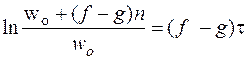 (2)
(2)
Число активных центров
 (3)
(3)
Скорость реакции – прирост активных центров в единицу времени
 (4)
(4)
Уравнение (4) − модельное уравнение любой цепной реакции.
|
|
|
|
Дата добавления: 2014-01-11; Просмотров: 5512; Нарушение авторских прав?; Мы поможем в написании вашей работы!