
КАТЕГОРИИ:
Архитектура-(3434)Астрономия-(809)Биология-(7483)Биотехнологии-(1457)Военное дело-(14632)Высокие технологии-(1363)География-(913)Геология-(1438)Государство-(451)Демография-(1065)Дом-(47672)Журналистика и СМИ-(912)Изобретательство-(14524)Иностранные языки-(4268)Информатика-(17799)Искусство-(1338)История-(13644)Компьютеры-(11121)Косметика-(55)Кулинария-(373)Культура-(8427)Лингвистика-(374)Литература-(1642)Маркетинг-(23702)Математика-(16968)Машиностроение-(1700)Медицина-(12668)Менеджмент-(24684)Механика-(15423)Науковедение-(506)Образование-(11852)Охрана труда-(3308)Педагогика-(5571)Полиграфия-(1312)Политика-(7869)Право-(5454)Приборостроение-(1369)Программирование-(2801)Производство-(97182)Промышленность-(8706)Психология-(18388)Религия-(3217)Связь-(10668)Сельское хозяйство-(299)Социология-(6455)Спорт-(42831)Строительство-(4793)Торговля-(5050)Транспорт-(2929)Туризм-(1568)Физика-(3942)Философия-(17015)Финансы-(26596)Химия-(22929)Экология-(12095)Экономика-(9961)Электроника-(8441)Электротехника-(4623)Энергетика-(12629)Юриспруденция-(1492)Ядерная техника-(1748)
Растворители в ТСХ
|
|
|
|
Применение чистых растворителей в большинстве литературы по ТСХ представляется как обязательное требование. С другой стороны, широкое применение в ТСХ бинарных элюентов (состоящих из смеси двух разных растворителей) и элюентов более сложного состава скорее ставит вопрос не столько о чистоте растворителей, сколько о постоянстве состава (или, даже, скорее, о его контролируемости) примесей одних растворителей в других. Так, применение элюентов, содержащих этанол и воду снимает необходимость использования абсолютного (безводного) этанола для приготовления элюента. Аналогично для приготовления элюента, содержащего в своем составе хлороформ, этанол и воду, нет необхолимости в приготовлении абсолютного хлороформа, а позволяет использовать “хлороформ для наркоза”, содержащий добавки этанола и воды для стабилизации. Эти примеры можно продолжить.
Действительно необходимым является отсутствие в растворителе примесей, которые могут взаимодействовать с какими либо компонентами анализируемой смеси. Если такие примеси будут присутствовать, на хроматограмме могут обнаруживаться артефакты (ложные пятна; свойство, привнесенное процедурой исследования; ложная информация или сигнал). Так, примесь фосгена в хлороформе (легко образуется при хранении безводного хлороформа) при анализе спиртов, первичных или вторичных аминов может приводить к образованию хлоформиатов, хлоримидатов, мочевин, изоцианатов и других веществ с Rf, отличным от Rf компонентов анализируемой пробы. Аналогично, примеси альдегидов и кетонов в спиртах при анализе производных гидразина могут приводить к частичной трансформации гидразинов в соответствующие гидразоны.
|
|
|
Нелетучие (труднолетучие) примеси в составе элюента могут затруднять или снижать чувствительность определения компонентов анализируемой смеси с применением проявляющих реактивов или УФ-облучения. Так, применение в составе элюента триэтиламина (или его присутствие в качестве примеси в другом растворителе) делает невозможным применение нингидрина для проявления хроматограммы аминов.
Существенным свойством растворителя для ТСХ является его летучесть. Это обусловлено тем, что ряд растворителей могут взаимодействовать с проявляющими реагентами ими поглощать УФ-излучение, препятствуя возбуждению флуоресценции анализируемого вещества или флуоресцентного индикатора. При недостаточной летучести эти растворители трудно удалить с поверхности после элюции хроматограммы, а повышение температуры при ее высушивании может привести к химической модификации анализируемого вещества или его потере. Поэтому при подборе элюента предпочтение при прочих равных условиях следует отдавать растворителю с меньшей температурой кипения (большей летучестью).
В основе элюирующего действия растворителей с поверхности адсорбента лежит конкуренция его молекул за центры адсорбции с молекулами анализируемого вещества. Чем выше энергия взаимодействия молекул растворителя с адсорбционным центрами, тем эта конкуренция эффективнее и тем большая доля молекул анилизируемого вещества оказывается в подвижной фазе, что приводит к увеличению Rf вещества. Однако, энергия адсорбции молекул растворителя на сорбенте – величина неудобная для непосредственного использования. Кроме того абсолютные величины ее в значительной степени зависят от состояния поверхности сорбента. В связи с этим для характеристики элюирующей способности элюентов удобнее использовать относительные эмпирические параметры, определенные Шнайдером. Значения этих параметров для основных растворителей, используемых в адсорбционной хроматографии приведены в таблице 6.2.
|
|
|
В идеальном случае при применении смеси растворителей элюотропный параметр смеси может быть рассчитан по уравнению 6.18.
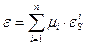 , ,
| ( | 6.18 | ) |
где
mi – мольная доля i -го растворителя в смеси;
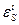 – элюотропный параметр i -го растворителя.
– элюотропный параметр i -го растворителя.
Однако, такая идеальная ситуация реализуется чрезвычайно редко – только при применении растворителей с очень близкими элюотропными параметрами, а такие смеси не имеют практически никакого преимущества перед чистыми растворителями.
| Таблица | 6.2 |
Эмпирические элюотропные параметры растворителей Шнайдера
| Растворители | eS (А1а03) | Растворители | eS (А13Оз) |
| Фторалканы | - 0.25 | 4-Метилпентанон-2 | 0.43 |
| н-Пентан | 0.00 | 1,2-Дихлорэтан | 0.44 |
| 2,2,4-Триметилпентан | 0.01 | Бутанон-2 | 0.51 |
| Петролейиый эфир | 0.01 | 1-Нитропропан | 0.53 |
| н-Декаи | 0.04 | Триэтиламин | 0.54 |
| Циклогексан | 0.04 | Ацетон | 0.56 |
| Циклопентан | 0.05 | 1,4-Диоксан | 0.56 |
| 2,4,4-Триметилбутен-1 | 0.06 | Тетрагидрофуран | 0.57 |
| Пентеи-1 | 0.08 | Этилацетат | 0.58 |
| Дисульфид углерода | 0.15 | Метилацетат | 0.60 |
| Тетрахлорметан | 0.18 | Пентанол-1 | 0.61 |
| 1-Хлор-н-пентан | 0.26 | Анилин | 0.62 |
| Ксилол | 0.26 | Диэтиламин | 0.63 |
| Диизопропиловый эфир | 0.28 | Нитрометан | 0.64 |
| 2-Хлорпропан | 0.29 | Ацетонитрил | 0.65 |
| Толуол | 0.29 | Пиридин | 0.71 |
| 1-Хлорпропан | 0.30 | 2-н-Бутоксиэтанол | 0.74 |
| Хлорбензол | 0.30 | Диметилсульфоксид | 0.75 |
| Бензол | 0.32 | Пропанол-1 | 0.82 |
| Бромэтан | 0.37 | Пропанол-2 | 0.82 |
| Диэтиловый эфир | 0.38 | Этанол | 0.88 |
| Диэтилсульфан | 0.38 | Метанол | 0.95 |
| Хлороформ | 0.40 | Этиленгликоль | 1.11 |
| Дихлорметан | 0.42 | Уксусная кислота | Большой |
В большинстве случаев в состав элюента входят растворители с весьма сильно различающимися элюотропными параметрами. В этом случае картина хроматографического процесса значительно усложняется – растворитель с бóльшим элюотропным параметром (B) избирательно сорбируется поверхностью, а свободная фаза оказывается состоящей из практически чистого растворителя с меньшим элюотропным параметром (A). По мере насыщения сорбента растворителем B, его концентрация в подвижной фазе постепенно возрастает и вскорости достигает максимума. Тем самым формируется “вторичный фронт”, отстающий от основного фронта (его еще называют b-фронтом). Зона, в которой возрастает концентрация второго растворителя тем уже, чем больше разница в элюотропных параметрах растворителей A и B, а расстояние между фронтами тем больше, чем меньше мольная доля “отстающего” растворителя (растворителя с большим eS). Если в состав элюента входит третий растворитель, возможно формирование третьего фронта. Следует иметь в виду, что даже за последним фронтом состав подвижной фазы отличается от приготавливаемого элюента и только в середине зоны за последним фронтом их можно считать приблизительно одинаковыми. Формирование вторичных фронтов может приводить к неприятным ошибкам в интерпретации хроматограммы: если два разных вещества имеет величины Rf, мало отличающиеся от 0 в первичной зоне, и близкие значения Rf, мало отличающиеся от 1 во вторичной, то они могут образовывать общее пятно непосредственно перед или сразу за вторичным фронтом. Таким образом, смесь двух веществ может быть принята за чистое вещество. Во избежание этих ошибок следует по возможности избегать применения таких элюентов и вводить в их состав растворители с промежуточными значениями eS.
|
|
|
Еще одним осложняющим фактором является отличие состава газовой фазы (парциальных давлений паров растворителей) и, следовательно, насыщенности “сухого” сорбента над линиией фронта, от приготавливаемого состава элюента. В связи с этим, чем сложнее состав элюента, тем сложнее оценить и учитывать все эти эффекты при подборе его и условий проведения ТСХ-анализа.
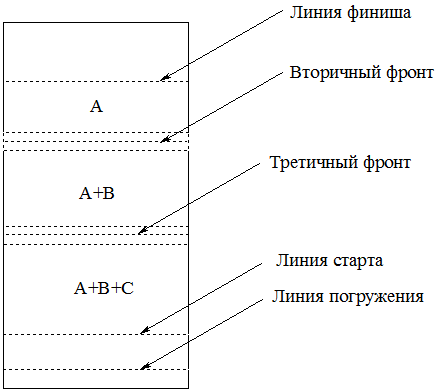
| Рисунок | 6.8 | – Формирование вторичного и третичного фронта |
A – зона (между линией финиша и вторичным фронтом) в которой подвижная фаза состоит только из растворителя A, сорбент насыщен этим растворителем; A+B – зона (между вторичным и третичным фронтами) – в которой элюент состоит из смеси растворителей A и B; A+B+C – зона (между третичным фронтом и линией погружение) – в которой элюент состоит из смеси растворителей A, B и C. Пунктирными линиями ввыше и ниже вторичного и третичного фронтов ограничены зоны в которых в подвижной фазе резко возрастает концентрация растворителя B и C, соответственно.
|
|
|
|
|
|
|
|
Дата добавления: 2014-01-13; Просмотров: 1564; Нарушение авторских прав?; Мы поможем в написании вашей работы!