
КАТЕГОРИИ:
Архитектура-(3434)Астрономия-(809)Биология-(7483)Биотехнологии-(1457)Военное дело-(14632)Высокие технологии-(1363)География-(913)Геология-(1438)Государство-(451)Демография-(1065)Дом-(47672)Журналистика и СМИ-(912)Изобретательство-(14524)Иностранные языки-(4268)Информатика-(17799)Искусство-(1338)История-(13644)Компьютеры-(11121)Косметика-(55)Кулинария-(373)Культура-(8427)Лингвистика-(374)Литература-(1642)Маркетинг-(23702)Математика-(16968)Машиностроение-(1700)Медицина-(12668)Менеджмент-(24684)Механика-(15423)Науковедение-(506)Образование-(11852)Охрана труда-(3308)Педагогика-(5571)Полиграфия-(1312)Политика-(7869)Право-(5454)Приборостроение-(1369)Программирование-(2801)Производство-(97182)Промышленность-(8706)Психология-(18388)Религия-(3217)Связь-(10668)Сельское хозяйство-(299)Социология-(6455)Спорт-(42831)Строительство-(4793)Торговля-(5050)Транспорт-(2929)Туризм-(1568)Физика-(3942)Философия-(17015)Финансы-(26596)Химия-(22929)Экология-(12095)Экономика-(9961)Электроника-(8441)Электротехника-(4623)Энергетика-(12629)Юриспруденция-(1492)Ядерная техника-(1748)
Основное уравнение молекулярно-кинетической теории идеального газа. Давление
|
|
|
|
Модель идеального газа
Основы молекулярно-кинетической теории идеальных газов
Наиболее простой моделью является модель идеального газа. Это газ, состоящий из точечных материальных частиц с конечной массой, силами взаимодействия между которыми можно пренебречь, и которые сталкиваются между собой по законам соударения упругих шаров. Следовательно, молекулы идеального газа обладают только кинетической энергией, поскольку потенциальной энергией взаимодействия молекул можно пренебречь. Молекулы движутся непрерывно и беспорядочно, следовательно, в среднем скорости молекул газа в разных направлениях одинаковы. Тот факт, что частицы точечные, позволяет считать, что газ занимает весь предоставленный ему объём, то есть, любая молекула в любой момент времени может находиться в любом месте предоставленного объёма.
Основное уравнение молекулярно-кинетической теории идеального газа связывает макроскопический параметр газа с микроскопическими характеристиками, относящимися к его структурным элементам - молекулам. Учитывая беспорядочное непрерывное движение молекул и их соударения со стенками сосуда и друг с другом, макроскопическим параметром может быть давление газа, которое связано с изменением импульса молекул (микроскопический параметр).
Как известно, величина давления определяется силой, действующей перпендикулярно на единицу площади поверхности: 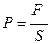 .
.
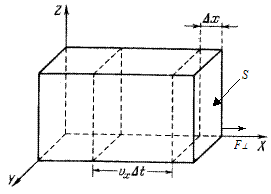 Рис. 2. 2
Рис. 2. 2
|
Давление газа на стенки обусловлено огромным числом столкновений молекул газа со стенками, согласно второму закону Ньютона: 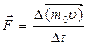
Импульс одной молекулы: вдоль оси Х равен 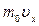 , где m0 - масса одной молекулы. Пусть в единице объема сосуда находится n молекул, из них половина движется вдоль оси Х, а другая половина - в противоположном направлении. За время Dt в слой Dx (Dx – расстояние, на котором проявляется действие молекул на стенку) слева направо входит
, где m0 - масса одной молекулы. Пусть в единице объема сосуда находится n молекул, из них половина движется вдоль оси Х, а другая половина - в противоположном направлении. За время Dt в слой Dx (Dx – расстояние, на котором проявляется действие молекул на стенку) слева направо входит 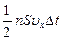 молекул. Каждая из них обладает импульсом
молекул. Каждая из них обладает импульсом 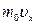 , следовательно, общий импульс, вносимый ими в слой, равен:
, следовательно, общий импульс, вносимый ими в слой, равен: 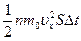 .
.
|
|
|
За это же время слой покидает, двигаясь, справа налево, такое же число молекул с таким же общим импульсом, но противоположного знака. Общее изменение импульса: 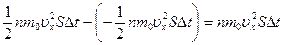 .
.
Импульс силы, действующей на стенку, площадью S, равен изменению импульса частиц 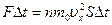 . Тогда давление на стенку, будет определяться формулой:
. Тогда давление на стенку, будет определяться формулой:
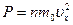 (2.1)
(2.1)
Двигаясь беспорядочно в пространстве, молекулы имеют составляющие скоростей и вдоль других осей. Полная скорость молекулы может быть выражена через её составляющие по трём независимым направлениям: 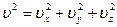 .
.
Поскольку в движении участвует множество молекул, то необходимо использовать средние квадраты скоростей:
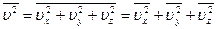 .
.
Так как движение беспорядочное, то все три компоненты скоростей равноправны
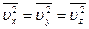 . Отсюда
. Отсюда 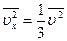 . После подстановки в уравнение (2.1) получим:
. После подстановки в уравнение (2.1) получим: 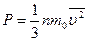 (2.2)
(2.2)
Уравнение (2.2) связывает макроскопический параметр давление и микроскопические – массу и средний квадрат скорости молекулы, поэтому его можно считать основным уравнением МКТ идеальных газов. Однако, часто это уравнение используют в другом виде:  . Здесь
. Здесь  - средняя кинетическая энергия поступательного движения молекулы. Таким образом, давление идеального газа определяется средней кинетической энергией поступательного движения молекулы и является среднестатистической величиной
- средняя кинетическая энергия поступательного движения молекулы. Таким образом, давление идеального газа определяется средней кинетической энергией поступательного движения молекулы и является среднестатистической величиной
 (2.3)
(2.3)
|
|
|
|
Дата добавления: 2014-01-13; Просмотров: 540; Нарушение авторских прав?; Мы поможем в написании вашей работы!