
КАТЕГОРИИ:
Архитектура-(3434)Астрономия-(809)Биология-(7483)Биотехнологии-(1457)Военное дело-(14632)Высокие технологии-(1363)География-(913)Геология-(1438)Государство-(451)Демография-(1065)Дом-(47672)Журналистика и СМИ-(912)Изобретательство-(14524)Иностранные языки-(4268)Информатика-(17799)Искусство-(1338)История-(13644)Компьютеры-(11121)Косметика-(55)Кулинария-(373)Культура-(8427)Лингвистика-(374)Литература-(1642)Маркетинг-(23702)Математика-(16968)Машиностроение-(1700)Медицина-(12668)Менеджмент-(24684)Механика-(15423)Науковедение-(506)Образование-(11852)Охрана труда-(3308)Педагогика-(5571)Полиграфия-(1312)Политика-(7869)Право-(5454)Приборостроение-(1369)Программирование-(2801)Производство-(97182)Промышленность-(8706)Психология-(18388)Религия-(3217)Связь-(10668)Сельское хозяйство-(299)Социология-(6455)Спорт-(42831)Строительство-(4793)Торговля-(5050)Транспорт-(2929)Туризм-(1568)Физика-(3942)Философия-(17015)Финансы-(26596)Химия-(22929)Экология-(12095)Экономика-(9961)Электроника-(8441)Электротехника-(4623)Энергетика-(12629)Юриспруденция-(1492)Ядерная техника-(1748)
Процесс горения
|
|
|
|
ТОПЛИВО ДЛЯ РАКЕТНОГО ДВИГАТЕЛЯ
Как любой двигатель ракетный для работы нуждается в каком-либо источнике энергии. В настоящее время широко используется химическая энергия. Эта энергия может выделяться в реакциях горения (соединения) или разложения различных топлив.
Реакция горения наиболее распространённая, используется в процессах подавляющего большинства тепловых двигателей (ракетные двигатели тоже тепловые). Но для р.д. необходим ещё и запас массы, которая отбрасывалась бы в процессе работы. Эту массу называют рабочим телом.
В ракетном двигателе (р.д.) источником химической энергии служит топливо, а рабочим телом – продукты реакции горения или разложения (например, перекиси водорода).
Возможно применение ядерной энергии. Ядерное топливо будет (носителем) источником энергии, а рабочее тело должно содержаться на борту Л.А. дополнительно.
Под процессом горения понимается химический процесс между двумя веществами – «горючим» и «окислителем», сопровождающийся выделением большого количества тепла.
В реакции горения энергетический уровень атомов определяется строением внешней электронной оболочки атома. На внешней оболочке может находиться определённое число электронов. Для элементов, используемых в топливах ракетных двигателей, предельное число заполнения равно восьми (исключение составляет водород: на внешней оболочке 2 электрона). Заполнение внешней оболочки электронами сопровождается падением энергетического уровня атомов. В случае предельного заполнения внешней оболочки электронами атом обладает минимальным энергетическим уровнем.
В процессе химической реакции горения не происходит изменения строения атомов и общее число электронов в атомах «Г» и «О» элементов остаётся постоянным. Однако при образовании продуктов сгорания происходит взаимное переплетение и такое преобразование электронных оболочек реагирующих атомов, что некоторые электроны оказываются входящими одновременно в оболочки атомов «Г» и «О» элементов.
 Это можно показать на примере образования водяного пара в результате горения Н2 и О2:
Это можно показать на примере образования водяного пара в результате горения Н2 и О2:
При образовании водяного пара в результате горения происходит такое преобразование электронных оболочек, в результате которого две группы по два электрона входят одновременно в оболочки атомов кислорода и водорода. При этом атом кислорода имеет на внешней оболочке восемь электронов, а атомы водорода – по два электрона, т.е. оболочки у всех атомов оказываются предельно заполненными электронами.
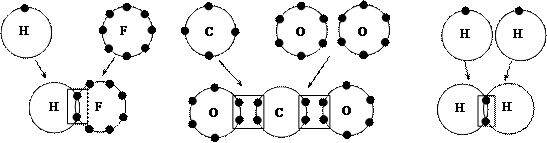 |
Также в молекулах (см. рис. ниже) фтористого водорода (HF), углекислого газа (СО2) и молекулярного водорода (Н2) совместное обладание электронами приводит к тому, что внешние электронные оболочки всех атомов, входящих в продукт реакции, оказываются предельно заполненными электронами. По этой причине энергетический уровень молекулы продукта реакции оказывается ниже, чем энергетический уровень атомов до вступления их в соединение. Разность энергетических уровней определяет величину химической энергии выделяющейся при данной реакции.
Так как элементы «Г» и «О» находятся в составе молекул простых или сложных веществ, то процесс горения с точки зрения выхода энергии представляется происходящим таким образом: вещество, находящееся в молекулярном виде, разлагается до атомов соответствующих элементов с затратой или выделением химической энергии. Затем атомы соединяются в продукты горения всегда с выделением химической энергии.
Общий выход химической энергии определяется алгебраической суммой химических энергий, соответствующих каждому из составляющих процессов.
Химическая энергия, выделяющаяся при реакции горения, может быть определена двумя способами:
1. на основании данных спектрального анализа частиц (атомов и молекул) вычисляются энергетические уровни частиц до и после реакции и по разности находится величина химической энергии;
2. калориметрическим способом определяется теплота образования (она не равна химической энергии, но находится в определённом соответствии с ней).
В калориметре осуществляют необходимую реакцию, в результате которой химическая энергия преобразуется в тепло, тепло расходуется на нагревание продуктов реакции, По окончании реакции продукты горения охлаждаются до температуры, которую имели вещества до реакции. Измеряется количество тепла, отводимое от продуктов реакции, так называемая теплота образования ∆Н.
Разница между ∆Н и химической энергией возникает вследствие того, что запас энергии вещества при горении меняется при одной и той же температуре.
|
|
|
|
|
Дата добавления: 2014-11-06; Просмотров: 967; Нарушение авторских прав?; Мы поможем в написании вашей работы!