
КАТЕГОРИИ:
Архитектура-(3434)Астрономия-(809)Биология-(7483)Биотехнологии-(1457)Военное дело-(14632)Высокие технологии-(1363)География-(913)Геология-(1438)Государство-(451)Демография-(1065)Дом-(47672)Журналистика и СМИ-(912)Изобретательство-(14524)Иностранные языки-(4268)Информатика-(17799)Искусство-(1338)История-(13644)Компьютеры-(11121)Косметика-(55)Кулинария-(373)Культура-(8427)Лингвистика-(374)Литература-(1642)Маркетинг-(23702)Математика-(16968)Машиностроение-(1700)Медицина-(12668)Менеджмент-(24684)Механика-(15423)Науковедение-(506)Образование-(11852)Охрана труда-(3308)Педагогика-(5571)Полиграфия-(1312)Политика-(7869)Право-(5454)Приборостроение-(1369)Программирование-(2801)Производство-(97182)Промышленность-(8706)Психология-(18388)Религия-(3217)Связь-(10668)Сельское хозяйство-(299)Социология-(6455)Спорт-(42831)Строительство-(4793)Торговля-(5050)Транспорт-(2929)Туризм-(1568)Физика-(3942)Философия-(17015)Финансы-(26596)Химия-(22929)Экология-(12095)Экономика-(9961)Электроника-(8441)Электротехника-(4623)Энергетика-(12629)Юриспруденция-(1492)Ядерная техника-(1748)
Основные законы и формулы. И его квантово-механическое описание
|
|
|
|
И его квантово-механическое описание
Атом водорода по Бору
1. Обобщенная формула Бальмера, описывающая серии в спектре излучения атома водорода,
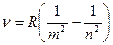 или
или 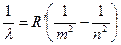 ,
,
где 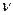 - частота спектральных линий в спектре атома водорода;
- частота спектральных линий в спектре атома водорода;
 – постоянная Ридберга;
– постоянная Ридберга;
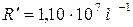 - постоянная Ридберга;
- постоянная Ридберга;
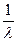 - волновое число;
- волновое число;
m определяет серию 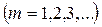 ;
;
n определяет отдельные линии соответствующей серии 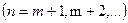 ;
;
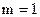 (серия Лаймена),
(серия Лаймена),
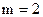 (серия Бальмера),
(серия Бальмера),
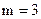 (серия Пашена),
(серия Пашена),
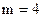 (серия Брэкета),
(серия Брэкета),
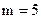 (серия Пфунда),
(серия Пфунда),
 (серия Хэмфри).
(серия Хэмфри).
2. Закон Мозли (спектральные линии характеристического рентгеновского излучения)
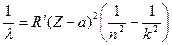 ,
,
где Z-порядковый номер элемента, n = 1,2,3,…; k =(n+1), (n+2),…
а - постоянная экранирования.
Первый постулат Бора (постулат стационарных состояний)
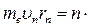 ћ,
ћ, 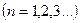
где 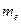 - масса электрона;
- масса электрона; 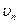 - скорость электрона на n -й орбите радиусом
- скорость электрона на n -й орбите радиусом 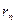 .
.
3. Второй постулат Бора (правило частот)
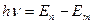 ,
,
где 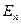 и
и 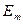 - энергии стационарных состояний атома соответственно до и после излучения (поглощения).
- энергии стационарных состояний атома соответственно до и после излучения (поглощения).
4. Радиус n - й стационарной орбиты в боровской модели атома водорода

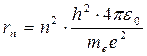 ,
, 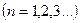
где ħ=h/2 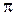 - приведенная постоянная Планка;
- приведенная постоянная Планка;
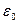 - электрическая постоянная;
- электрическая постоянная;  - масса электрона;
- масса электрона;
e – элементарный заряд.
5. Первый боровский радиус

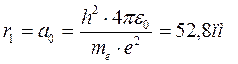
6. Энергия электрона в атоме водорода по Бору
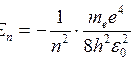
 ,
,
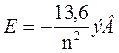

где h - постоянная Планка;
 - масса электрона;
- масса электрона;
e – элементарный заряд.
7. Потенциальная энергия в водородоподобном атоме
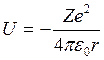 ,
,
где r – расстояние между электроном и ядром;
Z – порядковый номер элемента.
8. Собственное значение энергии электрона в водородоподобном атоме


9. Энергия электрона в атоме водорода при квантово-механическом описании
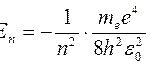

10. Энергия ионизации атома водорода
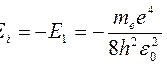
11. Момент импульса (механический орбитальный момент) электрона
|
|
|

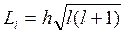 ,
,
где  - орбитальное квантовое число, принимающее при заданном n значения:
- орбитальное квантовое число, принимающее при заданном n значения:  (всего n значений).
(всего n значений).
12. Проекция момента импульса на направление Z внешнего магнитного поля

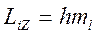 ,
,
где 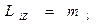 - магнитное квантовое число, принимающее при заданном
- магнитное квантовое число, принимающее при заданном  значения:
значения: 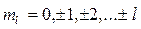 (всего
(всего  значений).
значений).
13. Правило отбора для орбитального и магнитного чисел
 ,
,
 .
.
|
|
|
|
|
Дата добавления: 2014-11-07; Просмотров: 600; Нарушение авторских прав?; Мы поможем в написании вашей работы!