
КАТЕГОРИИ:
Архитектура-(3434)Астрономия-(809)Биология-(7483)Биотехнологии-(1457)Военное дело-(14632)Высокие технологии-(1363)География-(913)Геология-(1438)Государство-(451)Демография-(1065)Дом-(47672)Журналистика и СМИ-(912)Изобретательство-(14524)Иностранные языки-(4268)Информатика-(17799)Искусство-(1338)История-(13644)Компьютеры-(11121)Косметика-(55)Кулинария-(373)Культура-(8427)Лингвистика-(374)Литература-(1642)Маркетинг-(23702)Математика-(16968)Машиностроение-(1700)Медицина-(12668)Менеджмент-(24684)Механика-(15423)Науковедение-(506)Образование-(11852)Охрана труда-(3308)Педагогика-(5571)Полиграфия-(1312)Политика-(7869)Право-(5454)Приборостроение-(1369)Программирование-(2801)Производство-(97182)Промышленность-(8706)Психология-(18388)Религия-(3217)Связь-(10668)Сельское хозяйство-(299)Социология-(6455)Спорт-(42831)Строительство-(4793)Торговля-(5050)Транспорт-(2929)Туризм-(1568)Физика-(3942)Философия-(17015)Финансы-(26596)Химия-(22929)Экология-(12095)Экономика-(9961)Электроника-(8441)Электротехника-(4623)Энергетика-(12629)Юриспруденция-(1492)Ядерная техника-(1748)
Химические свойства. Угольная кислота и карбонаты
Угольная кислота и карбонаты
Будучи 2-х основной кислотой, Н2СО3 диссоциирует ступенчато с образование гидрокарбонат- и карбонат-анионов:
H2CO3 ↔ H+ + HCO3- Кд = 4,5∙10-7 (25°С)
HCO3- ↔ H+ + CO32- Кд = 5,6∙10-11 (25°С)
Угольная кислота существует только в водных растворах, где количество ее молекул и анионов в сотни раз меньше, чем количество растворенных молекул СО2.
Н2СО3 как индивидуальное вещество не имеет никакого значения, но ее соли очень устойчивы и весьма распространены.
Соли угольной кислоты могут быть получены или действием диоксида углерода на щелочи, или путем обменных реакций между растворимыми солями угольной кислоты и солями других кислот. Например:
NаОН + СО2 = NаНСО3
NаНСО3 + NаОН = Nа2СО3 + Н2О
ВаС12 + Nа2СО3 = ВаСО3 ↓+ 2 NаС1
Со слабыми основаниями угольная кислота в большинстве случаев дает только основные соли, примером которых может служить карбонат гидроксомеди (СuОН)2СОз. Встречающийся в природе минерал такого состава называется малахитом.
1) При действии кислот, даже таких слабых, как уксусная, все карбонаты разлагаются с выделением диоксида углерода.
Na2CO3 + 2HCl = 2NaCl + H2O + CO2↑
(NH4)2CO3 + 2CH3COOH = 2CH3COONH4 + CO2↑ + H2O
2) При нагревании все карбонаты, кроме солей щелочных металлов, разлагаются с выделением СО2. Продуктами разложения в большинстве случаев являются оксиды соответствующих металлов. Термическое разложение CaCO3 широко используется для получения негашеной извести и СО2:
СаСО3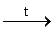 СаО + СО2 ↑
СаО + СО2 ↑
Особенно легко разлагается карбонат аммония:
(NH4)2CO3 = 3NH3↑ + CO2↑ + H2O
3) При пропускании СО2 в растворы карбонатов или при постепенном добавлении к ним кислот происходит образование кислых солей – гидрокарбонатов:
Na2CO3 + CO2 + H2O = 2NaHCO3
Na2CO3 + HCl = NaHCO3 + NaCl
В природе происходит медленное растворение известняков под действием атмосферных осадков и СО2:
CaCO3 + H2O + CO2 = Ca(HCO3)2
4) Растворы карбонатов щелочных металлов вследствие гидролиза имеют сильнощелочную реакцию:
Na2CO3 + H2O ═ NaHCO3 + NaOH
или
CO32ˉ + H2O ═ HCO3ˉ + OH ˉ
5) Все гидрокарбонаты легко растворяются в воде. Гидрокарбонаты металлов при нагревании переходят в карбонаты и гидроксиды металлов:
2 NаНСО3 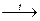 Nа2СO3 + СO2 ↑ + Н2О
Nа2СO3 + СO2 ↑ + Н2О
Ca(HCO3)2 → CaCO3↓ + CO2↑ + H2O
Mg(HCO3)2 → Mg(OH)2↓ + 2CO2↑ + H2O
Исторические и технические названия некоторых карбонатов
| Формула соли | Названия |
| Na2CO3∙10H2O | Кристаллическая сода |
| Na2CO3 | Кальцинированная сода |
| NaHCO3 | Питьевая сода |
| K2CO3 | Поташ |
| CaCO3 | Кальцит, известняк, мел, мрамор |
| MgCO3 | Магнезит |
| CaCO3∙MgCO3 | Доломит |
| (CuOH)2CO3 | Малахит, основной карбонат меди |
| FeCO3 | Шпатовый железняк |
|
|
Дата добавления: 2014-10-15; Просмотров: 4094; Нарушение авторских прав?; Мы поможем в написании вашей работы!