
КАТЕГОРИИ:
Архитектура-(3434)Астрономия-(809)Биология-(7483)Биотехнологии-(1457)Военное дело-(14632)Высокие технологии-(1363)География-(913)Геология-(1438)Государство-(451)Демография-(1065)Дом-(47672)Журналистика и СМИ-(912)Изобретательство-(14524)Иностранные языки-(4268)Информатика-(17799)Искусство-(1338)История-(13644)Компьютеры-(11121)Косметика-(55)Кулинария-(373)Культура-(8427)Лингвистика-(374)Литература-(1642)Маркетинг-(23702)Математика-(16968)Машиностроение-(1700)Медицина-(12668)Менеджмент-(24684)Механика-(15423)Науковедение-(506)Образование-(11852)Охрана труда-(3308)Педагогика-(5571)Полиграфия-(1312)Политика-(7869)Право-(5454)Приборостроение-(1369)Программирование-(2801)Производство-(97182)Промышленность-(8706)Психология-(18388)Религия-(3217)Связь-(10668)Сельское хозяйство-(299)Социология-(6455)Спорт-(42831)Строительство-(4793)Торговля-(5050)Транспорт-(2929)Туризм-(1568)Физика-(3942)Философия-(17015)Финансы-(26596)Химия-(22929)Экология-(12095)Экономика-(9961)Электроника-(8441)Электротехника-(4623)Энергетика-(12629)Юриспруденция-(1492)Ядерная техника-(1748)
Дослід 70. Бромування фенолу
|
|
|
|
Дослід 69.Утворення і розклад фенолятів.
Дослід 68. Реакція фенолів з хлоридом феруму (ІІІ).
ФЕНОЛИ І АРОМАТИЧНІ СПИРТИ
Лабораторна робота № 16
Дослід 67. Сульфування ароматичних вуглеводнів.
Реактиви: бензен, толуен,ксилен, концентрована сульфатна кислота.
Обладнання: хімічні стакани (50-100 мл), зворотні повітряні холодильники до пробірок, водяні бані.
В три пробірки наливають по 1мл бензену, тулуену і ксилену. В кожну пробірку додають по 4 мл концентрованої сульфатної кислоти. Пробірки закривають пробками з зворотними повітряними холодильниками і нагрівають на киплячій водяній бані, часто струшуючі реакційну суміш. В деяких пробірках спостерігається поступове розчинення вуглеводню. Коли це розчинення завершиться, пробірки охолоджують і їх вміст виливають в стакани, що містять 20 мл води.
Відмітьте вигляд суміші, що утворилася. Чи в усіх стаканах відбулося розчинення реакційної маси? Що виділяється: продукт реакції чи вихідний вуглеводень? Зробіть висновок щодо легкості сульфування різних ароматичних вуглеводнів. Поясніть механізм реакції
(Обережно! Феноли викликають опіки шкіри!)
Реактиви: 5%-й розчин фенолу, 5%-й розчин м- крезолу, 5%-й розчин п- крезолу, 5%-й розчин хлориду феруму (ІІІ).
Дослід проводять з кожним з фенолів. В пробірки наливають по 1 мл розчину відповідного фенолу і додають 1-2 краплі розчину хлориду феруму (ІІІ). З’являється інтенсивне забарвлення: для фенолу – фіолетове, для м- крезолу – червоно-фіолетове, для п- крезолу – темно-синє.
Реактиви: фенол, 2 н. розчин гідроксиду натрію, 2 н. розчин карбонату натрію, 2 н. розчин сульфатної кислоти, 2 н. розчин гідрокарбонату натрію.
|
|
|
а) До 0,1-0,2 г фенолу добавляють 1-2 мл розчину гідроксиду натрію. Поступово фенол розчиняється. Суміш нагрівають до одержання однорідної рідини. До охолодженого розчину приливають розведену сульфатну кислоту. Спостерігається помутніння розчину.
Напишіть рівняння реакції утворення феноляту натрію. Поясніть причину помутніння суміші при взаємодії з сульфатною кислотою.
б) Для проведення досліду в дві пробірки поміщають по 0,1-0,3 г фенолу. В одну пробірку приливають 1-2 мл розчину карбонату натрію, а в другу – такий же об’єм гідрокарбонату натрію. Чи в обох пробірках спостерігається розчинення фенолу і утворення однорідної рідини? Про що свідчить цей дослід? Напишіть рівняння реакції карбонату натрію з фенолом. Які властивості проявляє фенол при взаємодії з лугами і карбонатом натрію?
Реактиви: фенол (насичений розчин), бромна вода.
Обладнання: піпетки.
В пробірку наливають 1 мл насиченого водного розчину фенолу і при струшуванні по краплях додають бромну воду. Розчин знебарвлюється і випадає білий осад. При додаванні надлишку бромної води осад перетворюється в жовтий:
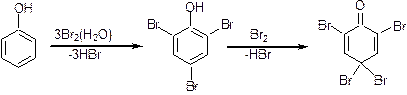
Фенол 2,4,6-трибромфенол трибромфенолбром
(Білий) (2,4,4,6-тетрабромцикло-
-гексадієнон) (Жовтий)
Фенол містить сильний електронодонорний замісник (групу –ОН), яка має сильно виражений +М-ефект і підвищує активність ароматичного ядра до реакцій електрофільного заміщення (SE). Бромування відбувається при кімнатній температурі зразу в положення 2-,4- і 6. Надлишок бромної води окислює трибромфенол до 2,4,4,6-тетрабромциклогексадієнону.
Порівняйте легкість бромування фенолу і бензену.
Дослід 71. Нітрування фенолу (одержання і властивості орто- і пара- нітрофенолів).
Реактиви: фенол, концентрована нітратна кислота, концентрована хлоридна кислота, 2 н. розчин гідроксиду натрію, насичені водні розчини о- і п- нітрофенолів.
|
|
|
Обладнання: вигнуті газовідвідні трубки, піпетки.
а) В пробірку з 1-1,5 г фенолу додають декілька крапель води до розчинення фенолу і утворення однорідної рідини. В другій пробірці змішують 2 мл концентрованої нітратної кислоти з 2 мл води. Одержану розведену нітратну кислоту повільно додають краплями (при струшуванні і охолодженні) до суміші фенолу і води, підтримуючи температуру 20-25оС. Через 15 хвилин темну рідину, що утворилась, виливають в 15 мл води. Після відстоювання суміші воду зливають, а напіврідку масу, що відокремилась, ще раз промивають 15 мл води, потім масло переливають у велику пробірку, додають 5-7 мл води, 2-3 кип’ятильника і закривають пробірку пробкою з вигнутою газовідвідною трубкою. Вільний кінець газовідвідної трубки опускають в пробірку-приймач, який охолоджується крижаною водою. Обережно прогрівають вміст пробірки з продуктом реакції, відгонюють в приймач суміш води з орто- нітрофенолом, який застигає у вигляді жовтих кристалів.
Напишіть рівняння реакції нітрування фенолу і розгляньте її механізм.
б) Взаємодія нітрофенолів з гідроксидом натрію. По декілька крапель насичених розчинів орто- і пара- нітрофенолу поміщають в дві пробірки і в кожну з них приливають розчин гідроксиду натрію до лужної реакції, а потім розведеної сульфатної кислоти.
Як змінюється забарвлення нітрофенолів в присутності лугу? Чим пояснити таку сильну зміну забарвлення? Які зміни відбуваються при підкисленні лужних розчинів нітрофенолів?
|
|
|
|
|
Дата добавления: 2014-11-09; Просмотров: 4815; Нарушение авторских прав?; Мы поможем в написании вашей работы!