
КАТЕГОРИИ:
Архитектура-(3434)Астрономия-(809)Биология-(7483)Биотехнологии-(1457)Военное дело-(14632)Высокие технологии-(1363)География-(913)Геология-(1438)Государство-(451)Демография-(1065)Дом-(47672)Журналистика и СМИ-(912)Изобретательство-(14524)Иностранные языки-(4268)Информатика-(17799)Искусство-(1338)История-(13644)Компьютеры-(11121)Косметика-(55)Кулинария-(373)Культура-(8427)Лингвистика-(374)Литература-(1642)Маркетинг-(23702)Математика-(16968)Машиностроение-(1700)Медицина-(12668)Менеджмент-(24684)Механика-(15423)Науковедение-(506)Образование-(11852)Охрана труда-(3308)Педагогика-(5571)Полиграфия-(1312)Политика-(7869)Право-(5454)Приборостроение-(1369)Программирование-(2801)Производство-(97182)Промышленность-(8706)Психология-(18388)Религия-(3217)Связь-(10668)Сельское хозяйство-(299)Социология-(6455)Спорт-(42831)Строительство-(4793)Торговля-(5050)Транспорт-(2929)Туризм-(1568)Физика-(3942)Философия-(17015)Финансы-(26596)Химия-(22929)Экология-(12095)Экономика-(9961)Электроника-(8441)Электротехника-(4623)Энергетика-(12629)Юриспруденция-(1492)Ядерная техника-(1748)
Контрольная работа №1
|
|
|
|
Методические указания к контрольным работам по дисциплине физическая и коллоидная химия.
Данные методические указания составлены на основе рабочей программы по специальности 240134 «Переработка нефти и газа» в соответствии ФГОС-03. Методические указания не включают весь курс дисциплины. Поэтому, при изучении тем разделов необходимо пользоваться учебным пособием.
В методические указания входят примеры решения типовых задач и вопросы для самоконтроля студентов для усвоения и закрепления знаний, умений и навыков.
Для контроля знаний студентов – заочников проводится одна контрольная работа. Она состоит из 10 вариантов по 8 заданий в каждом варианте.
Каждый студент выполняет только свой вариант. Номер варианта соответствует списочному составу группы. Работа, выполненная не по своему варианту, не рецензируется.
Контрольная работа должна выполняться в тетради с полями, в конце работы оставлять 1 страницу для рецензии. Написание контрольной работы допускается только синий или фиолетовой ручкой.
Каждая контрольная задача начинается с новой страницы, выписывается полностью условие задачи, делается краткая запись условия задания, перевод параметров в систему СИ, решение, ответ. Решение задач необходимо сопровождать кратким пояснением (по какому уравнению или закону решается данная задача). Вычисления излагаются подробно. Все справочные данные указаны в конце методических рекомендаций в приложениях.
Задания для контрольных работ
Вариант № 1
Задача 1
2,00 ×10-4кг вещества, испарившись при 22°C и 405 мм.рт.ст., заняло объём в 9,5 × 10-5 м3. Какова молярная масса этого вещества? Определить плотность его паров при 25°С и давление 745 мм.рт.ст.
|
|
|
Задача 2
Определить изохорный тепловой эффект реакции, если изобарный тепловой эффект равен 314,22 кДж/моль при 25°С
NH4ClГ = NН3 + HCl
Задача 3
Вычислить тепловой эффект реакции, являющейся частью технологического процесса, если она протекает по уравнению:
2СН4Г ® С2Н4Г + 2Н2Г при 1450°С
Задача 4
Вычислить на сколько градусов необходимо повысить температуру, чтобы скорость реакции возросла в 50 раз, если температурный коэффициент скорости реакции равен 3.
Задача 5
В какую сторону сместиться равновесие реакции СО + 2Н2 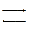 СН3ОНГ + 113 кДж
СН3ОНГ + 113 кДж
а) при повышении Т;
б) при понижении Р.
Задача 6
Для реакции РCl3 + Cl2 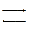 PCl5
PCl5
при 500 К Кр = 2,962×10-5. Будет ли происходить образование PCl5 в газовой смеси, если даны парциальные давления веществ?
Р (PCl3) = 101325 Па
P (PCl5) = 50662,5 Па
Р (Сl2) = 202650 Па.
Задача 7
Рассчитать состав пара при 30°С в молярных долях над смесью бензола и толуола, содержащих 0,6 молярных долей бензола. При 30°С давление пара чистого бензола 15756 Па, а толуола 4892 Па.
Задача 8
Вычислить потенциал серебряного электрода в 1моляльном растворе AgNO3 при 25°С.
Вариант № 2
Задача 1
Плотность оксида углерода CO при 800°C равно 7,1 кг/м3.Определить концентрацию и давление.
Задача 2
Температура реактора синтеза винилхлорида равна 200°С за счёт теплоотвода охлаждающим маслом. Определить расход масла на 1 кг продукта, если при образовании 1 кг винилхлорида выделяется теплота 112 кДж/кг, температура масла повышается от 20 до 180°С, теплоёмкость масла равна 2,6 кДж/кг×К.
Задача 3
Вычислить тепловой эффект реакции, являющейся частью технологического процесса, если она протекает по уравнению:
2CH4Г + O2Г ® 2CH3OHГ при 520°С
Задача 4
В результате осуществления кругового процесса получена работа, равная 70 кДж, а отдано холодильнику 47 кДж теплоты. Определить КПД тепловой машины и количество теплоты, сообщённое рабочему телу от нагревателя.
|
|
|
Задача 5
Во сколько раз увеличится скорость прямой реакции 2SO2 + O2 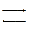 2SO3, протекающей в закрытом сосуде, если увеличить давление в 5 раз без изменения температуры.
2SO3, протекающей в закрытом сосуде, если увеличить давление в 5 раз без изменения температуры.
Задача 6
Изменением каких факторов можно осуществить сдвиг равновесия вправо для реакции: 2СО + 2Н2 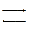 СН4 + СО2 + Q.
СН4 + СО2 + Q.
Задача 7
Вычислить молярную массу уксусной кислоты в эфире, если при 30°С давление пара раствора, содержащего 120 г уксусной кислоты в 740 г эфира (С2Н5)2О равно 90000 Па, а давление чистого эфира при той же t° равно 9,2×104 Па.
Задача 8
Вычислить потенциал цинкового электрода, погружённого в 0,1 моляльный раствор ZnSO4, и потенциал этого же электрода при разбавлении раствора в 10 раз (t = 25°С).
Вариант № 3
Задача 1
Плотность воздуха при н.у. 1,293 кг/м3. Какова его плотность при 273 К и 742 мм рт. ст.
Задача 2
Определить расход воды для охлаждения 2000 кг бутанола от 100 до 60°С, если температура воды в теплообменнике при этом повышается от 20 до 70°С, если сm (бутанола) = 125 Дж/(моль×К), а температурная зависимость воды выражается линейным уравнением:
сm = 39,02 + 76,64×10-3Т (Дж/моль×К).
Задача 3
Вычислить тепловой эффект реакции, являющейся частью технологического процесса, если она протекает по уравнению:
CH4Г + О2Г ® НСНОГ + Н2О при 520°С
Задача 4
Выяснить возможность протекания данной реакции при стандартных условиях по стандартной энергии Гиббса
4Al + 3SiO2 ® 3Si + 2Al2O3
Задача 5
Константа скорости омыления этилацетата едким натром при 9,4°С равна 2,37, а при 14,4°С равна 3,204. Рассчитать температурный коэффициент и энергию активации.
Задача 6
Изменением каких факторов можно осуществить сдвиг равновесия вправо для реакции:
MgCO3ТВ 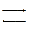 MgOТВ + СО2 - Q
MgOТВ + СО2 - Q
Задача 7
0,5 моляльный водный раствор сульфата алюминия замерзает при t = – 4,19°С. Определить степень диссоциации. Кк(Н2О)=1,85
Задача 8
Вычислить при 25°С ЭДС элемента, образованного цинковым электродом погружённым в 0,05 моляльный раствор ZnSO4, и медным элетродом, погруженным в 0,02 моляльный раствор CuSO4.
Вариант № 4
Задача 1
При давлении 2,026×105 Па и 0°С концентрация азота 0,08944 кмоль/м3. Вычислить, при какой температуре и том же давлении масса 3 м3 азота будет равна 8,4 кг.
Задача 2
В баллоне вместимостью 20л при 18°С находится смесь из 28 кг кислорода и 24 г аммиака. Определить парциальные давления каждого из газов и общее давление смеси.
|
|
|
Задача 3
Определить расход тепла на разогревание 3000 кг магнетитовой руды от 20 до 1200°С, если состав Fe3O4, если теплоёмкость выражается линейным уравнением
сР,m = 86,27 + 208,92×10-3T (Дж/моль×К)
Задача 4
Вычислить тепловой эффект реакции, являющейся частью технологического процесса, если она протекает по уравнению:
CH4Г + 2Н2ОГ ® СО2Г + 4Н2Г при 825°С
Задача 5
При нагревании оксида азота (IV) в закрытом сосуде до некоторой t° равновесие реакции 2NO2 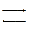 2NО + O2
2NО + O2
устанавливается при концентрации NO2 0,3 моль/л NО 1,2 моль/л, O2 0,6 моль/л. Вычислить константу равновесия реакции для этой температуры и исходную концентрацию оксида азота (IV).
Задача 6
В какую сторону сместиться равновесие реакции N2 + О2 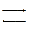 2NО – 181 кДж.
2NО – 181 кДж.
а) при повышении Т;
б) при понижении Р.
Задача 7
Сколько граммов этилового спирта С2Н5ОН необходимо растворить в 200 см3 воды, чтобы осмотическое давление раствора при 17°С было 2,026×105 Па
Задача 8
При электролизе раствора Сr(NO3)3 в течение 12 мин на катоде выделится 0,29 г хрома. Вычислить силу тока.
Вариант № 5
Задача 1
Плотность паров вещества при 25°С и 70 мм.рт.ст. равна 1,85 кг/м3. Какова молярная масса этого вещества?
Задача 2
Под давлением 1,325×106 Па 200г воздуха занимает объём 80л. Определить произведённую воздухом работу, если объём его при Р = const увеличится в 2 раза.
Задача 3
Вычислить тепловой эффект реакции, являющейся частью технологического процесса, если она протекает по уравнению:
2СН4Г + 3О2Г ® 2НСООНГ + 2Н2ОГ при 520°С
Задача 4
Выяснить возможность получения пропена из пропанола по стандартной энергии Гиббса для реакции:
С3Н7ОНж ® С3Н6Г + Н2Ож
Задача 5
Константа равновесия КР реакции СО + Cl2 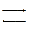 COCl2 при 600°С равна 1,67×10-6. Вычислить КС реакции при этой же температуре.
COCl2 при 600°С равна 1,67×10-6. Вычислить КС реакции при этой же температуре.
Задача 6
Изменением каких факторов можно осуществить сдвиг равновесия вправо для реакции:
4HClГ + О2 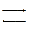 2Н2ОПАР + 2Сl2 + Q
2Н2ОПАР + 2Сl2 + Q
Задача 7
Определить осмотическое давление 0,3 молярного раствора ZnSO4 при 27°С. Степень диссоциации ZnSO4 40%.
Задача 8
Какое количество фенола можно извлечь из 100 мл водного раствора, содержащего 8 г фенола, экстракцией 50 мл амиловым спиртом. Коэффициент распределения = 0,0667.
|
|
|
Вариант № 6
Задача 1
Рассчитать парциальное давление и молярные концентрации компонентов газовой смеси ниже приведённого состава, если её температура 300°С, давление 2,5×106 Па:
С6Н6 = 47,5; С3Н6 = 15,8; С3Н8 = 36,7 (об %).
Задача 2
Вычислить по формуле Коновалова теплоту сгорания 1 моля коричного альдегида
| O // 2C6H5-CH=CH-C \ H | + 21O2 ® | 18CO2 + 8H2O |
Задача 3
Вычислить тепловой эффект реакции, являющейся частью технологического процесса, если она протекает по уравнению:
СН4Г + СО2Г ® 2СОГ + 2Н2Г при 850°С.
Задача 4
При низких температурах (стандартных условиях) серная кислота устойчива, а при высоких температурах диссоциирует
Н2SO4Ж ® Н2ОЖ + SO3Г.
Рассчитать температуру, при которой реакция возможна
Задача 5
В растворе, содержащем 1 моль хлорида олова (II) и 2 моль хлорида железа (III) протекает по уравнению SnCl2 + 2FeCl3 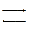 SnCl4 + 2FeCl2.
SnCl4 + 2FeCl2.
Во сколько раз уменьшиться скорость прямой реакции после того, как прореагирует 0,65 моль SnCl2.
Задача 6
Изменением, каких факторов можно осуществить сдвиг равновесия вправо для реакции:
С2Н2 + СО + 2Н2 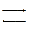 С3Н6ОГ
С3Н6ОГ
Задача 7
В 115,8 г воды содержится 34,2 г тростникового сахара С12Н22О11. Вычислить давление пара этого раствора при 30°С, если давление пара воды при 30°С равно 4242,3 Па.
Задача 8
Вычислить ЭДС гальванического элемента при 25°С:
Cd | CdSO4 ║ZnSO4 | Zn
m1 m2
Моляльная концентрация сульфата кадмия в растворе m 1 равна
0,1 моль/1 кг Н2О, а сульфата цинка 0,2, моль/1 кг Н2О
Вариант № 7
Задача 1
Определить, во сколько раз увеличится объём оболочки стратостата при подъёме, если температура при старте была – 10°С, давление 1,02×105 Па, на высоте 22 км температура стала – 55°С, а давление 5332 Па.
Задача 2
Какое количество теплоты потребуется для нагревания 100 м3 от 100°С до 200°С при нормальном давлении, если температурная зависимость объёмной теплоёмкости выражается формулой: соб = 1,62 + 3,56×10-3Т (кДж/(м3×К))
Задача 3
Тепловой эффект реакции N2 + 3H2 = 2NH3 при Р = const равен 46,26 кДж/моль при 25°С. Определить Qv.
Задача 4
Вычислить тепловой эффект реакции, являющейся частью технологического процесса, если она протекает по уравнению:
CH4Г ® С(графит) + 2Н2Г при 1450°С
Задача 5
Вычислить по правилу Вант – Гоффа константу скорости разложения йодистого водорода при 400°С, если при t = 360°С она равна 2,82×10-4, а температурный коэффициент скорости реакции равен 2.
Задача 6
В какую сторону сместиться равновесие реакции NH4ClТВ 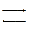 NH3Г + НСl – QX
NH3Г + НСl – QX
а) при повышении Т;
б) при повышении Р.
Задача 7
Осмотическое давление 0,125 моль/л раствора бромида калия равна 5,63×105 Па при 25°С. Определить степень диссоциации KBr.
Задача 8
Определить молярную массу растворённого вещества (неэлектролита), если раствор, содержащий 9,2 г растворённого вещества в 100 г воды, замерзает при температуре – 3,72°С, КК(Н2О) = 1,85.
Вариант № 8
Задача 1
При н.у. объём газа равен 100 м3. До какой температуры нужно нагреть этот газ, чтобы при 9,852×104 Па объём его стал равен 122 м3?
Задача 2
Промышленный способ получения 1,2 дихлорэтана основан на хлорировании этилена.
С2Н4 + Сl2 ® 1,2C2H4Cl2
Теплота образования продукта равна – 217,32 кДж/моль. Каким должен быть теплосъём (теплота) с реактора, рассчитанного на производство 5,0 тонн в час дихлорэтана?
Задача 3
Вычислить тепловой эффект реакции, являющейся частью технологического процесса, если она протекает по уравнению:
2СН4Г + О2Г ® 2СОГ + 4Н2Г при 1400°С
Задача 4
При низких температурах (стандартных условиях) окисление азота кислородом
N2Г + О2Г ® 2NOГ
не происходит, а при высоких температурах эта реакция идёт самопроизвольно. Определить температуру, выше которой эта реакция может быть использована в химической технологии
Задача 5
При нагревании водорода и йода в закрытом сосуде до 444°С протекает реакция
Н2 + I2 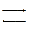 2HI.
2HI.
Равновесная смесь состоит из 9,48 моль НI; 0,56 моль I2 и 3,2 моль водорода. Вычислить константу равновесия данной реакции при 444°С, определить исходные концентрации водорода и йода.
Задача 6
Изменением, каких факторов можно осуществить сдвиг равновесия вправо для реакции:
Н2 + I2(Г) 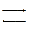 2НI – 52кДж
2НI – 52кДж
Задача 7
Рассчитать Т кристаллизации хладагента, приготовленного смешением 6л глицерина с 20л Н2О. r глицерина = 1,26×103 кг/м3, r воды = 1×103 кг/м3, КК (Н2О) = 1,85.
Задача 8
Осмотическое давление 0,2 молярного раствора NaCl равно 6×105 Па при 25°С. Определить степень диссоциации.
Вариант № 9
Задача 1
При 39°С и давлении 98740 Па масса 640 см3 газа равна 1,73 г. Вычислить молярную массу газа и его плотность.
Задача 2
Определить по формуле Коновалова теплоту сгорания 1 моля метана
2CH4Г + 3O2 ® 2HCOOH + 2H2O
Задача 3
Вычислить тепловой эффект реакции, являющейся частью технологического процесса, если она протекает по уравнению:
CH4Г + О2Г ® СОГ + Н2ОГ + Н2Г при 1500°С
Задача 4
Определить изменение энтропии при охлаждении 5 моль алюминия от 0 до – 100°С, если теплоёмкость в указанном интервале равна сР = 812,9 Дж/кг×К.
Задача 5
Разложение оксида азота на поверхности золота при высоких температурах протекает по уравнению N2O 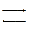 N2 + O
N2 + O
Константа скорости данной реакции при 900°С равна 5×10-4. Начальная концентрация N2O 3,2 моль/л. Определить скорость реакции при данной t° в начальный момент и когда прореагирует 78% начального количества оксида.
Задача 6 Изменением каких факторов можно осуществить сдвиг равновесия вправо для реакции:
NH4ClТВ 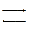 NH3Г + НСlГ – Q
NH3Г + НСlГ – Q
Задача 7
0,3 моляльный раствор сульфата аммония замерзает при – 1°С. Определить степень диссоциации. КК(Н2О) = 1,85.
Задача 8
Коэффициент распределения йода между амиловым спиртом и водой равен 230. Исходный раствор – амиловый спирт, объёмом 0,4 л, содержащий 2,5 г йода. Экстрагент – вода, объёмом 1л. Определить количество йода, перешедшее в водный слой.
Вариант № 10
Задача 1
Определить, во сколько раз увеличится объём оболочки стратостата при подъёме, если температура при старте была – 10°С, давление 1,02×105 Па, на высоте 22 км температура стала – 55°С, а давление 5332 Па.
Задача 2
Какую работу могут совершить 12 кг водорода при повышении температуры на 12К при Р = const?
Задача 3
Вычислить тепловой эффект реакции, являющейся частью технологического процесса, если она протекает по уравнению:
2CH4Г + 2NH3Г + 3О2Г ® 2НСNГ + 6Н2ОГ при 1000°С
Задача 4
Определить изменение энтропии 5 кг магнетитовой руды (Fe3O4) при нагревании от 25°С до 150°С, если сР,m = 150,79 Дж/моль×К.
Задача 5
Муравьиная кислота разлагается на диоксид углерода и водород на поверхности золота. Константа скорости этой реакции при 140°С равна 5,5×10-4, а при 180°С равна 9,2×10-3. Вычислить температурный коэффициент скорости реакции в указанном интервале температур.
Задача 6
В какое сторону сместится равновесия реакции 2Н2S 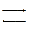 2Н2 + S2 (пар) – 42кДж
2Н2 + S2 (пар) – 42кДж
а) при понижении Т;
б) при увеличении концентрации [H2S]
Задача 7
Осмотическое давление 0,2 молярного раствора NaCl равно 6×105 Па при 25°С. Определить степень диссоциации.
Задача 8
Медный электрод погружён в 0,1 моляльный раствор CuSO4, а таллиевый – 0,01 моляльный раствор TlCl. Вычислить ЭДС гальванического элемента из указанных электродов при 25°С. Учесть коэффициенты активности γ± электролитов при заданных температуре и концентрациях солей в растворах
Приложения
Приложение 1
|
|
|
|
|
Дата добавления: 2014-11-18; Просмотров: 2693; Нарушение авторских прав?; Мы поможем в написании вашей работы!