
КАТЕГОРИИ:
Архитектура-(3434)Астрономия-(809)Биология-(7483)Биотехнологии-(1457)Военное дело-(14632)Высокие технологии-(1363)География-(913)Геология-(1438)Государство-(451)Демография-(1065)Дом-(47672)Журналистика и СМИ-(912)Изобретательство-(14524)Иностранные языки-(4268)Информатика-(17799)Искусство-(1338)История-(13644)Компьютеры-(11121)Косметика-(55)Кулинария-(373)Культура-(8427)Лингвистика-(374)Литература-(1642)Маркетинг-(23702)Математика-(16968)Машиностроение-(1700)Медицина-(12668)Менеджмент-(24684)Механика-(15423)Науковедение-(506)Образование-(11852)Охрана труда-(3308)Педагогика-(5571)Полиграфия-(1312)Политика-(7869)Право-(5454)Приборостроение-(1369)Программирование-(2801)Производство-(97182)Промышленность-(8706)Психология-(18388)Религия-(3217)Связь-(10668)Сельское хозяйство-(299)Социология-(6455)Спорт-(42831)Строительство-(4793)Торговля-(5050)Транспорт-(2929)Туризм-(1568)Физика-(3942)Философия-(17015)Финансы-(26596)Химия-(22929)Экология-(12095)Экономика-(9961)Электроника-(8441)Электротехника-(4623)Энергетика-(12629)Юриспруденция-(1492)Ядерная техника-(1748)
Реальные газы
|
|
|
|
Ур-я Максвелла, которые позволяют осуществить преобразования т.д. соотношений, выраженных не через измеряемые параметры в выр-я через параметры которые могут быть измерены экспериментальным путем.
Основные дифференциальные соотношения термодинамики
Объединенное ур-е I и II закона т.д. имеет следующий вид
Tds = du + dl = du + pdu; du = Tds - pdu (1)
Для получения основных дифференциальных соотношений, воспользуемся одним из основных св-в высшего порядка. В соответствии с св-вом, величина производной не зависит от порядка дифференцирования. Для любой производной 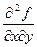 =
= 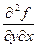 ;
;
запишем (1) следующим образом (x,y – любая пара параметров P,V,T,S, u = f(x)):
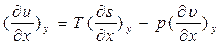
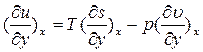
найдем смежные производные
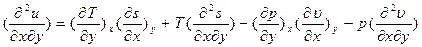
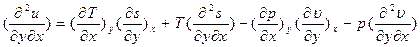
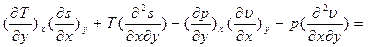
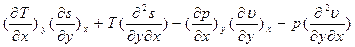
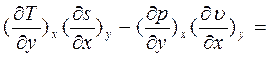
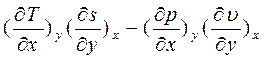
Рассмотрим полученное выр-е для первой пары параметров: x= p, y = s;
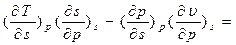
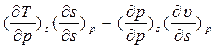
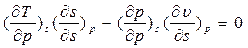 =>
=> 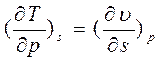
Лекция №6
Частные производные внутренней энергии и энтропии
Воспользуемся ур-ями первого и второго законов термодинамики для получения основных дифференциальных соотношений между параметрами состояния:
dq = du + pdu = Tds
du = Tds - pdu
При T = const, это ур-е может быть записано:
(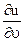 )T = T(
)T = T(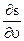 )T – p изменим на (
)T – p изменим на (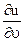 )T = T(
)T = T(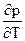 )u - p
)u - p
Аналогично установим зависимость между изменением внутренней энергии рабочего тела и давлением в изотермическом процессе
( )T = T(
)T = T(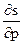 )T - p(
)T - p(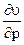 )T
)T
Из 3-го ур-я Максвелла подставляем
( )T = - T(
)T = - T(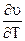 )p - p(
)p - p(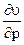 )T (
)T (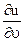 )T = T(
)T = T(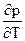 )u - p
)u - p
pu = RT
u = const; udp = RdT
(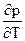 )u =
)u =  (
(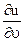 )T = T
)T = T  - p = 0.
- p = 0.
Получим аналогично основные дифференциальные соотношения для энтальпии любого газа
h = u + pu
dh = du + d(pu) = du + pdu + udp = dq + udp = Tds + udp
(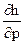 )T = T(
)T = T(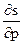 )T +u; (
)T +u; (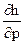 )T = u - T(
)T = u - T(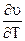 )p; (
)p; (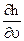 )T = T(
)T = T(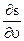 )T + u (
)T + u (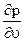 )T;
)T;
(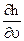 )T = T(
)T = T(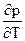 )u + u (
)u + u (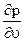 )T;
)T;
Рабочие тела в различных теплоэнергетических установках обычно по своим свойствам не являются идеальными газами. Это связано с тем, что давление рабочих тел достаточно велико, а температура близка к температурам фазовых превращений. В этом случае нельзя пренебречь собственным объемом между молекулами и силами взаимодействия между ними. А ошибка, получаемая в результате использования уравнения Менделеева-Клапейрона может достигать 20-30%. Реальные свойства газа могут быть оценены по величине коэффициента сжимаемости:
|
|
|


 Z =
Z = 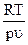 Z реальный газ
Z реальный газ

идеальный газ
 |
Водяной пар является основным рабочим телом в теплоэнергетических установках. Его применение обусловлено следующим:
1. Вода широко распространена.
2. Вода безвредна для окружающей среды и персонала.
3. Вода характеризуется большим отношением удельным объемом в газообразном состоянии
Простейшим ур-им состояния реального газа является ур-е Вандервальса
(P + 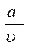 ) × (u - b) = RT
) × (u - b) = RT
Это уравнение является уравнением третьей степени относительно удельного объема и поэтому должно иметь три корня. Возможны следующие варианты:
1. Все три корня действительные и разные.
2. Все три корня действительные и равные между собой.
3. Один корень действителен и два мнимых.
Рассмотрим кривые изотермического сжатия реального газа, построенные в соответствии уравнением Ван-дер-Ваальса:

 p
p
 K
K
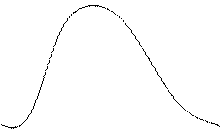
 I c’’ Т > Tкр
I c’’ Т > Tкр

 b’’ a’’ T = Tкр
b’’ a’’ T = Tкр
 b’ Т1
b’ Т1
|
|
|
|
|
Дата добавления: 2014-11-18; Просмотров: 413; Нарушение авторских прав?; Мы поможем в написании вашей работы!