
КАТЕГОРИИ:
Архитектура-(3434)Астрономия-(809)Биология-(7483)Биотехнологии-(1457)Военное дело-(14632)Высокие технологии-(1363)География-(913)Геология-(1438)Государство-(451)Демография-(1065)Дом-(47672)Журналистика и СМИ-(912)Изобретательство-(14524)Иностранные языки-(4268)Информатика-(17799)Искусство-(1338)История-(13644)Компьютеры-(11121)Косметика-(55)Кулинария-(373)Культура-(8427)Лингвистика-(374)Литература-(1642)Маркетинг-(23702)Математика-(16968)Машиностроение-(1700)Медицина-(12668)Менеджмент-(24684)Механика-(15423)Науковедение-(506)Образование-(11852)Охрана труда-(3308)Педагогика-(5571)Полиграфия-(1312)Политика-(7869)Право-(5454)Приборостроение-(1369)Программирование-(2801)Производство-(97182)Промышленность-(8706)Психология-(18388)Религия-(3217)Связь-(10668)Сельское хозяйство-(299)Социология-(6455)Спорт-(42831)Строительство-(4793)Торговля-(5050)Транспорт-(2929)Туризм-(1568)Физика-(3942)Философия-(17015)Финансы-(26596)Химия-(22929)Экология-(12095)Экономика-(9961)Электроника-(8441)Электротехника-(4623)Энергетика-(12629)Юриспруденция-(1492)Ядерная техника-(1748)
Нафтоли 1 страница
|
|
|
|
План
ФЕНОЛИ
План
План
План
План
План
План
План
1. Загальна характеристика гомологічного ряду алканів.
2. Будова, ізомерія, номенклатура.
3. Поширення у природі та способи добування.
4. Фізичні та хімічні властивості алканів.
5. Окремі представники, похідні, їх значення і використання.
Ключові слова: карбоновий ланцюг, радикальний механізм реакцій, іонний механізм, номенклатура, ізомерія, структурні формули, алкани, гомологічний ряд, радикали, синтез Вюрца, інертність, реакція заміщення, крекінг, піроліз.
Література: [1] с. 21 - 33; [3] с. 133 – 145
1. Загальна характеристика гомологічного ряду алканів
Алкани - насичені вуглеводні, в молекулах яких атоми Карбону сполучені між собою s — зв’язками.
Алкани утворюють гомологічний ряд сполук, який відповідає загальній формулі 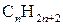 . Першим членом цього ряду є метан
. Першим членом цього ряду є метан 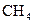 . Кожен наступний член ряду відрізняється від попереднього на групу
. Кожен наступний член ряду відрізняється від попереднього на групу 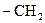 , яка називається гомологічною різницею.
, яка називається гомологічною різницею.
2. Будова, ізомерія та номенклатура алканів
Будова (стан 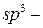 гібридизації, тип зв’язків, їх напрямленність). Структурні формули. Ізомерія алканів: структурна ізомерія, а саме ізомерія карбонового ланцюга, що обумовлена різноманітним порядком зв’язку атомів в молекулі.
гібридизації, тип зв’язків, їх напрямленність). Структурні формули. Ізомерія алканів: структурна ізомерія, а саме ізомерія карбонового ланцюга, що обумовлена різноманітним порядком зв’язку атомів в молекулі.
Номенклатура. Уявлення про радикали — структура та назва радикалів для перших чотирьох членів гомологічного ряду.
3. Поширення у природі та способи добування алканів
Алкани широко розповсюджені в природі. Здебільшого вони знаходяться у певних видах нафти, у природних та супутніх газах. Тверді насичені вуглеводні є головною складовою частиною бітумів, асфальтів, озокериту (гірський віск).
Основними способами промислового добування алканів із природних джерел є виділення їх у вигляді сумішей (фракцій) або індивідуальних сполук за допомогою, як правило, розгонки або ректифікації.
Найважливішим синтетичним методом одержання алканів є синтез Вюрца (1855р.) — взаємодія галогеналкілів з металічним натрієм:
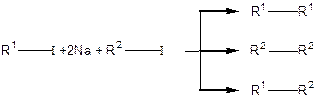
|
Алкани також можна добути із солей карбонових кислот, гідруванням ненасичених вуглеводнів, відновленням галогенопохідних.
4. Фізичні та хімічні властивості алканів
Закономірності зміни фізичних властивостей в гомологічному ряду і залежно від структури ізомерів.
Інертність у хімічному відношенні — за звичайних температур не окиснюються, не взаємодіють із концентрованою сульфатною кислотою та деякими іншими реагентами. Якісна реакція — алкани не знебарвлюють бромну воду та розчин калій перманганату. За певними умовами алкани вступають у реакції заміщення, окиснюються, за високих температур без доступу повітря відбувається крекінг і піроліз.
Реакції заміщення
Відбуваються за радикальним механізмом 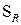 .
.
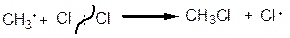
1. Галогенування
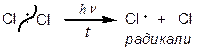
|
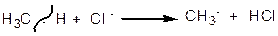
|
|
За таким же механізмом відбуваються реакції нітрування, сульфування та сульфохлорування.
2. Нітрування — реакція Коновалова, 1889 р.:
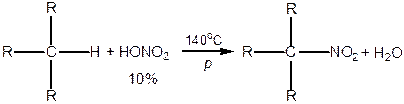
|
3. Сульфування — при взаємодії з димлячою сульфатною кислотою:

|
4. Сульфохлорування — дія на алкани сумішшю сірчистого газу та хлору:
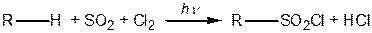
|
Сульфохлориди можна розглядати як хлорангідриди сульфокислоти, тому вони легко гідролізуються до сульфокислот 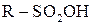 (
(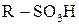 ).
).

|
Натрієві солі цих кислот називаються сульфонатами. Практичне значення мають сульфонати з числом атомів Карбону 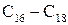 вони входять до складу синтетичних миючих засобів.
вони входять до складу синтетичних миючих засобів.
Окиснення алканів
За звичайних умов алкани стійкі до дії окисників, а в умовах нагрівання окиснюються з розривом карбонового ланцюга і утворенням різноманітних кисневмісних продуктів. Розроблено метод окиснення вищих насичених вуглеводнів під дією кисню повітря з метою добування вищих жирних кислот для миловаріння. Реакція відбувається з розривом карбонового ланцюга (реакція Намьоткіна):
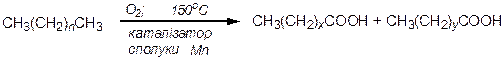
|
Повне окиснення — горіння. Підпалені на повітрі, вуглеводні горять, перетворюючись на 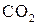 і
і 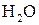 із виділенням великої кількості тепла. Реакція широко застосовується в енергетичних, а не в хімічних цілях. Таке згоряння палива відбувається у двигунах всіх типів.
із виділенням великої кількості тепла. Реакція широко застосовується в енергетичних, а не в хімічних цілях. Таке згоряння палива відбувається у двигунах всіх типів.
Крекінг, піроліз
Нагрівання вуглеводнів до високих температур (300°С ‑700°С, 1000°С) без доступу повітря призводить до їх розкладу, що супроводжується розривом карбонових ланцюгів і утворенням значно простіших насичених та ненасичених вуглеводнів. У цьому випадку відбувається гомолітичний розрив зв’язків С-Н і С-С. Може відбуватись також дегідрування, ізомеризація, циклізація та ароматизація вуглеводнів.
Крекінг має велике практичне значення. Реакція крекінгу важких фракцій нафти широко використовується для одержання алканів збагачених більш легкими фракціями - бензинів та газоподібних продуктів.
5. Окремі представники, їх значення та використання
Метан, етан, бутан. Використання насичених вуглеводнів в органічному синтезі.
Широке використання знаходять суміші насичених вуглеводнів. Вазелінове масло (у молекулах вуглеводнів міститься до 15 атомів Карбону) — прозора рідина без запаху і смаку, яку використовують у медицині, парфюмерії, косметиці. Вазелін (суміш рідких і твердих насичених вуглеводнів із кількістю Карбону до 25) застосовують як основу для виготовлення лікувальних мазей.
Парафін (суміш твердих вуглеводнів 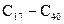 ) — біла тверда маса без запаху і смаку (
) — біла тверда маса без запаху і смаку (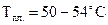 ). Його застосовують для теплових процедур при лікуванні нефритів, артритів та інших хвороб. Із парафіну виготовляють свічки, ним просочують папір, який використовують для пакування продуктів тощо.
). Його застосовують для теплових процедур при лікуванні нефритів, артритів та інших хвороб. Із парафіну виготовляють свічки, ним просочують папір, який використовують для пакування продуктів тощо.
Озокерит, або гірський віск — суміш твердих вуглеводнів. Використовується для лікувальних теплових процедур.
АЛКЕНИ. АЛКАДІЄНИ
Лекція № 3 (2 години)
1. Загальна характеристика гомологічного ряду алкенів.
2. Будова, ізомерія, номенклатура.
3. Поширення у природі та способи добування алкенів.
4. Фізичні та хімічні властивості алкенів.
5. Окремі представники, похідні, їх значення і використання.
6. Загальна характеристика та будова алкадієнів.
7. Хімічні властивості алкадієнів, їх значення та використання.
Ключові слова: ненасичені вуглеводні, алкени, подвійний зв'язок, просторова ізомерія, реакція відщеплення, реакція приєднання, електрофільне приєднання, правилоВ.В. Марковникова, реакція Вагнера, озонування, полімеризація.
Література: [1] с. 34 - 53; [3] с.145 – 167
1. Загальна характеристика гомологічного ряду алкенів
Алкени - ненасичені вуглеводні, в молекулах яких атоми Карбону сполучені подвійним зв’язком. Алкени утворюють гомологічний ряд, сполуки якого мають загальну формулу СnН2n. Найпростішим представником акенів є етен С2Н4.
2. Будова, ізомерія, номенклатура алкенів
Будова (стан  гібридизації). Подвійний ковалентний зв’язок - сполучення σ- та π - зв’язків. Ізомерія алкенів обумовлена будовою карбонового ланцюга та положенням подвійного зв’язку. Просторова — цис-транс -ізомерія. Номенклатура. Ненасичені радикали.
гібридизації). Подвійний ковалентний зв’язок - сполучення σ- та π - зв’язків. Ізомерія алкенів обумовлена будовою карбонового ланцюга та положенням подвійного зв’язку. Просторова — цис-транс -ізомерія. Номенклатура. Ненасичені радикали.
3. Поширення у природі та способи добування алкенів
Основний промисловий спосіб добування – крекінг та піроліз алканів.
Методи синтезу, як правило, основані на реакції відщеплення (елімінування) атомів або груп від сусідніх атомів Карбону:
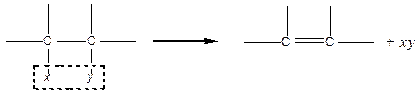
|
Способи одержання алкенів: дегідратація спиртів; дегідрогалогенування галогенопохідних алканів; дегалогенування віцинальних дигалогенопохідних алканів та ін. Правило Зайцева.
4. Фізичні та хімічні властивості алкенів
Закономірності зміни фізичних властивостей в гомологічному ряду і залежно від структури ізомерів.
Хімічні властивості алкенів обумовлені наявністю в їх молекулах подвійного зв’язку.
Реакції приєднання
Оскільки подвійний зв'язок виявляє електронодонорні властивості, алкени переважно вступають у реакції електрофільного приєднання за двостадійним механізмом.
Механізм реакції електрофільного приєднання  :
:
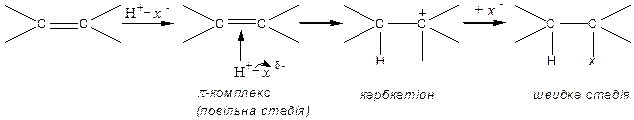
|
За таким механізмом приєднується: водень, галогени, галогеноводні, вода, кислоти тощо. Знебарвлення бромної води – якісна реакція на кратний зв’язок.
Правило В.В. Марковникова. Взаємний вплив атомів у молекулах. Індукційний ефект.
Реакції окиснення
Алкени легко окиснюються за звичайних умов під дією кисню повітря та окисників. Наприклад, алкени знебарвлюють водний розчин  (реакція Вагнера) — це якісна реакція на алкени:
(реакція Вагнера) — це якісна реакція на алкени:
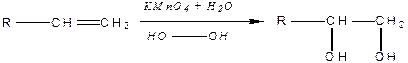
|
Сильні окисники окиснюють алкени до кислот та кетонів, що супроводжується розривом карбонового ланцюга за місцем подвійного зв'язку. Реакція їх горіння перебігає з утворенням кінцевих продуктів — води та вуглекислого газу (карбон (IV) оксиду).
Реакція озонування
Як специфічний окисник використовують озон. За продуктами гідролізу озонідів встановлюється місце розташування подвійного зв’язку у вихідному алкені.
Полімеризація алкенів
Важлива реакція, яка перебігає з утворенням цінних полімерних матеріалів. Відбувається за рахунок розриву подвійних зв’язків:

| |
| Мономер | Полімер (п — від 10 до кількох тисяч) |
Лінійна та ступінчаста полімеризація. Радикальна та іонна полімеризація.
5. Окремі представники, їх значення та використання
Етилен, пропілен, бутилен, їх промислові джерела та шляхи їх хімічної переробки. Поліетилен, поліпропілен, їх значення.
6. Загальна характеристика та будова алкадієнів
Вуглеводні, що містять у карбоновому ланцюгу два подвійних зв’язки, називають дієновими. Загальна формула сполук гомологічного ряду дієнових вуглеводнів - 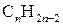 .
.
Дієни з кумульованими, супряженими та ізольованими подвійними зв’язками. Ізомерія алкадієнів обумовлена будовою карбонового ланцюгу та положенням подвійних зв’язків. Номенклатура.
7. Хімічні властивості алкадієнів, їх значення та використання
Хімічні властивості алкадієнів обумовлені наявністю подвійних зв'язків.
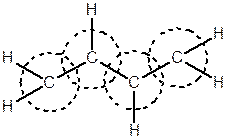
Дієни з кумульованими та ізольованими подвійними зв’язками мають властивості близькі до властивостей олефінів. Важливою особливістю сполук із спряженими зв’язками є їх значно вища реакційна здатність, порівняно зі сполуками, що мають ізольовані зв’язки. Крім того, вони здатні вступати в реакції приєднання таким чином, що приєднання відбувається до першого та четвертого атомів Карбону, а між другим та третім атомами Карбону утворюється подвійний зв'язок.
|
Така взаємодія двох сусідніх p -зв’язків називається спряженням (pp -спряженням), а його прояв – ефектом спряження. У молекулі утворюється єдина, спільна для усієї молекули p -електронна хмара з найбільшою електронною густиною між 1-2 та 3-4 атомами.
→ СН2(СІ) - СН=СН - СН2(СІ) - 1,4 дихлорбутен-2
СН2 = СН - СН = СН2 + СІ2 —
→ СН2(СІ) - СН(СІ) - СН =СН2 - 1,2 дихлорбутен-3
Окремі представники. Дивініл (1,4-бутадієн), ізопрен (2-метил-1,3-бутадієн).
Поняття про високомолекулярні сполуки, натуральні та синтетичні каучуки.
Продукти полімеризації спряжених дієнів називають синтетичними каучуками. Натуральний каучук - природний ненасичений стереорегулярний полімер ізопрену в цис -формі з молекулярною масою від 15000 до 500000, який добувається з соку тропічних дерев. Вперше синтетичний каучук у промисловому масштабі добуто в Росії за способом С.В. Лебедєва, який запропонував одержання бутадієнового каучуку за допомогою р-ції полімеризації бутадієну за наявності каталізатора - металевого натрію.
АЛКІНИ
Лекція № 4 (2 години)
1. Загальна характеристика гомологічного ряду алкінів.
2. Будова, ізомерія, номенклатура алкінів.
3. Способи добування алкінів.
4. Фізичні властивості.
5. Хімічні властивості.
6. Окремі представники, похідні, їх значення і використання.
Ключові слова: алкіни, потрійний зв'язок, етин, алкініли, реакція Кучерова, реакція А.Е. Фаворського, поляризація зв’язку, ацетиленіди, димеризація, купрен, полімеризація, вінілацетилен, синтетичний каучук, штучна шкіра.
Література: [1] с. 54 - 62; [3] с. 167 – 175
1.Загальна характеристика гомологічного ряду алкінів
Алкіни – ненасичені вуглеводні, в молекулах яких атоми Карбону сполучені потрійним зв’язком. Загальна формула сполук 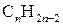 .
.
2. Будова, ізомерія та номенклатура алкінів
Будова (стан sp- гібридизації). Потрійний ковалентний зв’язок – сполучення σ- та двох π - зв’язків. Ізомерія алкінів обумовлена будовою карбонового ланцюгу та положенням потрійного зв’язку. Номенклатура. Ненасичені радикали – алкініли.
3. Способи добування алкінів
Одержання етину з карбіду кальцію:
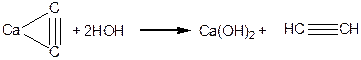
|
Способи одержання алкінів: дегідрогалогенування дигалогенопохідних алканів; алкілування ацетиленідів.
4. Фізичні властивості алкінів
Закономірності зміни фізичних властивостей в гомологічному ряду і залежно від структури ізомерів.
5. Хімічні властивості алкінів
Хімічні властивості алкінів обумовлені наявністю в їх молекулах потрійного зв’язку.
Реакції приєднання
Реакції електрофільного приєднання 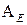 : водню, галогенів, галогеноводнів, води (реакція Кучерова), спиртів (реакція А.Е. Фаворського). Для алкінів реакції приєднання перебігають у дві стадії.
: водню, галогенів, галогеноводнів, води (реакція Кучерова), спиртів (реакція А.Е. Фаворського). Для алкінів реакції приєднання перебігають у дві стадії.
Реакція знебарвлення бромної води – якісна реакція на потрійний зв’язок.
Реакції окиснення
В результаті окиснення етину під дією водного розчину калій перманганату 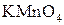 утворюється калієва сіль етандіової кислоти:
утворюється калієва сіль етандіової кислоти:
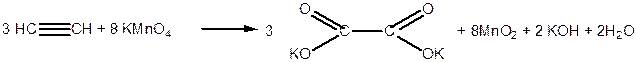
|
Наведену реакцію використовують як якісну реакцію на потрійний зв’язок.
Під дією сильних окисників в молекулі алкінів відбувається розрив карбонового ланцюга за місцем потрійного зв’язку, в результаті чого утворюються карбонові кислоти.
На повітрі ацетилен горить кіптявим полум’ям, під дією кисню – сліпучим полум’ям із виділенням великої кількості тепла.
Специфічні реакції
Для алкінів характерні реакції заміщення, що обумовлено значною поляризацією ≡С-Н зв’язку.
Утворення металевих похідних — ацетиленідів:
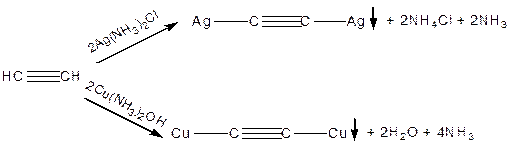
|
Це якісні р-ції на атом Гідрогену, що знаходиться біля Карбону з потрійним зв’язком. Їх використовують для виділення алкінів з суміші. Після осадження і виділення ацетиленідів під дією мінеральних кислот знову утворюються алкіни.
Реакції полімеризації
Полімеризація ацетилену: утворення вінілацетилену, бензолу, циклооктатетраєну, купрену.
6. Окремі представники, їх значення та використання
Промислове застосування ацетилену: добування оцтового альдегіду, синтетичного каучуку, штучної шкіри тощо. Використання ацетилену для різання і зварювання металів.
АЛІЦИКЛІЧНІ ВУГЛЕВОДНІ. ТЕРПЕНИ
(На самостійне опрацювання)
План лекції:
1. Загальна характеристика гомологічного ряду циклоалканів.
2. Будова, ізомерія, номенклатура циклоалканів.
3. Поширення у природі, способи добування циклоалканів.
4. Фізичні та хімічні властивості циклоалканів.
5. Теорія напруження А.Байєра.
6. Окремі представники, їх значення та використання.
Ключові слова: циклоалкани, стійкість циклів, теорія напруження А.Байєра, конформаційна ізомерія, кутове напруження, форма «ванни», форма «крісла», терпени, ефірна олія, моноциклічних терпени, біциклічні терпени.
Література: [2] с. 176 - 185; [1] с. 63 – 74
1. Загальна характеристика гомологічного ряду циклоалканів
Циклоалкани – вуглеводні циклічної будови, молекули яких містять замкнені цикли (кільця) з атомів Карбону, сполучених між собою ординарними зв’язками. Загальна формула циклопарафінів 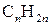 . За властивостями вони близькі до аліфатичних вуглеводнів, тому в назві мають аналогічний префікс
. За властивостями вони близькі до аліфатичних вуглеводнів, тому в назві мають аналогічний префікс 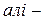 .
.
Аліциклічні сполуки можуть бути насиченими (циклоалкани) чи ненасиченими (циклоалкени і циклоалкадієни) залежно від відсутності або наявності подвійного зв’язку.
2. Будова, ізомерія та номенклатура циклоалканів
Будова (стан 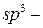 гібридизації, тип зв’язків, їх напрямленність). Структурна ізомерія обумовлена розміром циклу; ізомерією радикалів в циклі; ізомерією за положенням радикалів в циклі. Просторова ізомерія обумовлена різним просторовим розміщенням замісників відносно площини кільця.
гібридизації, тип зв’язків, їх напрямленність). Структурна ізомерія обумовлена розміром циклу; ізомерією радикалів в циклі; ізомерією за положенням радикалів в циклі. Просторова ізомерія обумовлена різним просторовим розміщенням замісників відносно площини кільця.
За міжнародною номенклатурою назви циклопарафінів утворюють від назв відповідних (за числом атомів Карбону) насичених вуглеводнів, додаючи префікс — 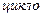 -: циклопропан, циклобутан і т.д. Нумерацію проводять таким чином, щоб замісники отримували найменші номери. Із метою спрощення написання формул циклічні сполуки умовно зображують у вигляді геометричних фігур, в яких число кутів відповідає числу атомів Карбону в циклі (трикутник, п’ятикутник тощо).
-: циклопропан, циклобутан і т.д. Нумерацію проводять таким чином, щоб замісники отримували найменші номери. Із метою спрощення написання формул циклічні сполуки умовно зображують у вигляді геометричних фігур, в яких число кутів відповідає числу атомів Карбону в циклі (трикутник, п’ятикутник тощо).
3. Поширення у природі, способи добування циклоалканів
Циклоалкани розповсюджені в природі - вони є головною складовою частиною деяких видів нафти, а також зустрічаються в ефірних оліях.
Способи добування: одержання із дигалогенопохідних алканів, гідрування ароматичних вуглеводнів, піроліз солей двохосновних кислот.
4.Фізичні та хімічні властивості циклоалканів
Для циклоалканів спостерігаються тіж самі закономірності в зміні фізичних властивостей як і для інших вуглеводнів.
Найпростіші циклоалкани — гази (циклопропан, циклобутан), а вищі — рідини або тверді речовини. Температура кипіння і густина у циклоалканів декілька вищі, ніж у їх аліфатичних аналогів із відповідним числом атомів Карбону. Циклоалкани малополярні і практично нерозчинні у воді.
Хімічні властивості циклоалканів значною мірою залежать від стійкості їх циклів. Так, циклопропану і циклобутану характерна підвищена реакційна здатність, вони легко вступають в реакції приєднання з розривом циклу і за властивостями нагадують алкени. Але вони не знебарвлюють бромну воду й розчин калій перманганату.
Вуглеводні з циклами з п’яти й більше атомами Карбону більш стійкі, для них подібно насиченим алканам характерні реакції заміщення.
1. Реакції приєднання
До реакцій приєднання у першу чергу схильні циклопропан і циклобутан.
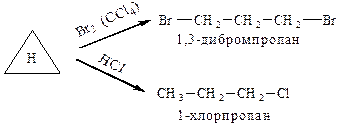
| |
| циклопропан |
2. Реакції заміщення
Реакції заміщення більше характерні для п’яти-, шестичленних і вищих циклів, які подібно алканам вступають до реакції заміщення в основному за радикальним механізмом.
3. Гідрування циклоалканів
На прикладі реакції гідрування нижчих моноциклоалканів за однакових умов, крім температури, наочно спостерігається відносна стійкість циклів та їх здатність до реакцій приєднання:
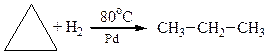
|
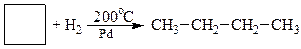
|
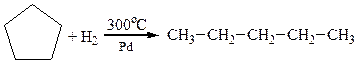
|
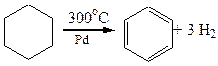
|
4. Реакції окиснення
Циклоалкани досить стійкі до дії окисників, а умови перебігу, напрямок і результат окиснення визначаються їх будовою. Із наведених реакцій видно, що хімічна поведінка циклоалканів тісно пов’язана з розмірами циклів.
5. Теорія напруження А.Байєра (1885 р.)
Передумовою сучасного трактування будови циклічних сполук була теорія напруження А.Байєра, який виходив із їх плоскої будови і пояснював стійкість циклів відхиленням їх валентних кутів від тетраедричного кута 109°28¢ у метані.
Із посилки — всі атоми в циклі розміщені в одній площині слідувало, що валентні кути в 3-членному циклі дорівнюють 60°, в 4-членному — 90°, в 5-членному — 108°, в 6-членному — 120° і т.д.
Чим більше відхилення валентного кута у циклі від кута в тетраедрі, тим більше напруження і менша стійкість циклу. Мірою напруження Байєр запропонував вважати половину різниці між кутом в тетраедрі і валентним кутом того чи іншого циклу (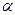 ):
):
| Циклопропан | 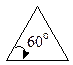
| 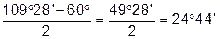
|
| Циклобутан | 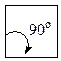
| 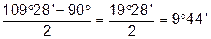
|
| Циклопентан | 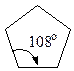
| 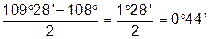
|
| Циклогексан | 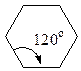
| 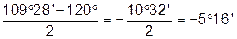
|
| Циклогептан | 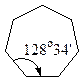
| 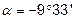
|
Як видно з наведених розрахунків найменше відхилення валентних зв’язків спостерігається у циклопентану, тому його кільце має незначну напругу. Воно міцніше, ніж кільця 3- та 4-членних циклів. Таким чином, теорія напруження пояснювала причину нестійкості 3- та 4-членних циклів, але не допускала можливості існування стійких вищих циклів, в яких напруження повинно бути великим. Ружечка добув стійкий циклогептадекан  , який витримував нагрівання до 400°С. Пояснення цей факт отримав після відкриття конформаційної — поворотної ізомерії органічних сполук.
, який витримував нагрівання до 400°С. Пояснення цей факт отримав після відкриття конформаційної — поворотної ізомерії органічних сполук.
Конформаційна (поворотна) ізомерія є результатом не досить вільного (обмежено вільного) обертання груп атомів молекули навколо 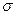 -зв’язків і зумовлює існування конформаційних ізомерів. Конформаційні ізомери – стереоізомери, які мають неоднакове просторове розміщення атомів або атомних груп, зумовлене обертанням навколо ординарного карбон-карбонового зв’язку. Ці ізомери називають ще конформірами або конформаціями. Конформація – різне просторове розташування атомів або груп атомів в молекулах певної конфігурації, зумовлене обертанням навколо
-зв’язків і зумовлює існування конформаційних ізомерів. Конформаційні ізомери – стереоізомери, які мають неоднакове просторове розміщення атомів або атомних груп, зумовлене обертанням навколо ординарного карбон-карбонового зв’язку. Ці ізомери називають ще конформірами або конформаціями. Конформація – різне просторове розташування атомів або груп атомів в молекулах певної конфігурації, зумовлене обертанням навколо 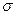 -зв’язків. Конформації мають різний запас вільної енергії, і звідси, є неоднакова вірогідність існування молекули у вигляді тої чи іншої конформації.
-зв’язків. Конформації мають різний запас вільної енергії, і звідси, є неоднакова вірогідність існування молекули у вигляді тої чи іншої конформації.
Г.Закс (1890 р.) і Е.Мор (1918 р.) припустили існування в циклах певних просторових неплоских побудов, що нині підтверджено різними фізичними методами. На поведінку складних циклів значний вплив має будова поворотних ізомерів.
Розглянемо поворотну ізомерію циклів на прикладі циклогексану. Атоми Карбону в циклогексані можуть розміщуватися в різних площинах у просторі і не змінюють валентних кутів атома Карбону. Для циклогексану можливе існування двох просторових форм (конформацій) без кутового напруження — форми “C” — [це] або “ванни” (човна) і форми “Z” — [зет] або “крісла”. Більш енергетично вигідною є форма “Z” — “крісла”, вона на 28,9 кДж/моль (5 ккал/моль) менша.
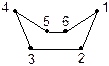
| 
|
| Форма “C” — “ванни” | Форма “Z” — “крісла” |
У конформації “ванна” чотири атоми Карбону (2,3,5,6) лежать в одній площині, а два (1,4) — піднімаються над нею. А в конформації “крісло” атоми 1 або 4 опущені вниз, за площину, де знаходяться чотири (2,3,5,6) атоми Карбону.
6. Окремі представники, їх значення та використання
Уявлення про циклоалкени, циклоалкадієни.
Терпени складають значну частину рослинних речовин, що входять до складу ефірних олій. Ефірні олії — рідини, що мають специфічний запах, нерозчинні у воді, але леткі з водяною парою. До ефірних олій відносяться: м’ятна, лимонна, гвоздична, трояндова та інші олії; скипидар — соснова ефірна олія. Їм притаманний специфічний запах, вони широко використовуються в парфумерній і харчовій промисловості.
В основі будови моноциклічних терпенів лежить вуглеводень С10 Н20 - ментан (1-метил-4-ізопропілциклогексан). В лимонній олії та скипидарі міститься один з простіших моноциклічних терпенів лимонен. Ментол належить до числа важливих кисневих моноциклічних терпенів. Має слабкі антисептичні властивості. Використовується в медицині.
|
|
|
|
|
Дата добавления: 2014-12-08; Просмотров: 1740; Нарушение авторских прав?; Мы поможем в написании вашей работы!