
КАТЕГОРИИ:
Архитектура-(3434)Астрономия-(809)Биология-(7483)Биотехнологии-(1457)Военное дело-(14632)Высокие технологии-(1363)География-(913)Геология-(1438)Государство-(451)Демография-(1065)Дом-(47672)Журналистика и СМИ-(912)Изобретательство-(14524)Иностранные языки-(4268)Информатика-(17799)Искусство-(1338)История-(13644)Компьютеры-(11121)Косметика-(55)Кулинария-(373)Культура-(8427)Лингвистика-(374)Литература-(1642)Маркетинг-(23702)Математика-(16968)Машиностроение-(1700)Медицина-(12668)Менеджмент-(24684)Механика-(15423)Науковедение-(506)Образование-(11852)Охрана труда-(3308)Педагогика-(5571)Полиграфия-(1312)Политика-(7869)Право-(5454)Приборостроение-(1369)Программирование-(2801)Производство-(97182)Промышленность-(8706)Психология-(18388)Религия-(3217)Связь-(10668)Сельское хозяйство-(299)Социология-(6455)Спорт-(42831)Строительство-(4793)Торговля-(5050)Транспорт-(2929)Туризм-(1568)Физика-(3942)Философия-(17015)Финансы-(26596)Химия-(22929)Экология-(12095)Экономика-(9961)Электроника-(8441)Электротехника-(4623)Энергетика-(12629)Юриспруденция-(1492)Ядерная техника-(1748)
Рентгеноструктурный анализ
|
|
|
|
В настоящее время РСА перестал быть экзотическим методом установления структур органических соединений. А монокристаллы можно получать практически из всех классов соединений, пользуясь при необходимости возможностями соле- и комплексообразования для плохо кристаллизующихся объектов.
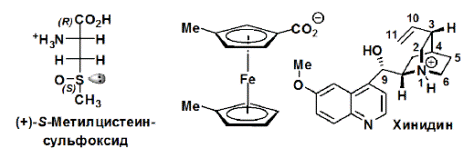
Как отмечалось выше, в отсутствии аномального рассеяния Бийво РСА не позволяет определить абсолютную конфигурацию, тем не менее, если для молекулы известна абсолютная конфигурация одного асимметрического центра, то по данным РСА легко определить и конфигурацию всех остальных. Например, при структурном исследовании природного продукта (+)-S-метилцистеинсульфоксида было установлено, что для серы реализуется (S)-конфигурация. Этот вывод сделан на том основании, что природный L-цистеин имеет (R)-конфигурацию, а относительная конфигурация второго хирального центра молекулы очевидна из РСА. Фактически, метод РСА-корреляции можно применять для определения абсолютной конфигурации любой хиральной молекулы с неизвестной конфигурацией, если её как-нибудь (ковалентно, ионно, комплексно) объединить с другим соединением, абсолютная конфигурация которого известна. Этот приём был использован впервые A. McL. Mathieson в 1956 г. (Acta Crystallogr. 1956, 9, 317). Так была установлена абсолютная конфигурация (R)-1,1’-диметилферроцен-3-карбоновой кислоты в составе её соли с хинидином, абсолютная конфигурация которого была уже известна.
2. Химическая корреляция: превращения, не затрагивающие связи со стереогенным центром
Этот метод основан на превращении соединения с неизвестной конфигурацией в соединение с известной конфигурацией или наоборот − образованием неизвестной конфигурации из известной без затрагивания хирального центра. Поскольку в ходе превращения хиральный центр не затрагивается, очевидно, что продукт должен иметь ту же абсолютную конфигурацию, что и исходное соединение.
|
|
|
При этом вовсе не обязательно, что если известное соединение относится к (R)-ряду, то и неизвестное, полученное из первого, будет иметь (R)-конфигурацию. Например, при восстановлении (R)-1-бром-2-бутанола в 2-бутанол, не затрагивающем хиральный центр, продуктом будет (S)-энантиомер несмотря на то, что его конфигурация не изменилась. Это связано с тем, что этильная группа по номенклатуре КИП младше группы BrCH2, но старше группы СН3.

Ниже приведен пример конфигурационной корреляции (+)-винной кислоты с (+)-(R)-глицериновым альдегидом на основе превращений, не затрагивающих асимметрический центр.
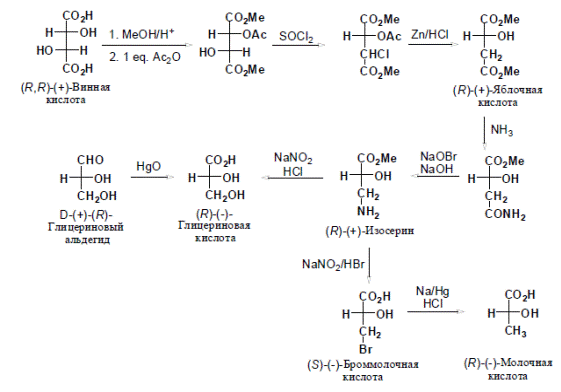
Эта схема синтезов имела основополагающее значение для стереохимии, т.к. позволила скоррелировать друг с другом важнейшие ряды природных оптически активных веществ: сахара, гидроксикислоты и аминокислоты.
Другим интересным примером является корреляция между алифатическими и ароматическими аминосоединениями, которая была применена для определения конфигурации фенилэтиламина и родственных соединений.
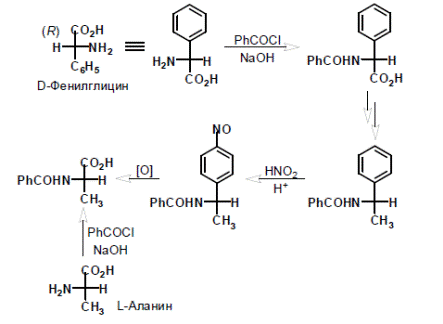
Возможны случаи, когда часть химических превращений проводят с веществом, конфигурация которого известна, часть – с исследуемым веществом с неизвестной конфигурацией, причем из обоих веществ образуется общий промежуточный продукт.
Так, например, (S)-яблочная кислота (конфигурация известная) и (−)-β-метоксиадипиновая кислота (конфигурация неизвестна) в результате превращений дают один и тот же промежуточный продукт. Отсюда следует, что (−)-β-метоксиадипиновой кислоте отвечает проекционная формула А, а ее (+)-изомеру формула Б.

|
|
|
|
|
Дата добавления: 2014-12-08; Просмотров: 550; Нарушение авторских прав?; Мы поможем в написании вашей работы!