
КАТЕГОРИИ:
Архитектура-(3434)Астрономия-(809)Биология-(7483)Биотехнологии-(1457)Военное дело-(14632)Высокие технологии-(1363)География-(913)Геология-(1438)Государство-(451)Демография-(1065)Дом-(47672)Журналистика и СМИ-(912)Изобретательство-(14524)Иностранные языки-(4268)Информатика-(17799)Искусство-(1338)История-(13644)Компьютеры-(11121)Косметика-(55)Кулинария-(373)Культура-(8427)Лингвистика-(374)Литература-(1642)Маркетинг-(23702)Математика-(16968)Машиностроение-(1700)Медицина-(12668)Менеджмент-(24684)Механика-(15423)Науковедение-(506)Образование-(11852)Охрана труда-(3308)Педагогика-(5571)Полиграфия-(1312)Политика-(7869)Право-(5454)Приборостроение-(1369)Программирование-(2801)Производство-(97182)Промышленность-(8706)Психология-(18388)Религия-(3217)Связь-(10668)Сельское хозяйство-(299)Социология-(6455)Спорт-(42831)Строительство-(4793)Торговля-(5050)Транспорт-(2929)Туризм-(1568)Физика-(3942)Философия-(17015)Финансы-(26596)Химия-(22929)Экология-(12095)Экономика-(9961)Электроника-(8441)Электротехника-(4623)Энергетика-(12629)Юриспруденция-(1492)Ядерная техника-(1748)
План заняття. 1. Вивчити окислення формальдегіду дегідрогеназою молока
|
|
|
|
1. Вивчити окислення формальдегіду дегідрогеназою молока.
2. Виявити вплив підвищеної температури на активність перок-сидази хріну.
3. Дослідити властивості рибофлавіну утворювати зворотню окислювально-відновлювальну систему.
4. Визначити роль поліфенолоксидази овочів у зміні їх забарв-лення.
Клас оксидоредуктаз включає ферменти, що беруть участь в окисленні та відновлюванні різних речовин. Окислення може здійснюватися декількома шляхами:
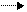 1. АО + ½ О2 АО2 (приєднання кисню);
1. АО + ½ О2 АО2 (приєднання кисню);
 2. АН2 + В А + ВН2 (відняття водню);
2. АН2 + В А + ВН2 (відняття водню);
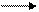 3. А2+ А3+ + е0 (відняття електрона).
3. А2+ А3+ + е0 (відняття електрона).
 Ферментам цього класу належить важлива роль у диханні та бродінні. До оксидоредуктаз належать, зокрема, дегідрогенази, оксидази і пероксидази.
Ферментам цього класу належить важлива роль у диханні та бродінні. До оксидоредуктаз належать, зокрема, дегідрогенази, оксидази і пероксидази.
Дегідрогенази. Дегідрогенази каталізують окислення субстрату шляхом відняття від нього водню, тобто перенесення водню від донора (здатного до окислення субстрату) на відповідний акцептор. Акцептором може бути кисень або будь-яка речовина, що міститься у тканинах організму. У дослідах використовують штучний акцептор – метиленову синь (МС). Дегідрогеназа відбирає водень від субстрату і віддає його МС, яка відновлюється і перетворюється в безбарвну сполуку (МСН2). Отже, обезбарвлення розчину може свідчити про дію дегідрогенази. Лейкоформа (МСН2) легко окислюється киснем повітря, тому досліди проводять при відсутності повітря (у пробірках Тунберга або звичайних пробірках під шаром рослинної олії).
Оксидази. Окислення різних субстратів за рахунок кисню повітря каталізують оксидази. До цієї групи ферментів належать поліфенолоксидаза і тирозиназа. Саме дією поліфенолоксидази пояснюється потемніння поверхні розрізаного яблука або картоплини. Цей фермент окислює полі- і монофеноли, дубильні речовини та інші органічні сполуки з утворенням темнозабарвлених продуктів. Тирозиназа бере участь в окисленні амінокислоти тирозину до темного пігменту меланіна («мелас» – від грецьк. чорний).
|
|
|
Пероксидаза. У лабораторіях широко використовують метод визначення активності пероксидази, в основу якого покладено окислення пірогалолу в присутності перекису водню до пурпурогаліну, що утворює в розчині червоно-бурий осад.
1. Окислення формальдегіду дегідрогеназою молока
У молоці містяться дегідрогенази, що потрапляють із молочної залози та з мікрофлори молока. Альдегіддегідрогеназа окислює формальдегід до мурашиної кислоти.
Об’єкт дослідження: Молоко (джерело ферменту).
Обладнання і посуд: 1. Штатив із пробірками;
2. Водяна баня на 40оС;
3. Годинник або секундомір.
Реактиви: 1.Формальдегід, 0,4 %-й розчин;
2. Метиленова синь (МС), 0,001 %-й розчин;
3. Трихлороцтова кислота, 20 %-й розчин.
Техніка виконання роботи
В одну пробірку вливають 5 мл кип’яченого молока, у другу – 5 мл свіжого. В обидві пробірки додають 0,5 мл розчину формальдегіду та 3 краплі розчину МС. Вміст струшують і пробірки розташовують у водяній бані (400С). Фіксують час, необхідний для знебарвлення МС. Активність дегідрогенази виражають у хвилинах, необхідних для знебарвлення МС. Одержані результати записують і роблять висновок.
Одержані результати записують і пояснюють.
У всіх дослідах з дегідрогеназами використовували ТХО або високу температуру для інактивації ферменту. Ці фактори незворотне денатурують ферментний білок, тому при послідуючій інкубації в оптимальних умовах активність ферментів не виявлялася (контрольний варіант дослідів).
2. Вплив температури на активність пероксидази хрону
Об’єкт дослідження: Екстракт хрону.
Обладнання і посуд: 1. Штатив із пробірками;
|
|
|
2. Палички скляні;
3. Піпетки;
4. Термостат.
Реактиви: 1. Пірогалол, 1 %-й розчин;
2. Перекис водню, 2 %-й розчин.
Техніка виконання роботи
Щоб визначити вплив температури на активність пероксидази, проводять досліди при 0...4оС (холодильник) та 37оС (термостат).
В пробірку вносять 1 мл розчину перекису водню й 1,5 мл розчину пірогалолу. Вміст пробірки доводять до заданої температури (нагріваючи або охолоджуючи), а потім додають 1,5 мл екстракту хрону, заздалегідь термостатованого при тій самій температурі в окремій пробірці. Вміст пробірки постійно перемішують скляною паличкою. Заміряють час до появи червоно-бурого осаду. Активність пероксидази виражають у секундах, необхідних для появи забарвлення.
3. Дослідження властивості рибофлавіну утворювати зворотню окислювально-відновлювальну систему
Об’єкт дослідження: Рибофлавін.
Обладнання і посуд: 1. Штатив із пробірками;
2. Гумові або коркові пробки.
Реактиви: 1. Рибофлавін, 0,015 %-й розчин;
2. НСl, концентрована;
3. Цинк, шматочки.
Техніка виконання роботи
У пробірку наливають 1 мл розчину рибофлавіну, потім додають 5 крапель НСl та шматочок цинку. Закорковують і залишають на 10...20 хв. спостерігають зникнення жовтого кольору рибофлавіну. Спочатку під впливом виділяющогося водню колір розчину поступово змінюється: спочатку з жовтого на зелений, а потім на рожевий і поступово обезбарвлюється (рибофлавін відновлений). Через 10...20 хвилин спостерігають появу жовтого кольору розчину (рибофлавін окислений).
4. Визначення ролі поліфенолоксидази в зміні забарвлення овочів та впливу на них гіпосульфіту натрію
Під впливом цього ферменту з циклічних амінокислот, що входять до складу білків картоплі, утворюються темнозабарвлені сполуки, внаслідок чого він темніє.
Об’єкт дослідження: Сира картопля.
Обладнання і посуд: Парцелянові ступки з товкачиками.
Реактиви: Гіпосульфіт натрію, 0,1 н розчин.
Техніка виконання роботи
У дві ступки кладуть по шматочку картоплі (1...2 г) і розтирають до однородної маси. Потім в першу ступку додають 2...3 мл розчину гіпосульфіту Na та перемішують. Сполуки залишають на повітрі на 15...20 хв., потім фіксують зміну забарвлення у кожній ступці.
|
|
|
Контрольні запитання
1. Яка роль ферментів в організмі?
2. Розповідайте про будову ферментів й їхніх активних центрів.
3. Якими властивостями володіють ферменти?
4. Як впливають на активність ферментів фізичні й хімічні фактори?
5. Чим обумовлена специфічність дії ферментів? Види специфічності.
6. Які номенклатура й класифікація ферментів?
7. Охарактеризуйте різні класи ферментів.
8. Які процеси харчових виробництв засновані на дії ферментів?
9. Які ферменти застосовуються в консервній промисловості?
10. Які ферменти застосовуються в м‘ясопереробній промисловості?
11. Які ферменти застосовуються в крохмале-патоковій промисловості?
12. Яка роль біологічного окислювання для процесів життєдіяльності організму?
13. Які розходження біологічного окислювання й окислювання в неживій природі?
14. Назвіть групи ферментів, що приймають участь у біологічному окислюванні.
15. Як побудовані анаеробні і аеробні дегідрогенази?
16. Розповісти про ролі гемінових ферментів у біологічному окислюванні.
17. Як здійснюється транспорт електронів і протонів у біологічному окислюванні?
18. Які речовини є кінцевими продуктами біологічного окислювання?
19. Чим відрізняються окислені форми НАД і ФАД від відновлених?
20. При підвищенні функції щитовидної залози різко збільшується утворення тепла, підвищується температура тіла. Які біохімічні процеси обумовлюють це явище?
|
|
|
|
|
Дата добавления: 2014-12-08; Просмотров: 534; Нарушение авторских прав?; Мы поможем в написании вашей работы!