
КАТЕГОРИИ:
Архитектура-(3434)Астрономия-(809)Биология-(7483)Биотехнологии-(1457)Военное дело-(14632)Высокие технологии-(1363)География-(913)Геология-(1438)Государство-(451)Демография-(1065)Дом-(47672)Журналистика и СМИ-(912)Изобретательство-(14524)Иностранные языки-(4268)Информатика-(17799)Искусство-(1338)История-(13644)Компьютеры-(11121)Косметика-(55)Кулинария-(373)Культура-(8427)Лингвистика-(374)Литература-(1642)Маркетинг-(23702)Математика-(16968)Машиностроение-(1700)Медицина-(12668)Менеджмент-(24684)Механика-(15423)Науковедение-(506)Образование-(11852)Охрана труда-(3308)Педагогика-(5571)Полиграфия-(1312)Политика-(7869)Право-(5454)Приборостроение-(1369)Программирование-(2801)Производство-(97182)Промышленность-(8706)Психология-(18388)Религия-(3217)Связь-(10668)Сельское хозяйство-(299)Социология-(6455)Спорт-(42831)Строительство-(4793)Торговля-(5050)Транспорт-(2929)Туризм-(1568)Физика-(3942)Философия-(17015)Финансы-(26596)Химия-(22929)Экология-(12095)Экономика-(9961)Электроника-(8441)Электротехника-(4623)Энергетика-(12629)Юриспруденция-(1492)Ядерная техника-(1748)
Правило фаз Гиббса. В 1876 г. Гиббс вывел простую формулу, связывающую число фаз (Ф), находящихся в равновесии, число компонентов (К) и число степеней свободы (С) системы
|
|
|
|
В 1876 г. Гиббс вывел простую формулу, связывающую число фаз (Ф), находящихся в равновесии, число компонентов (К) и число степеней свободы (С) системы. При равновесии должны быть выполнены следующие условия:
давление (Р) и температура (Т) одинаковы во всех точках системы,
химический потенциал (m i) каждого i - ого компонента одинаков во всех фазах.
Рассмотрим равновесную систему из Ф фаз и К компонентов. Состав каждой фазы можно определить с помощью (К -1) концентраций, поскольку все концентрации связаны условием:  , где
, где 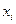 — мольная доля i - ого компонента. Общее число переменных, характеризующих систему, равно
— мольная доля i - ого компонента. Общее число переменных, характеризующих систему, равно 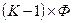 концентраций плюс 2 (температура и давление):
концентраций плюс 2 (температура и давление):
(K – 1) ´ Ф + 2 (IV, 19)
Если только одна из этих переменных (температура или давление) поддерживается постоянной, то число независимых переменных составит (K – 1) ´ Ф + 1. Если же на систему действует, например, внешнее магнитное поле, то общее число независимых переменных увеличится и составит (K – 1) ´ Ф + 3.
Часть переменных связана уравнениями, вытекающими из условий равновесия (смотри (IV, 13)):
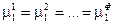
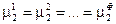
…………………
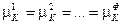
Общее число таких уравнений равно числу строк (оно соответствует числу компонентов К), умноженному на число равенств в строке (Ф – 1)
K ´ (Ф – 1) (IV, 20)
Если число независимых переменных равно числу уравнений, их связывающих, то каждая независимая переменная принимает некоторое строго определенное значение и вся система может существовать только при этом единственно возможном сочетании значений температуры, давления и концентраций компонентов во всех фазах.
Если же число уравнений меньше числа независимых переменных, то их разность, которую мы определили как число термодинамических степеней свободы (С) представляет собой число переменных, которым можно придавать произвольные значения при имеющемся числе уравнений, а следовательно, и при данном числе фаз, т. к. число уравнений определяется числом фаз.
Число термодинамических степеней свободы С равно общему числу переменных (IV, 19) минус число уравнений (IV, 20), связывающих эти переменные: 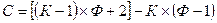 .
.
Раскрывая скобки и группируя слагаемые, получим правило фаз Гиббса:
С = К – Ф+ 2
Согласно этому правилу, чем больше компонентов в системе, тем больше степеней свободы.
Для любой системы число фаз максимально, когда С = 0.
Для однокомпонентной системы К = 1 и максимальное число фаз Ф = 3.
Для двухкомпонентной системы К = 2 и максимальное число фаз Ф = 4.
Правило фаз Гиббса устанавливает общую закономерность, которой подчиняются гетерогенные системы, состоящие из любого числа фаз и любого числа компонентов.
|
|
|
|
|
Дата добавления: 2014-11-29; Просмотров: 472; Нарушение авторских прав?; Мы поможем в написании вашей работы!