
КАТЕГОРИИ:
Архитектура-(3434)Астрономия-(809)Биология-(7483)Биотехнологии-(1457)Военное дело-(14632)Высокие технологии-(1363)География-(913)Геология-(1438)Государство-(451)Демография-(1065)Дом-(47672)Журналистика и СМИ-(912)Изобретательство-(14524)Иностранные языки-(4268)Информатика-(17799)Искусство-(1338)История-(13644)Компьютеры-(11121)Косметика-(55)Кулинария-(373)Культура-(8427)Лингвистика-(374)Литература-(1642)Маркетинг-(23702)Математика-(16968)Машиностроение-(1700)Медицина-(12668)Менеджмент-(24684)Механика-(15423)Науковедение-(506)Образование-(11852)Охрана труда-(3308)Педагогика-(5571)Полиграфия-(1312)Политика-(7869)Право-(5454)Приборостроение-(1369)Программирование-(2801)Производство-(97182)Промышленность-(8706)Психология-(18388)Религия-(3217)Связь-(10668)Сельское хозяйство-(299)Социология-(6455)Спорт-(42831)Строительство-(4793)Торговля-(5050)Транспорт-(2929)Туризм-(1568)Физика-(3942)Философия-(17015)Финансы-(26596)Химия-(22929)Экология-(12095)Экономика-(9961)Электроника-(8441)Электротехника-(4623)Энергетика-(12629)Юриспруденция-(1492)Ядерная техника-(1748)
Актиноиды 2 страница
|
|
|
|
i= V H2×96500/ V г-экв Н2 t.
Объем грамм-эквивалента водорода при н.у. равен половине грамм-молекулярного объема 22,4/2 = 11,2 л. Подставив в приведенную формулу значения V H2=1,4, V г-экв Н2 = 11,2, t = 6025 (1 ч 40 мин 26 с = 6025 с), находим
i = 1,4 ´ 96500/11,2 ´ 6025 = 2 А.
Пример 4. Сколько граммов едкого кали образовалось у катода при электролизе раствора K2SO4, если на аноде выделилось 11,2 л кислорода, измеренного при нормальных условиях?
Решение. Объем грамм-эквивалента кислорода (н. у.) 22,4/4 = 5,6 л. Следовательно, 11,2 л составляют 2 г-экв кислорода. Столько же, т, е. 2 г-экв КОН образовалось у катода, или 56,11 ´ 2 = 112,22 г (56,11 г - г×экв КОН).
241. Электролиз раствора K2SО4 проводили при силе тока 5 А в течение 3 ч. Составьте электронные уравнения процессов, происходящих на электродах, вычислите объем выделяющихся на электродах веществ.
242. Составьте электронные уравнения процессов, происходящих на электродах при электролизе растворов AlCl3, NiSO4. В обоих случаях анод угольный.
243. При электролизе раствора CuSO4 на аноде выделилось 168 см3 кислорода, измеренного при н. у. Сколько граммов меди выделилось на катоде? Составьте электронные уравнения процессов, происходящих на электродах.
244. Сколько граммов воды разложилось при электролизе раствора Na2SO4 при силе тока 7 А в течение 5 ч? Составьте электронные уравнения процессов, происходящих на электродах.
245. Электролиз раствора нитрата серебра проводили при силе тока 2 А в течение 4 ч. Сколько граммов серебра выделилось на катоде? Составьте электронные уравнения процессов, происходящих на электродах.
246. Электролиз раствора сульфата некоторого металла проводили при силе тока 6 А в течение 45 мин, в результате чего на катоде выделилось 5,49 г металла. Вычислите эквивалент металла. Составьте электронные уравнения процессов, происходящих на электродах.
247. Составьте электронные уравнения процессов, происходящих на электродах при электролизе раствора КОН, расплава КОН.
248. Электролиз раствора сульфата цинка проводили в течение 5 ч, в результате чего выделилось 6 л кислорода, измеренного при н. у. Вычислите силу тока. Составьте электронные уравнения процессов, происходящих на электродах.
249. Составьте электронные уравнения процессов, происходящих на электродах при электролизе раствора А12(SO4)3 в случае угольного анода; в случае алюминиевого анода.
250. Какие вещества и в каком количестве выделятся на угольных электродах при электролизе раствора NaI в течение 2,5 ч, если сила тока равна 6 А? Составьте электронные уравнения процессов, происходящих на электродах.
251. При электролизе раствора AgNO3 масса серебряного анода уменьшилась на 5,4 г. Сколько электричества в кулонах израсходовано на этот процесс? Составьте электронные уравнения процессов, происходящих на электродах.
252. Какие вещества и в каком количестве выделяются на угольных электродах при электролизе раствора КВr в течение 1 ч 35 мин при силе тока 16 А? Составьте электронные уравнения процессов, происходящих на электродах.
253. Составьте электронные уравнения процессов, происходящих при электролизе CuCl2, если анод медный; если анод угольный?
254. На электролиз раствора CaCl2 израсходовано 10722,2 Кл электричества. Вычислите массу выделяющихся на угольных электродах и образующегося возле катода веществ. Составьте электронные уравнения процессов, происходящих на электродах.
255. Составьте электронные уравнения процессов, происходящих на электродах при электролизе раствора КС1; расплава КС1.
256. Сколько времени проводят электролиз раствора электролита при силе тока 5 А, если на катоде выделяется 0,1 г-экв вещества? Сколько выделится вещества на аноде? Составьте электронные уравнения процессов, происходящих на электродах.
257. При электролизе растворов MgSO4 и ZnCl2 , соединенных последовательно с источником тока, на одном из катодов выделилось 0,25 г водорода. Сколько граммов вещества выделится на другом катоде; на анодах? Составьте электронные уравнения процессов, происходящих на электродах.
258. Чему равна сила тока, если при электролизе раствора MgCl2 в течении 30 мин на катоде выделилось 8,4 л водорода, измеренного при н. у. Вычислите массу вещества, выделяющегося на аноде. Составьте электронные уравнения процессов, происходящих на электродах.
259. Сколько граммов Н2SO4 образуется возле анода при электролизе раствора Na2SO4, если на аноде выделяется 1,12 л кислорода, измеренного при н. у.? Вычислите массу вещества, выделяющегося на катоде. Составьте электронные уравнения процессов, происходящих на электродах.
260. Вычислите силу тока, зная, что при электролизе раствора КОН в течение 1 ч 15 мин 20 с на аноде выделилось 6,4 г кислорода. Какое вещество и в каком количестве выделяется на катоде? Составьте электронные уравнения процессов, происходящих на электродах.
Коррозия металлов*
Коррозия – это самопроизвольно протекающий процесс разрушения металлов в результате химического или электрохимического взаимодействия их с окружающей средой.
При электрохимической коррозии на поверхности металла одновременно протекает два процесса:
анодный – окисление металла
Ме0 – n ×ē = Men+,
катодный – восстановление ионов водорода
2H+ + 2ē = H2
или молекул кислорода, растворенного в воде
O2 + 2H2O +4ē = 4OH–.
Ионы или молекулы, которые восстанавливаются на катоде, называют деполяризаторами.
261. Как происходит атмосферная коррозия луженого и оцинкованного железа при нарушении покрытия? Составьте электронные уравнения анодного и катодного процессов.
262. Медь не вытесняет водород из разбавленных кислот. Почему? Однако, если к медной пластинке, опущенной в кислоту, прикоснуться цинковой, то на меди начинается бурное выделение водорода. Дайте этому объяснение, составив электронные уравнения анодного и катодного процессов. Напишите уравнение протекающей химической реакции.
263. Как происходит атмосферная коррозия луженого железа и луженой меди при нарушении покрытия? Составьте электронные уравнения анодного и катодного процессов.
264. Если пластинку из чистого цинка опустить в разбавленную кислоту, то начинающееся выделение водорода вскоре почти прекращается. Однако при прикосновении к цинку медной палочкой на последней начинается бурное выделение водорода. Дайте этому объяснение, составив электронные уравнения анодного и катодного процессов. Напишите уравнение протекающей химической реакции.
265. В чем заключается сущность протекторной защиты металлов от коррозии? Приведите пример протекторной защиты никеля в электролите, содержащем растворенный кислород. Составьте электронные уравнения анодного и катодного процессов.
266. Если на стальной предмет нанести каплю воды, то коррозии подвергается средняя, а не внешняя часть смоченного металла. После высыхания капли в ее центре появляется пятно ржавчины. Чем это можно объяснить? Какой участок металла, находящийся под каплей воды, является анодным и какой катодным? Составьте электронные и молекулярные уравнения соответствующих процессов.
267. Если гвоздь вбить во влажное дерево, то ржавчиной покрывается та его часть, которая находится внутри дерева. Чем это можно объяснить? Анодом или катодом является эта часть гвоздя? Составьте электронные уравнения соответствующих процессов.
268. В раствор соляной кислоты поместили цинковую пластинку и цинковую пластинку, частично покрытую медью. В каком случае процесс коррозии цинка происходит интенсивнее? Ответ мотивируйте, составив электронные уравнения соответствующих процессов.
269. Почему химически чистое железо является более стойким против коррозии, чем техническое железо? Составьте электронные уравнения анодного и катодного процессов, происходящих при коррозии технического железа во влажном воздухе и в сильнокислой среде.
270. Какое покрытиеметалла называется анодным и какое катодным? Назовите несколько металлов, которые могут служить для анодного и катодного покрытия железа. Составьте электронные уравнения анодного и катодного процессов, происходящих при коррозии железа, покрытого медью во влажном воздухе и в сильнокислой среде.
271. Железное изделие покрыли кадмием. Какое это покрытие – анодное или катодное? Почему? Составьте электронные уравнения анодного и катодного процессов коррозии этого изделия при нарушении покрытия во влажном воздухе и в соляной кислоте. Какие продукты коррозии образуются в первом и во втором случаях?
272. Железное изделие покрыли свинцом. Какое это покрытие – анодное или катодное? Почему? Составьте электронные уравнения анодного и катодного процессов коррозии этого изделия при нарушении покрытия во влажном воздухе и в соляной кислоте. Какие продукты коррозии образуются в первом и во втором случаях?
273. Две железные пластинки, частично покрытые одна оловом, другая медью, находятся во влажном воздухе. Обе ли пластинки подвержены коррозии? Почему? Составьте электронные уравнения возможных анодного и катодного процессов коррозии этих пластинок. Каков состав продуктов коррозии железа?
274. Железное изделие покрыли цинком. Какое это покрытие анодное или катодное? Почему? Составьте электронные уравнения анодного и катодного процессов коррозии этого изделия при нарушении покрытия во влажном воздухе и в разбавленной серной кислоте. Какие продукты коррозии образуются в первом и во втором случаях?
275. Если пластинку из чистого железа опустить в соляную кислоту, то выделение на ней водорода идет медленно и со временем почти прекращается. Однако, если цинковой палочкой прикоснуться к железной пластинке, то на последней начинается бурное выделение водорода. Почему? Какой металл при этом растворяется? Составьте электронные уравнения анодного и катодного процессов.
276. Цинковую и железную пластинки опустили в раствор сульфата меди. Составьте электронные и ионные уравнения реакций, происходящих на каждой из этих пластинок. Какие процессы будут проходить на пластинках, если наружные концы их соединить проводником?
277. Как влияет рН среды на скорость коррозии железа и цинка? Почему? Составьте электронные уравнения анодного и катодного процессов атмосферной коррозии этих металлов.
278. В раствор электролита, содержащего растворенный кислород, опустили цинковую пластинку и цинковую пластинку, частично покрытую медью. В каком случае процесс коррозии цинка происходит интенсивнее? Составьте электронные уравнения анодного и катодного процессов.
279. Железные бочки применяют для транспортировки концентрированной серной кислоты, но после освобождения от кислоты бочки часто совершенно разрушаются вследствие коррозии. Чем это можно объяснить? Что является анодом и что катодом? Составьте электронные уравнения соответствующих процессов.
280. Как протекает атмосферная коррозия железа, покрытого слоем никеля, если покрытие нарушено? Составьте электронные уравнения анодного и катодного процессов. Каков состав продуктов коррозии?
s -элементы (... ns 1-2)*
281. Какую степень окисления может проявлять водород в своих соединениях? Приведите примеры реакций, в которых газообразный водород играет роль окислителя, и в которых - роль восстановителя.
282. Напишите уравнения реакций натрия с водородом, кислородом, азотом и серой. Какую степень окисления приобретают атомы окислителя в каждой из этих реакций?
283. Напишите уравнения реакций с водой следующих соединений натрия:Na2O2, Na2S, NaH, Na3N.
284. Как получают металлический натрий? Составьте электронные уравнения процессов, проходящих на электродах при электролизе расплава NaOH.
285. Какие свойства может проявлять перекись водорода в окислительно-восстановительных реакциях? Почему? На основании электронных уравнений напишите уравнения реакции Н2О2: а) с Ag2O; б) с KI.
286. Почему перекись водорода способна диспропорционировать (самоокисляться - самовосcтанавливаться)? Составьте электронные и молекулярные уравнения процесса разложения Н2О2.
287. Как можно получить гидрид и нитрид кальция? Напишите уравнения реакций этих соединений с водой. К окислительно-восстановительным реакциям составьте электронные уравнения.
288. Назовите три изотопа водорода. Укажите состав их ядер. Что такое тяжелая вода? Как она получается и каковы ее свойства?
289. Гидроксид какого из s- элементов проявляет амфотерные свойства? Составьте молекулярные и ионные уравнения реакций этого гидроксида: а) с кислотой; б) со щелочью.
290. При пропускании диоксида углерода через известковую воду (раствор (Са(ОН)2) образуется осадок, который при дальнейшем пропускании СО2 растворяется. Дайте объяснение этому явлению. Составьте уравнения реакций.
291. Составьте электронные и молекулярные уравнения реакций: а) бериллия с раствором щелочи; б) магния с концентрированной серной кислотой, имеяв видумаксимальное восстановление последней.
292. При сплавлении оксид бериллия взаимодействует с диоксидом кремния и с оксидом натрия. Напишите уравнения соответствующих реакций. О каких свойствах ВеО говорят эти реакции?
293. Какие соединения магния и кальция применяются в качестве вяжущих строительных материалов?Чемобусловлены их вяжущие свойства?
294. Как можно получить карбид кальция? Что образуется при его взаимодействии с водой? Напишите уравнения соответствующих реакций.
295. Как можно получить гидроксиды щелочных металлов? Почему едкие щелочи необходимо хранить в хорошо закрытой посуде? Составьте уравнения реакций, происходящих при насыщении едкого натра: а) хлором; б) сернистым ангидридом; в) сероводородом.
296. Чем можно объяснить большую восстановительную способность щелочных металлов? При сплавлении едкого натра с металлическим натрием последний восстанавливает водород щелочи в гидрид-ион. Составьте электронные и молекулярное уравнения этой реакции.
297. Какое свойство кальция позволяет применять его в металлотермии для получения некоторых металлов из их соединений? Составьте электронные и молекулярные уравнения реакций кальция: а) с V2O5; б) с СаSO4. В каждой из этих реакций окислитель восстанавливается максимально, приобретая низшую степень окисления.
298. Какие соединения называются негашеной и гашеной известью? Составьте уравнения реакций ихполучения. Какое соединение образуется при накаливании негашеной извести с углем? Что является окислителем и восстановителем в последней реакции? Составьте электронные и молекулярные уравнения.
299. Составьте электронные и молекулярные уравнения реакций: а) кальция с водой; б) магния с азотной кислотой, учитывая максимальное восстановление последней.
300. Составьте уравнения реакций, которые нужно провести для осуществления следующих превращений;
Са ® СаH2 ® Ca(ОН)2 ® СаСО3 ® Сa(НCO3)2.
Жесткость воды и методы ее устранения
Пример 1. Вычислить жесткость воды, зная, что в 500 л ее содержится 202,5 г Са(НСO3)2.
Решение. В 1л воды содержится 202,5: 500 = 0,405 г Са(НСО3)2, что составляет 0,405: 81 = 0,005 г-экв, или 5 мг-экв (81—эквивалент Са(НСО3)2). Следовательно, жесткость воды 5 мг-экв.
Пример 2. Сколько граммов СаSO4 содержится в 1 м3 воды, если жесткость, обусловленная присутствием этой соли, равна 4 мг-экв?
Решение. Грамм-молекула СаSO4 136,14 г; грамм-эквивалент равен половине грамм-молекулы, т. е. 68,07 г., а миллиграмм-эквивалент 68,07 мг. В 1 м3 воды с жесткостью 4 мг-экв содержится 4×1000 = 4000 мг-экв, или 4000×´ ×68,07 = 272280 мг = 272,280 г СаSO4.
Пример 3. Сколько граммов соды надо прибавить к 500 л воды, чтобы устранить ее жесткость, равную 5 мг-экв?
Решение. В 500 л воды содержится 500 × 5 = 2500 мг-экв или 2,5 г-экв солей, обусловливающих жесткость воды. Для устранения жесткости следует прибавить 2,5 × 53 = 132,5 г cоды (53 г – г-экв Na2CO3).
Пример 4. Вычислить карбонатную жесткость воды, зная, что на титрование 100 см3 этой воды, содержащей гидрокарбонат кальция, потребовалось 6,25 см3 0,08 н раствора НСl.
Решение. Вычисляем нормальность раствора гидрокарбоната кальция. Обозначив число грамм-эквивалентов растворенного вещества в 1 л раствора, т. е. нормальность, через х, составляем пропорцию:
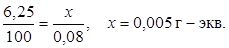
Таким образом, в 1 л исследуемой воды содержится 0,005×1000 = 5 мг-экв гидрокарбоната кальция или 5 мг-экв Са2+-ионов. Карбонатная жесткость воды 5 мг-экв.
Приведенные примеры решают, используя формулу
Ж=т/ЭV,
где m - масса вещества, обусловливающего жесткость воды или применяемого для устранения жесткости воды, мг; Э - эквивалент этого вещества; V - объем воды, л.
Решение примера 1.
Ж = т/ЭV = 202500/81×500 = 5 мг-экв.
81 - эквивалентСа(НСО3)2, равный половине егомолекулярного веса.
Решение примера 2. Из формулы Ж = m /ЭV = 4 68,07×1000 = 272280 мг = 272,280 г СаSO4.
301. Сколько граммов Na3РO4 надоприбавить к 500 лводы, чтобы устранятьее карбонатнуюжесткость, равную5 мг-экв?
302. Какие соли обуслoвливают жесткость природной воды? Какую жесткость называют карбонатной,некарбонатной? Как можно устранить карбонатную, некарбонатную жесткость? Напишите уравнения соответствующих реакций.
303. Вычислите карбонатную жесткость воды, зная, что для реакции с гидрокарбонатом кальция, содержащимся в 200 см3 воды, требуется 15 см3 0,08 н., раствора НСl.
304. В 1 л воды содержится 36,47 мг-ион магния и 50,1 мг-ион кальция. Чему равна жесткость этой воды?
305. Сколько граммов карбоната натрия надо прибавить к 400 л воды, чтобы устранить жесткость, равную 3 мг-экв?
306. Вода содержащая только сульфат магния, имеет жесткость 7 мг-экв. Сколько граммов сульфата магния содержится в 300 л этой воды?
307. Вычислите жесткость воды, зная, что в 600 л еесодержатся 65,7 г гидрокарбоната магния и 61,2 г сульфата кальция.
308. В 220 л воды содержится 11 г сульфатамагния.Чему равна жесткость этой воды?
309. Жесткость воды, в которой растворен только гидрокарбонат кальция, равна 4 мг-экв. Сколько 0,1 н. раствора НСI потребуется для реакции с гидрокарбонатом кальция, содержащимся в 75 см3 этой воды?
300. В 1 м3 воды содержится140 г сульфата магния.Вычислите жесткость этой воды.
311. Вода, содержащая только гидрокарбонат магния, имеет жесткость 3,5 мг-экв. Сколько граммов гидрокарбоната магния содержится в 200 л этой воды?
312. К 1 м3 жесткой воды прибавили 132,5 г карбоната натрия. На сколько миллиграмм-эквивалентов понизилась жесткость?
313. Чему равна жесткость воды, если для ее устранения к 50 л воды потребовалось прибавить 21,2 г карбоната натрия?
314. Сколько граммов СаSO4 содержится в 200 л воды, если жесткость, обусловливаемая этой солью, равна 8 мг-экв?
315. Вода, содержащая только гидрокарбонат кальция, имеет жесткость 9 мг-экв. Сколько граммов гидрокарбоната кальция содержится в 600 л этой воды?
316. Какие надо удалить ионы из природной воды, чтобы сделать ее мягкой? Введением каких ионов можно умягчить воду? Составьте уравнения соответствующих реакций.
317. Сколько граммов карбоната натрия надо прибавить к 0,1 м3 воды, чтобы устранить жесткость, равную 4 мг-экв?
318. К 100 л жесткой воды прибавили 12, г гидроксида кальция. На сколько миллиграмм-эквивалентов понизилась карбонатная жесткость?
319. Чему равна карбонатная жесткость воды, если в 1 л ее содержится 0,292 г гидрокарбоната магния и 0,2025 г гидрокарбоната кальция?
320. Сколько граммов гидроксида кальция надо прибавить к 275 л воды, чтобы устранитьее карбонатную жесткость, равную 5,5 мг-экв?
p -элементы (… ns 2 nр 1-6)*
321. Составьте уравнения реакций, которые нужно провести, для осуществления следующих превращений:
Аl ® Al2(SO4)3 ® Na[Al(OH)4] ® Al(NO3)3.
322. Составьте электронные и молекулярные уравнения реакций: а) алюминия с раствором щелочи; б) бора с концентрированной азотной кислотой.
323. Какой процесс называется алюминотермией? Составьте электронные и молекулярное уравнения реакции, восстановления металлического хрома из оксида хрома (III) алюминием.
324. Составьте уравнения реакций, которые нужно провести для осуществления следующих превращений: В ® Н3ВО3 ® Nа2В4O7 ® H3ВО3. Уравнение окислительно-восстановительной реакции составьтена основании электронных уравнений.
325. Какая степень окисления наиболее характерна для олова и какая для свинца? Составьте электронные и молекулярные уравнения реакций олова и свинца с концентрированной азотной кислотой.
326. Чем можно объяснить восстановительные свойства соединений олова (+2) и окислительные – cвинца (+4)? На основании электронных уравнений составьте уравнения реакций: а) SnCl2 с НgСl2; б) РbО2 с НСlконц.
327. Какие оксиды и гидроксиды образуют олово и свинец? Как изменяются их кислотно-основные и окислительно-восстановительные свойства в зависимости от степени окисления элементов? Составьте молекулярные и ионные уравнения реакций взаимодействия раствора едкого натра: а) с оловом; б) с дигидроксидом свинца.
328. При высокой температуре алюминий взаимодействует с азотом, серой и углеродом. Напишите электронные и молекулярные реакции получения нитрида, сульфида и карбида алюминия. Какие продукты образуются при взаимодействии этих соединений с водой?
329. На основании электронных уравнений составьте уравнение реакции фосфора с азотной кислотой, учитывая, что фосфор окисляется максимально, а азот восстанавливается минимально.
330. Почему атомы большинства р -элементов способны к реакциям диспропорционирования (самоокисления – самовосстановления)? На основании электронных уравнений напишите уравнение реакции растворения серы в концентрированном растворе щелочи. Один из продуктов содержит серу со степенью окисления +4.
331. Почему сернистая кислота может проявлять как окислительные, так и восстановительные свойства? На основании электронных уравнений составьте уравнения реакций Н2SO3: а) с сероводородом; б) с хлором.
332. Какие свойства проявляет сероводород в окислительно-восстановительных реакциях? Почему? Составьте электронные и молекулярные, уравнения реакций взаимодействия раствора сероводорода: а) с хлором; б) с кислородом.
333. Почему азотистая кислота может проявлять как окислительные, так и восстановительные свойства? На основании электронных уравнений составьте уравнения реакций НNO2: а) с бромной водой; б) с НI.
334. Почему диоксид азота способен к реакциям самоокисления — самовосстановления (диспропорционирования)? На основании электронных уравнений напишите уравнение реакции растворения NО2 в едком натре.
335. Какие свойства в окислительно-восстановительных реакциях проявляет серная кислота? Напишите уравнения реакций взаимодействия разбавленной серной кислоты с магнием и концентрированной – с медью. Укажите окислитель и восстановитель.
336. В каком газообразном соединении азот проявляет свою низшую степень окисления? Напишите уравнения реакций получения этого соединения: а) при взаимодействии хлорида аммония с гидроксидом кальция; б) разложением нитрида магния водой.
337. Почему фосфористая кислота способна к реакциям самоокисления – самовосстановления (диспропорционирования)? На основании электронных уравнений составьте уравнение процесса разложения Н3РО3, учитывая, что при этом фосфор приобретает минимальную и максимальную степень окисления.
338. В каком газообразном соединении фосфор проявляет свою низшую степень окисления? Напишите уравнения реакций: а) получения этого соединения при взаимодействии фосфида кальция с соляной кислотой; б) горения его в кислороде.
339. Какую степень окисления могут проявлять мышьяк, сурьма и висмут в соединениях? Какая степень окисления является более характерной для каждого из них? Почему? Составьте электронные и молекулярные уравнения реакций: а) мышьяка с концентрированной азотной кислотой; б) висмута с концентрированной серной кислотой.
340. Как изменяются окислительные свойства галогенов при переходе от фтора к иоду и восстановительные свойства их отрицательно заряженных ионов? Почему? Составьте электронные и молекулярные уравнения реакций: а) Сl2 + l2 + H2O =?; б) Кl + Вr2 =. Укажите окислитель и восстановитель.
341. Составьте электронные и молекулярные уравнения реакции, происходящей при пропускании хлора через горячий раствор едкого кали. К какому типу окислительно-восстановительных процессов относится данная реакция?
342. Какие реакции нужно провести для осуществления следующих превращений: NаСl ® НСl ® Cl2 ® КСlO3. Уравнения окислительно-восстано-вительных реакций составьте на основании электронных уравнений.
343. К раствору, содержащему SbСl3 и ВiСl3, добавили избыток раствора едкого кали. Напишите молекулярные и ионные уравнения происходящих реакций. Какое вещество находится в осадке?
344. Чем существенно отличается действие разбавленной азотной кислоты на металлы от действия соляной и разбавленной серной кислот? Что является окислителем в первом случае, что – в двух других. Приведите примеры.
345. Напишите формулы и назовите кислородные кислоты хлора, укажите степень окисления хлора в каждой из них. Какая из этих кислот является более сильной? Почему? Какие свойства проявляет соли этих кислот в окислительно-восстановительных реакциях? Приведите примеры.
346. Напишите формулы оксидов азота в различных степенях окисления. Какие из оксидов являются кислотообразующими? Составьте формулы соответствующих кислот. Какие свойства может проявлять азотистая кислота и ее соли в окислительно-восстановительных реакциях? Составьте электронные уравнения следующих реакций:
KNO2 + Cl2 + H2O → KNO3 + HCl,
KNO2 + KI + H2SO4 → NO + I2 + K2SO4 + H2O.
|
|
|
|
|
Дата добавления: 2014-12-17; Просмотров: 826; Нарушение авторских прав?; Мы поможем в написании вашей работы!