
КАТЕГОРИИ:
Архитектура-(3434)Астрономия-(809)Биология-(7483)Биотехнологии-(1457)Военное дело-(14632)Высокие технологии-(1363)География-(913)Геология-(1438)Государство-(451)Демография-(1065)Дом-(47672)Журналистика и СМИ-(912)Изобретательство-(14524)Иностранные языки-(4268)Информатика-(17799)Искусство-(1338)История-(13644)Компьютеры-(11121)Косметика-(55)Кулинария-(373)Культура-(8427)Лингвистика-(374)Литература-(1642)Маркетинг-(23702)Математика-(16968)Машиностроение-(1700)Медицина-(12668)Менеджмент-(24684)Механика-(15423)Науковедение-(506)Образование-(11852)Охрана труда-(3308)Педагогика-(5571)Полиграфия-(1312)Политика-(7869)Право-(5454)Приборостроение-(1369)Программирование-(2801)Производство-(97182)Промышленность-(8706)Психология-(18388)Религия-(3217)Связь-(10668)Сельское хозяйство-(299)Социология-(6455)Спорт-(42831)Строительство-(4793)Торговля-(5050)Транспорт-(2929)Туризм-(1568)Физика-(3942)Философия-(17015)Финансы-(26596)Химия-(22929)Экология-(12095)Экономика-(9961)Электроника-(8441)Электротехника-(4623)Энергетика-(12629)Юриспруденция-(1492)Ядерная техника-(1748)
Параметри GasFET сенсорів на водень. Сенсори інших газів на основі польового транзистора. Модель чутливості до аміаку МОН-структури. Польовий транзистор з підвішеною мембраною
|
|
|
|
Принцип дії сенсору GasFET сенсора на водень. Модель чутливості до водню для Pd затворів. Як розрахувати парціальний тиск водню? Як впливає на чутливість до водню атмосферний кисень?
Принцип дії сенсору GasFET сенсора на водень. У структурі, яка має назву GasFET (газовий польовий транзистор), як затворний метал використовують плівку Pd або інших перехідних металів, які є каталізаторами до водню. Молекули водню з атмосфери адсорбуються на поверхні каталізатора й дисоціюють на атоми водню, частина атомів водню дифундує крізь шар Pd і адсорбується в інтерфейсі Pd-оксид (або інший діелектрик). Кількість
адсорбованих атомів водню в інтерфейсі визначається концентрацією молекул водню в атмосфері та хімічними реакціями на поверхні. В інтерфейсі адсорбовані атоми водню поляризуються і створюють дипольний шар, який змінює потенціал затвора на величину ΔV, що зменшує роботу виходу металу в інтерфейсі.
|
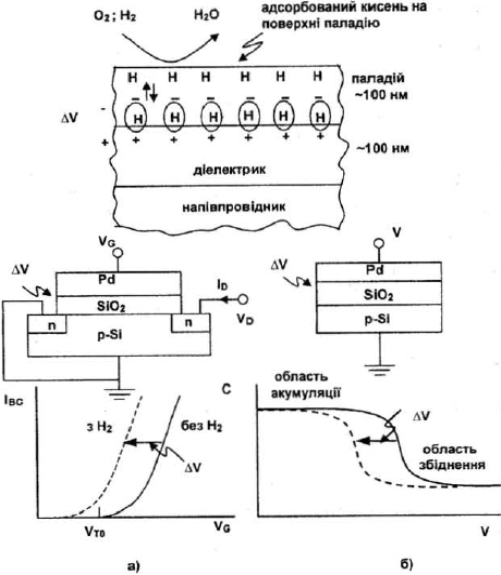
| Рис. 3.2. МОН-структура Pd–SiO2–p-Si за присутності молекул водню та кисню (нагорі): а) схема вимірювань і крива струму витік – стік залежно від напруги на затворі транзистора; б) МОН-ємність і відповідні ВФХ. Стрілка показує напрямок зсуву характеристик при адсорбції водню на поверхні паладію |
Як сенсор водню МОН-структура може працювати в режимі польового транзистора чи МОН-ємності (рис. 3.2). У першому випадку вимірюється струм витік – стік залежно від прикладеної до затвора напруги, у другому – зміна ємності структури. За присутності адсорбованого водню крива струму витік – стік від напруги затвора зсувається вздовж осі напруг на величину ΔV, оскільки порогова напруга VT для виникнення інверсного шару зменшується:
VT=VTO-ΔV (3.7) де VTO – порогова напруга виникнення інверсного шару без присутності водню. Аналогічно, ємність МОН-структури також зсувається вздовж осі напруг на величину ΔV, оскільки напруга плоских зон VFB залежить від роботи виходу металу й входить до величини VT (вирази (3.5), (3.6)).
|
|
|
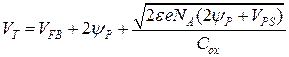 (3.5) де ψp – потенціал у р-області, Vps – напруга зворотного зміщення на підкладці, а величина напруги плоских зон VFB дорівнює:
(3.5) де ψp – потенціал у р-області, Vps – напруга зворотного зміщення на підкладці, а величина напруги плоских зон VFB дорівнює:
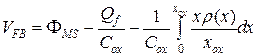 (3.6)
(3.6)
Величина ΔV дорівнює:
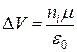 (3.8)
(3.8)
де ni – кількість атомів водню в області інтерфейсу (на одиниці поверхні, см–2), μ – дипольний момент адсорбованих атомів водню в інтерфейсі, ε0 – діелектрична проникність вакууму. Зростання ΔV відповідає зменшенню роботи виходу металу.
Для того, щоб описати фізико-хімічні причини виникнення зміни електричних характеристик МОН-структури необхідно розглянути три різних процеси: 1) поверхневі реакції, які ведуть до адсорбції атомів водню на зовнішній поверхні металу; 2) транспорт атомів водню крізь плівку каталітичного металу; 3) утворення диполів в інтерфейсі метал–діелектрик чи метал–напівпровідник (у випадку контакту типу Шотткі).
Модель чутливості до водню для Pd затворів.
Основні припущення моделі такі (рис. 3.3):
1) молекули водню адсорбуються та дисоціюють на поверхні каталізатора. Концентрація адсорбованих атомів на поверхні пропорційна парціальному тиску водню та кількості вільних вузлів адсорбції;
|
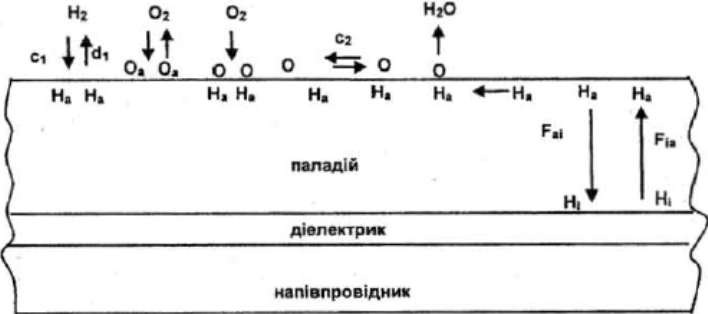
| Рис. 3.3. Хімічні реакції при адсорбції водню та кисню на МОН-структурі з паладієм |
2) водень десорбується з поверхні металу за рахунок рекомбінації та утворення молекул Н2 чи за рахунок хімічної реакції з киснем і утворенням молекул води. Тобто механізми 1 та 2 описуються такими реакціями:
· дисоціація молекул водню H2à2Ha (зі швидкістю c1);
· рекомбінація адсорбованих атомів водню 2НаàН2 (зі швидкістю d1);
· дисоціація молекул кисню О2à2Оа;
· рекомбінація адсорбованих атомів кисню 2ОаàО2;
|
|
|
· утворення та десорбція молекул води 4На+О2à2Н2О.
Залежно від температури реакції утворення води та гідроксилів можуть відбуватися також за іншими каналами (рис. 3.3), а саме:
· з утворенням адсорбованих OH -груп 2На+О2à2ОНа, (зі швидкістю c2) На+ОаàОНа;
· дисоціації ОН-груп ОНаàОа+На;
· утворенням молекул води ОНа+НаàН2О.
При балансі вказаних реакцій встановлюється рівноважній стан, який залежить від співвідношень парціальних тисків водню та кисню.
3) атоми водню дифундують крізь метал і адсорбуються в інтерфейсі метал–діелектрик. Завдяки дуже високій швидкості дифузії (час дифузії крізь 200нм шар паладію дорівнює 10мкс при 150 0С та 0,15мс при кімнатній температурі) завжди існує рівновага між кількістю водневих атомів на двох поверхнях: На«Нi;
4) атоми водню, які адсорбуються в інтерфейсі метал–діелектрик, стають поляризованими, що веде до зсуву напруги ΔV, який пропорційний кількості адсорбованих водневих атомів в інтерфейсі (3.8).
Як розрахувати парціальний тиск водню? Як впливає на чутливість до водню атмосферний кисень? Ці реакції можуть бути виражені простими кінетичними рівняннями для коефіцієнта покриття поверхні металу адсорбованими атомами водню θa (відношення кількості адсорбованого водню на загальну кількість вузлів адсорбції на поверхні каталізатора) з урахуванням лише найбільш вірогідних реакцій. Тоді з припущень 1 та 2 випливає, що адсорбція атомів кисню блокує хімічні реакції на поверхні. Якщо формування молекул ОНа іде за рахунок адсорбованих атомів водню і молекулярного кисню, то емпірично можна встановити, що:
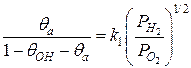 (3.9)
(3.9)
де θOH – покриття ОН-групами поверхні каталізатора, PH2 та PO2 – парціальний тиск Н2 і О2, відповідно, θa пропорційне квадратному кореню з парціального тиску водню за умови θa << 1 - θOH і PO2 = const.
Якщо ОНа створюються за рахунок адсорбованих кисню та водню і процес дисоціації ОНа швидкий, то адсорбовані кисневі атоми блокуватимуть дисоціацію молекул водню і співвідношення (3.9) буде іншим:
 (3.10)
(3.10)
де нехтуємо рекомбінацією двох атомів водню в молекулу водню, оскільки швидкість утворення молекул води значно вища за швидкість рекомбінації при концентрації кисню порядку відсотків. Якщо атмосфера інертна, то спонтанна рекомбінація атомів водню вже істотна й тоді:
|
|
|
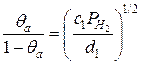 (3.11)
(3.11)
Ці результати можуть бути зрозумілими на підставі аналізу простих кінетичних рівнянь для θa. Рівняння (3.9) можна отримати з кінетичного рівняння:
d(a)011H(2O1H)2a2O222aaiiacPcPFF
 (3.12)
(3.12)
де θ0 – це покриття атомами кисню, яке блокує дисоціацію водню на поверхні, Fai та Fia – це потоки атомів водню з поверхні в діелектричний шар, і навпаки (рис. 3.3), які однакові за рівноважних умов. Введемо величину ступеня покриття воднем інтерфейсу метал–діелектрик θi. Тоді для цих потоків можна записати:
 (3.13)
(3.13)
де c, d – відповідно, швидкості дифузії HaàHi та HiàHa. За рівноважних умов Fai=Fia. Звідси
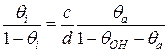 (3.14)
(3.14)
Якщо вузли адсорбції на поверхні та в інтерфейсі мають одну природу й однакову теплоту адсорбції, то c/d=1. Ця умова виконується для паладієвої МОН-структури при роботі за атмосферних умов. Таким чином, концентрація атомів водню в інтерфейсі визначається концентрацією молекул водню у вимірюваній атмосфері та хімічними реакціями на поверхні каталізатора. В інтерфейсі при адсорбції атомів водню виникає дипольний шар і додаткове падіння напруги, яке змінює роботу виходу металу в інтерфейсі. Якщо припустити, що
ΔV=ΔVmaxθi (3.15)
то можна отримати рівняння для залежності зсуву I-V та C-V характеристик від парціального тиску водню й кисню:
 (3.16)
(3.16)
або від парціального тиску водню в інертній атмосфері:
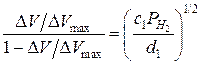 (3.17)
(3.17)
де K – постійна, а функція f (PO2), згідно з рівняннями (3.9) та (3.10) дорівнює PO2 або PO21/2. Тобто напруга зсуву залежить як корінь квадратний від парціального тиску водню
|
|
|
|
|
Дата добавления: 2015-01-03; Просмотров: 359; Нарушение авторских прав?; Мы поможем в написании вашей работы!