
КАТЕГОРИИ:
Архитектура-(3434)Астрономия-(809)Биология-(7483)Биотехнологии-(1457)Военное дело-(14632)Высокие технологии-(1363)География-(913)Геология-(1438)Государство-(451)Демография-(1065)Дом-(47672)Журналистика и СМИ-(912)Изобретательство-(14524)Иностранные языки-(4268)Информатика-(17799)Искусство-(1338)История-(13644)Компьютеры-(11121)Косметика-(55)Кулинария-(373)Культура-(8427)Лингвистика-(374)Литература-(1642)Маркетинг-(23702)Математика-(16968)Машиностроение-(1700)Медицина-(12668)Менеджмент-(24684)Механика-(15423)Науковедение-(506)Образование-(11852)Охрана труда-(3308)Педагогика-(5571)Полиграфия-(1312)Политика-(7869)Право-(5454)Приборостроение-(1369)Программирование-(2801)Производство-(97182)Промышленность-(8706)Психология-(18388)Религия-(3217)Связь-(10668)Сельское хозяйство-(299)Социология-(6455)Спорт-(42831)Строительство-(4793)Торговля-(5050)Транспорт-(2929)Туризм-(1568)Физика-(3942)Философия-(17015)Финансы-(26596)Химия-(22929)Экология-(12095)Экономика-(9961)Электроника-(8441)Электротехника-(4623)Энергетика-(12629)Юриспруденция-(1492)Ядерная техника-(1748)
В кислой среде индикатор фенолфталеин будет
|
|
|
|
бесцветным.
В растворе при... лакмус окрасится в красный цвет.
рН<7
В растворе при... фенолфталеин окрасится в малиновый цвет.
рН>7
В присутствии щелочей фенолфталеин окрасится:
малиновой.
Уравнение закона эквивалентов:
C1V1=C2V2
Титрование – это добавление:
эквивалентного количества раствора с известной концентрацией к раствору с неизвестной концентрацией
Титрантами ацидиметрического титрования являются:
HCl,H2SO4
Титрантами алкалиметрического титрования являются:
NaOH,KOH
Титрантом метода перманганатометрии является:
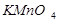 KMnO4
KMnO4
Если соляную кислоту титровать 0,1н NaОН, то это... способ титрования
прямой
На титрование 50мл 0,2н  пошло 25мл
пошло 25мл  . Нормальность кислоты равна:
. Нормальность кислоты равна:
0,4 н
На титрование 30мл 0,5н  пошло 50мл
пошло 50мл 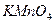 . Нормальность
. Нормальность 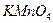 равна:
равна:
0,3 н
Объем 0,2н серной кислоты, пошедший на титрование 40мл 0,20н  равен... см3.
равен... см3.
При титровании cоляной кислоты щелочью используется... индикатор.
метилоранж
Кислотно – основное титрование основано на:
переносе протонов.
Титр раствора –это масса вещества:
в граммах, содержащая в 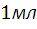 раствора.
раствора.
Титриметрический анализ основан на:
измерении точного объема титранта и анализируемого вещества.
Метод титриметрии основан на законе:
эквивалентов.
В основе кислотно-основного титрования лежит реакция:
нейтрализации.
В основе оксидиметрического титрования лежит реакция:
окисления-восстановления.
На титрование 10мл  пошло 15мл 0,1н
пошло 15мл 0,1н  . Концентрация
. Концентрация  равна:
равна:
0,15 н
На титрование 20мл соляной кислоты пошло 25мл 2н натрия гидроксида. Эквивалентная концентрация соляной кислоты равна:
2,5 н
Титрантом для  является:
является:
NaOH
0,04г вещества растворено в 100мл раствора. Титр этого раствора равен:
0,0004 г/мл
0,2г вещества растворено в 10мл раствора. Титр этого раствора равен:
|
|
|

Кислотно-основным методом определяют:

Мерным посудам относится:
пипетка, бюретка, мерная колба
Точка эквивалентности – это:
завершение процесса титрования
В титириметрическом методе индикаторы применяются для определения:
точки эквивалентности.
На нейтрализацию 15мл 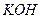 пошло 15мл 0,1 н
пошло 15мл 0,1 н  . Концентрация
. Концентрация 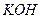 равна:
равна:
0,1 н
На титрование 10мл  пошло 12мл 0,2н
пошло 12мл 0,2н  . Нормальная концентрация
. Нормальная концентрация  равна:
равна:
0,24 н
На титрование 15мл  пошло 16мл. 0,1н
пошло 16мл. 0,1н  . Нормальная концентрация
. Нормальная концентрация  равна:
равна:
0,106 н
10 мл 0,1н  титровали с 0,2н
титровали с 0,2н 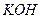 . Объем израсходованного
. Объем израсходованного 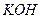 равен... мл.
равен... мл.
В методе перманганатометрии точку эквивалентности устанавливают:
без индикатора.
Титрантами иодометрического титрования являются:
I2, Na2S2O3
Индикатором иодометрического титрования является:
крахмал
Реакция комплексонометрического метода - это:
образования комплексного соединения
Медленное добавление титранта к анализируемому веществу – это:
титрование.
Метод титрования кислоты щелочью называется:
алкалиметрией.
Метод титрования щелочи кислотой называется:
ацидиметрией
Формула титра:
T=m/V
Расчетная формула титра:
T=Cн*Mэ/1000
В законе эквивалентов используется... концентрация.
нормальная
Рабочий раствор, используемый для титрования называется:
только растворы окислителей
Для химической реакции 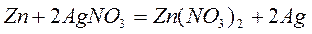 схема гальванического элемента:
схема гальванического элемента:
Zn/Zn2+//Ag+/Ag
Для химической реакции  схема гальванического элемента:
схема гальванического элемента:
Mg/Mg2+//Ag+/Ag
Для химической реакции  схема гальванического элемента:
схема гальванического элемента:
Fe/Fe2+//Hg2+/Hg
Для химической реакции 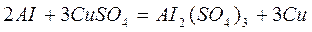 схема гальванического элемента:
схема гальванического элемента:
Al /Al3+//Cu2+Cu
В гальваническом элементе Ca/Ca2+//Pt2+/Pt протекает электрохимическая реакция:
Ca0+Pt2+=Ca2++Pt0
В гальваническом элементе Zn/Zn2+//Cu2+/Cu протекает электрохимическая реакция:
Zn0+Cu2+=Cu0+Zn2+
В гальваническом элементе Ni/Ni2+//Ag+/Ag протекает электрохимическая реакция:
Ni0+2Ag+=Ni2++2Ag0
В гальваническом элементе Sn/Sn2+//Au+/Au протекает электрохимическая реакция:
|
|
|
Sn0+2Au+=Sn2++2Au0
Потенциал стандартного водородного электрода:
j0=0
Условия стандартного водородного электрода:
aH+=1
Условия индикаторного водородного электрода:
аН+¹1
|
|
|
|
|
Дата добавления: 2015-04-24; Просмотров: 1334; Нарушение авторских прав?; Мы поможем в написании вашей работы!