
КАТЕГОРИИ:
Архитектура-(3434)Астрономия-(809)Биология-(7483)Биотехнологии-(1457)Военное дело-(14632)Высокие технологии-(1363)География-(913)Геология-(1438)Государство-(451)Демография-(1065)Дом-(47672)Журналистика и СМИ-(912)Изобретательство-(14524)Иностранные языки-(4268)Информатика-(17799)Искусство-(1338)История-(13644)Компьютеры-(11121)Косметика-(55)Кулинария-(373)Культура-(8427)Лингвистика-(374)Литература-(1642)Маркетинг-(23702)Математика-(16968)Машиностроение-(1700)Медицина-(12668)Менеджмент-(24684)Механика-(15423)Науковедение-(506)Образование-(11852)Охрана труда-(3308)Педагогика-(5571)Полиграфия-(1312)Политика-(7869)Право-(5454)Приборостроение-(1369)Программирование-(2801)Производство-(97182)Промышленность-(8706)Психология-(18388)Религия-(3217)Связь-(10668)Сельское хозяйство-(299)Социология-(6455)Спорт-(42831)Строительство-(4793)Торговля-(5050)Транспорт-(2929)Туризм-(1568)Физика-(3942)Философия-(17015)Финансы-(26596)Химия-(22929)Экология-(12095)Экономика-(9961)Электроника-(8441)Электротехника-(4623)Энергетика-(12629)Юриспруденция-(1492)Ядерная техника-(1748)
Основные термины
|
|
|
|
1. Атомная орбиталь -часть пространства вокруг ядра, в котором вероятность нахождения электрона максимальна. Это такое состояние электрона в атоме, которое имеет пространственные и энергетические характеристики.
2. Водородная связь - это слабое электростатическое взаимодействие между водородным атомом, ковалентная связь которого с другим атомом резко полярная, и другим электроотрицательным атомом, имеющим неподелённую пару электронов.Водородная связь между двумя фрагментами одной молекулы называется внутримолекулярной, а между двумя разными молекулами - межмолекулярной.
3. Гибридизация - своеобразная комбинация атомных орбиталей, имевших разную конфигурацию и разную энергию, в результате чего образуются орбитали одинаковой конфигурации с равным запасом энергии. Тип гибридизации (sp3, sp2 или sp) определяется числом
р-орбиталей, принимающих участие в гибридизации с одной s-орбиталью. Гибридные орбитали свойственны только атомам в молекулах, а не отдельным атомам в свободном состоянии. Все гибридные орбитали отличаются пространственной ориентацией:
sp3-орбитали расположены под углом 109028′; sp2-орбитали - под углом 1200; sp -орбитали - под углом 1800.
Чтобы по структурной формуле определить состояние гибридизации атомоа в молекуле, необходимо определить число "групп", связанных с интересующим атомом (под "группами " подразумевают атомы и неподелённые пары электронов) Если с исследуемым атомом связаны четыре "группы" - sp3 -гибридизация, если три - sp2-гибридизация, и если две - sp –гибридизация.
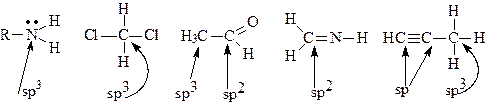
4 Донорно-акцепторная (координационная) связь- ковалентная связь,образованная за счет пары электронов одного атома.
5. Индуктивный эффект - перераспределение электронной
плотности в системе σ-связей, которое возникает вследствие разной
электроотрицательности атомов, участвующих в образовании связей
6. Ковалентная связь - связь между двумя атомами за счет обобщенной электронной пары. Она может рассматриваться как результат электростатического притяжения ядер двух атомов к этой электронной паре. Ковалентная связь бывает двух типов: σ-связь и π-.
|
|
|
|
|
Дата добавления: 2015-05-26; Просмотров: 398; Нарушение авторских прав?; Мы поможем в написании вашей работы!