
КАТЕГОРИИ:
Архитектура-(3434)Астрономия-(809)Биология-(7483)Биотехнологии-(1457)Военное дело-(14632)Высокие технологии-(1363)География-(913)Геология-(1438)Государство-(451)Демография-(1065)Дом-(47672)Журналистика и СМИ-(912)Изобретательство-(14524)Иностранные языки-(4268)Информатика-(17799)Искусство-(1338)История-(13644)Компьютеры-(11121)Косметика-(55)Кулинария-(373)Культура-(8427)Лингвистика-(374)Литература-(1642)Маркетинг-(23702)Математика-(16968)Машиностроение-(1700)Медицина-(12668)Менеджмент-(24684)Механика-(15423)Науковедение-(506)Образование-(11852)Охрана труда-(3308)Педагогика-(5571)Полиграфия-(1312)Политика-(7869)Право-(5454)Приборостроение-(1369)Программирование-(2801)Производство-(97182)Промышленность-(8706)Психология-(18388)Религия-(3217)Связь-(10668)Сельское хозяйство-(299)Социология-(6455)Спорт-(42831)Строительство-(4793)Торговля-(5050)Транспорт-(2929)Туризм-(1568)Физика-(3942)Философия-(17015)Финансы-(26596)Химия-(22929)Экология-(12095)Экономика-(9961)Электроника-(8441)Электротехника-(4623)Энергетика-(12629)Юриспруденция-(1492)Ядерная техника-(1748)
Второе начало термодинамики
Второе начало термодинамики связано с направлением протекания тепловых процессов в системах без внешних воздействий.
По Р. Клаузиусу (1850 г.): невозможен процесс, единственным результатом которого является передача теплоты от холодного тела к горячему.
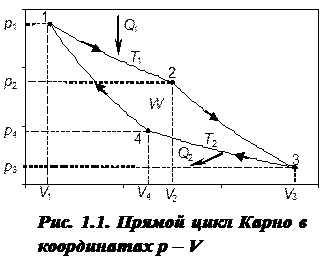 А по У. Томсону (1851 г.): невозможен процесс, единственным результатом которого является совершение работы за счет охлаждения одного тела.
А по У. Томсону (1851 г.): невозможен процесс, единственным результатом которого является совершение работы за счет охлаждения одного тела.
Закономерности превращения теплоты в работу и работы в теплоту можно получить на основе анализа работы тепловых машин. Теорию тепловых машин разработал С. Карно (1824 г.). В основу его тепловой машины был положен цикл, состоящий из двух изотерм и двух адиабат (рис. 1.1), носящий название «цикл Карно».
Термодинамический цикл – это совокупность термодинамических процессов, после совершения которых система возвращается в исходное состояние. При этом изменение внутренней энергии равно нулю, поэтому по первому началу термодинамики
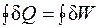 .
.
Но не следует понимать, что вся подведенная теплота превращается в работу. Часть теплоты отдается окружающей среде, то есть
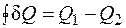 ,
,
где Q 1 – подведенная к системе теплота; Q 2 – теплота, переданная окружающей среде.
Коэффициент полезного действия (КПД) любого цикла определяется по формуле
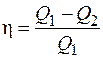 , (1.16)
, (1.16)
но тепловая машина, работающая по циклу Карно, имеет максимальный КПД, определяемый по формуле
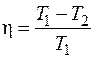 . (1.17)
. (1.17)
Поскольку Т 1 > Т 2, КПД цикла Карно всегда меньше единицы.
По формуле (1.17) рассчитывается КПД тепловой машины, работающей по циклу Карно и имеющей в качестве рабочего тела как идеальный газ, так и газ Ван-дер-Ваальса.
Температура Т 1 (теплоотдатчика) в цикле Карно больше температуры Т 2 (теплоприемника), поэтому тепловая машина, работающая по прямому циклу Карно, называется тепловым двигателем, то есть фактически превращает разность количеств теплоты 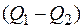 в эквивалентную работу W.
в эквивалентную работу W.
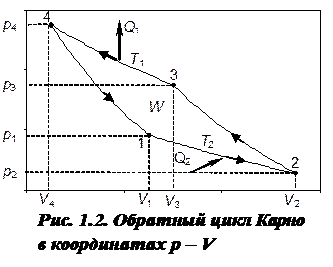 Если цикл Карно осуществляется в обратном направлении, то такая тепловая машина работает в качестве холодильника. При этом осуществляется охлаждение рабочего тела за счет совершения работы. На рис. 1.2 представлен обратный цикл Карно в координатах р, V. Изотермическое расширение из состояния 1 в состояние 2 осуществляется при температуре Т 2, а изотермическое сжатие – при более высокой температуре Т 1, поэтому теплота Q 1, отдаваемая теплообменнику:
Если цикл Карно осуществляется в обратном направлении, то такая тепловая машина работает в качестве холодильника. При этом осуществляется охлаждение рабочего тела за счет совершения работы. На рис. 1.2 представлен обратный цикл Карно в координатах р, V. Изотермическое расширение из состояния 1 в состояние 2 осуществляется при температуре Т 2, а изотермическое сжатие – при более высокой температуре Т 1, поэтому теплота Q 1, отдаваемая теплообменнику:
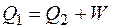 .
.
Таким образом, тепловая машина, работающая по обратному циклу Карно, называется холодильной машиной, если при этом Q 1 передается окружающей среде посредством теплообменника. Она характеризуется холодильным коэффициентом:
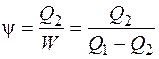 , (1.18)
, (1.18)
где Q 2 – теплота, полученная рабочим телом в процессе изотермического расширения из состояния 1 в состояние 2.
В принципе коэффициент y может быть больше или меньше единицы. Коэффициент y не следует путать с коэффициентом полезного действия h, который всегда меньше единицы.
Таким образом, процессы превращения теплоты в работу и работы в теплоту не являются равноценными. Работа может непосредственно пойти на увеличение любого вида энергии, например, механической, тепловой, электрической и т. д. Теплота в работу может быть превращена только в круговых процессах, в которых при протекании процесса в обратном направлении происходит передача части полученного тепла системой окружающим телам. Этот процесс передачи части полученного тепла холодильнику называют компенсацией. Устройство, которое могло бы без компенсации превращать теплоту в работу, исторически назвали вечным двигателем второго рода. Формулировка второго начала термодинамики: невозможен вечный двигатель второго рода.
Если процесс перехода системы из состояния 1 в состояние 2 и обратно осуществляется без каких-либо изменений в окружающих телах, то этот процесс называют обратимым. При этом внутренняя энергия системы не изменяется, т. к. она не зависит от пути протекания процесса, а только от начального и конечного состояний системы.
Если процесс обратного перехода системы из состояния 2 в состояние 1 без компенсации осуществить невозможно, то процесс перехода системы из состояния 1 в состояние 2 называют необратимым.
Большинство наблюдаемых термодинамических процессов в системах являются необратимыми. Действительно, это все механические процессы, в которых часть работы превращается в тепло, которое превратить в работу без дополнительной компенсации невозможно.
К необратимым процессам можно отнести также процессы теплопередачи (от горячего тела к холодному), диффузии газов, жидкостей, точечных дефектов кристаллических структур и т. д.
На основе анализа данных процессов второе начало термодинамики сформулировано как существование однозначной функции системы S, называемой энтропией, которая в изолированных системах при обратимых процессах не изменяется, а при необратимых возрастает. Для обратимого процесса математически второе начало термодинамики записывается следующим образом:
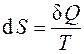 . (1.19)
. (1.19)
Если система не является изолированной, то для обратимого процесса
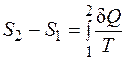 . (1.20)
. (1.20)
В адиабатно изолированной системе для обратимого процесса изменение энтропии равно нулю:
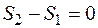 , (1.21)
, (1.21)
а для необратимого:
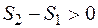 .
.
Для равновесного процесса из (1.19) следует:
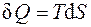 , (1.22)
, (1.22)
тогда основное уравнение термодинамики для равновесного процесса запишется:
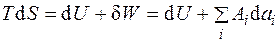 , (1.23)
, (1.23)
а для неравновесного:
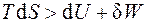 . (1.24)
. (1.24)
Статистическая физика раскрывает смысл энтропии как функции состояния, характеризующей вероятность состояния системы, то есть
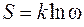 , (1.25)
, (1.25)
где 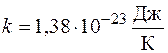 – постоянная Больцмана; w – термодинамическая вероятность, определяемая числом микросостояний, реализующих данное макросостояние.
– постоянная Больцмана; w – термодинамическая вероятность, определяемая числом микросостояний, реализующих данное макросостояние.
 Изменение энтропии системы носит односторонний характер, что связано с переходом системы из менее устойчивого состояния (менее вероятного) в более устойчивое (более вероятное), что сопровождается ростом ее энтропии. Энтропия системы вычисляется с точностью до постоянной, которая может быть определена с помощью третьего начала термодинамики.
Изменение энтропии системы носит односторонний характер, что связано с переходом системы из менее устойчивого состояния (менее вероятного) в более устойчивое (более вероятное), что сопровождается ростом ее энтропии. Энтропия системы вычисляется с точностью до постоянной, которая может быть определена с помощью третьего начала термодинамики.
В заключение параграфа отметим, что цикл Карно можно также изобразить в координатах T, S (рис. 1.3), где процессы 1–2 и 3–4 являются изотермическими, а 2–3 и 4–1 – адиабатными. Площадь цикла равна работе:
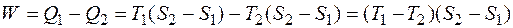 ,
,
где 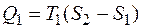 , а
, а 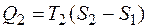 . Тогда КПД цикла Карно будет равен
. Тогда КПД цикла Карно будет равен
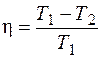 .
.
Следовательно, КПД цикла Карно не зависит от природы рабочего тела, а определяется температурой теплоотдатчика Т 1 и теплоприемника Т 2. Это первая теорема Карно.
Согласно второй теореме Карно КПД тепловой машины, работающей по необратимому циклу, всегда меньше КПД обратимой тепловой машины, то есть hнеобр < hобр.
Как эффективнее повысить КПД цикла? Очевидно, что либо путем повышения Т 1, либо – понижением Т 2. Но сравнивая производные:
 ,
, 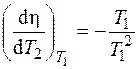 ,
,
можно заключить, что 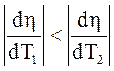 , т. к. Т 2 < Т 1. Следовательно, более эффективно повышать КПД можно путем понижения Т 2. Но следует заметить, что осуществить цикл при Т 2 = 0 К нельзя, это противоречит II началу термодинамики, поскольку при этом отсутствует компенсация, т. е. Q 2 = 0.
, т. к. Т 2 < Т 1. Следовательно, более эффективно повышать КПД можно путем понижения Т 2. Но следует заметить, что осуществить цикл при Т 2 = 0 К нельзя, это противоречит II началу термодинамики, поскольку при этом отсутствует компенсация, т. е. Q 2 = 0.
|
|
Дата добавления: 2015-05-26; Просмотров: 1324; Нарушение авторских прав?; Мы поможем в написании вашей работы!