
КАТЕГОРИИ:
Архитектура-(3434)Астрономия-(809)Биология-(7483)Биотехнологии-(1457)Военное дело-(14632)Высокие технологии-(1363)География-(913)Геология-(1438)Государство-(451)Демография-(1065)Дом-(47672)Журналистика и СМИ-(912)Изобретательство-(14524)Иностранные языки-(4268)Информатика-(17799)Искусство-(1338)История-(13644)Компьютеры-(11121)Косметика-(55)Кулинария-(373)Культура-(8427)Лингвистика-(374)Литература-(1642)Маркетинг-(23702)Математика-(16968)Машиностроение-(1700)Медицина-(12668)Менеджмент-(24684)Механика-(15423)Науковедение-(506)Образование-(11852)Охрана труда-(3308)Педагогика-(5571)Полиграфия-(1312)Политика-(7869)Право-(5454)Приборостроение-(1369)Программирование-(2801)Производство-(97182)Промышленность-(8706)Психология-(18388)Религия-(3217)Связь-(10668)Сельское хозяйство-(299)Социология-(6455)Спорт-(42831)Строительство-(4793)Торговля-(5050)Транспорт-(2929)Туризм-(1568)Физика-(3942)Философия-(17015)Финансы-(26596)Химия-(22929)Экология-(12095)Экономика-(9961)Электроника-(8441)Электротехника-(4623)Энергетика-(12629)Юриспруденция-(1492)Ядерная техника-(1748)
Гравиметрический анализ
|
|
|
|
Примеры решения задач
Пример 1. Вычислить фактор пересчета для определения калия, если после осаждения его в виде K2PtCl6 гравиметрической формой является Pt.
Решение. Из цепочки превращений
2K®K2PtCl6®Pt
следует, что 2 молям K соответствует 1 моль Pt. Фактор пересчета равен:
 .
.
Пример 2. Рассчитать массу силикатной породы, содержащей около 5% CaO, которая необходима для получения 0.3 г CaSO4.
Решение. Фактор пересчета
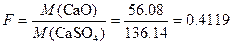 .
.
Масса m (CaO) в силикатной породе

Отсюда для массы силикатной породы имеем

Пример 3. Какой объем 2%-го раствора AgNO3 потребуется для осаждения хлорида из навески CaCl2×6H2O массой 0.4382 г?
Решение. Находим массу, необходимую для осаждения хлорид-ионов
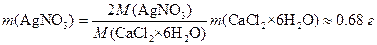
Объем раствора будет равен
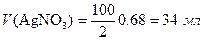 .
.
Пример 4. Из навески каменного угля массой 2.6248 г после соответствующей обработки получили 0.3248 г BaSO4. Вычислить массовую долю (%) серы в каменном угле. Пересчитать массовую долю (%) на сухое вещество, если содержание влаги в образце 2.58 %.
Решение. Фактор пересчета
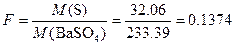 .
.
Масса серы в образце равна:
m (S)= F × m (BaSO4)=0.04462 г.
Содержание серы в образце
 .
.
В пересчете на сухое вещество
 .
.
Пример 5. При определении оксидов щелочных металлов из образца силикатной породы массой 1.2505 г выделили смесь NaCl и KCl массой 0.1500 г. После обработки этой смеси серной кислотой получили сульфаты Na2SO4 и K2SO4 массой 0.1800 г. Вычислить массовую долю (%) Na2O и K2O в силикатной породе.
Решение. Факторы пересчета Na2O и K2O в хлориды и сульфаты будут следующими:
 ,
, 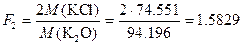
 ,
, 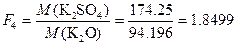
Массы хлоридов и сульфатов будут соответственно равны:
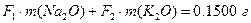 ,
,
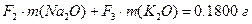 .
.
Решая полученную систему уравнений и деля найденные массы оксидов на массу образца, получаем: w (Na2O)=4.28%, w (K2O)=2.48%.
Пример 6. Вычислить потери (г и %) за счет растворимости осадка СаС2О4×H2O, если к 20 мл 0,1 М CaCl2 добавили: а) эквивалентное количество 0,1 М (NН4)2С2О4; б) полуторный избыток 0,1 М (NН4)2С2О4
|
|
|
Решение. а) Масса осадка СаС2О4×Н2О (М=146,12), образующегося при осаждении, равна
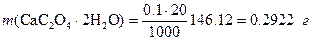 .
.
Объем раствора после добавления эквивалентного количества осадителя 20+20=40 мл; ПР (CaC2O4)=2.3×10–9. Отсюда 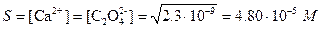 . Потеря оксалата кальция за счет растворимости составит
. Потеря оксалата кальция за счет растворимости составит
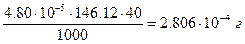
или

б) При использовании полуторного избытка осадителя масса осадка остается практически неизменной - 0,2922 г СаС2О4×Н2О. Объем раствора после осаждения равен 20+20×1,5=50 мл. При добавлении полуторного количества осадителя избыток его составляет 10 мл 0.1 М. Концентрация ионов С2О42– в полученном растворе будет составлять 0.1×10/50= 0.02 М. Поскольку в растворе находится избыток С2О42– растворимость СаС2О4 будет определяться концентрацией ионов кальция и
 или
или  , что составляет 2.9×10–4 %.
, что составляет 2.9×10–4 %.
Пример 7. Сколько процентов составят потери за счет растворимости при промывании 0,2 г осадка Мg(ОН)2 250 мл воды? Какова должна быть концентрация аммиака в промывной жидкости, чтобы потери промывании осадка таким же объемом составляли не более 0,1%?
Решение. На основании ПР=[Mg2+][OH-]2=6,0×10-19 определяем концентрацию Мg2+ и равную ей концентрацию Мg(ОН)2 в насыщенном растворе. Согласно уравнению реакции
Mg(OH)2ÛMg2++2OH-
|
|
|
|
|
Дата добавления: 2015-06-25; Просмотров: 5409; Нарушение авторских прав?; Мы поможем в написании вашей работы!