
КАТЕГОРИИ:
Архитектура-(3434)Астрономия-(809)Биология-(7483)Биотехнологии-(1457)Военное дело-(14632)Высокие технологии-(1363)География-(913)Геология-(1438)Государство-(451)Демография-(1065)Дом-(47672)Журналистика и СМИ-(912)Изобретательство-(14524)Иностранные языки-(4268)Информатика-(17799)Искусство-(1338)История-(13644)Компьютеры-(11121)Косметика-(55)Кулинария-(373)Культура-(8427)Лингвистика-(374)Литература-(1642)Маркетинг-(23702)Математика-(16968)Машиностроение-(1700)Медицина-(12668)Менеджмент-(24684)Механика-(15423)Науковедение-(506)Образование-(11852)Охрана труда-(3308)Педагогика-(5571)Полиграфия-(1312)Политика-(7869)Право-(5454)Приборостроение-(1369)Программирование-(2801)Производство-(97182)Промышленность-(8706)Психология-(18388)Религия-(3217)Связь-(10668)Сельское хозяйство-(299)Социология-(6455)Спорт-(42831)Строительство-(4793)Торговля-(5050)Транспорт-(2929)Туризм-(1568)Физика-(3942)Философия-(17015)Финансы-(26596)Химия-(22929)Экология-(12095)Экономика-(9961)Электроника-(8441)Электротехника-(4623)Энергетика-(12629)Юриспруденция-(1492)Ядерная техника-(1748)
Получение лимонной кислоты 3 страница
|
|
|
|
| Сухой продукт | Жидкий продукт | Сухой продукт | Жидкий продукт | Сухой продукт | Жидкий продукт |


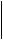


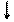








 Хранение
Хранение
 Применение
Применение
Рис. 3.1. Принципиальная биотехнологическая схема производства
продуктов микробного синтеза
3.2. Получение посевного материала
Поддержание чистой культуры штамма-продуцента - ключевая задача любого биотехнологического производства. Культуры микроорганизмов-продуцентов заводы получают из коллекций в пробирках на агаризованных питательных средах или в ампулах. Чистая культура микроорганизма может постоянно или по мере необходимости использоваться в производстве. При длительном хранении чистых культур могут происходить случайные нерегулируемые мутации. Для избежания мутаций следует не только соблюдать правила хранения и поддержания исходной культуры, но и периодически проводить пересев культуры и проверку ее однородности как по морфологическим, так и по физиологическим признакам.
Посевным материалом (инокулятом) называют чистую культуру микроорганизма, которую получают путем ее последовательного пересева из пробирки в колбу, а затем в аппараты увеличивающегося объема до количества, необходимого для промышленного производства. Сначала чистую культуру размножают в лаборатории, затем в цехе чистых культур и инокуляции, далее направляют на культивирование. Приготовление посевного материала состоит из следующих стадий:
1. Получение культуры микроорганизма в микробиологической лаборатории завода.
2. Выращивание микроорганизмов в малом посевном аппарате.
3. Выращивание микроорганизмов в большом посевном аппарате.
4. Накопление культуры микроорганизмов в малом ферментере.
|
|
|
Передачу чистых культур из одного аппарата в другой осуществляют в конце логарифмической фазы роста. Качество полученного посевного материала контролируют путем микроскопирования.
В биотехнологии широко применяются плесневые грибы, дрожжи, актиномицеты ( грамположительные бактерии, не образующие спор), бактерии и водоросли в виде чистых и смешанных культур. В традиционных процессах ферментации предпочтение обычно отдается смешанным культурам, а в большинстве современных ферментационных процессов – монокультурам (чистым культурам), выращиваемых в асептических условиях. Большинство используемых сегодня культур получено из природных источников, однако затем эти культуры были улучшены или путем выращивания в условиях, характерных для данного процесса (для повышения выхода биомассы и первичных метаболитов), или с помощью мутагенеза или генетической инженерии (для производства вторичных метаболитов).
3.3. Ферментация (культивирование)
Это самый важный и продолжительный этап биотехнологического производства. Ферментация представляет собой совокупность последовательных операций от внесения в заранее приготовленную и термостатированную питательную среду посевного материала до завершения процессов роста и биосинтеза вследствие исчерпывания питательных веществ среды. Существует два основных типа ферментаций: получение биомассы микроорганизмов и получение ценных веществ (метаболитов), возникающих в ходе роста или на последующих стадиях развития культуры.
Как говорилось ранее (п. 2.1), для выращивания любой культуры необходимы: жизнеспособный посевной материал; источники энергии и углерода; питательные вещества для синтеза биомассы; отсутствие ингибиторов роста; соответствующие физико-химические условия.
На оптимальной питательной среде при благоприятных значениях рН и температуры, при условии подачи требуемого количества воздуха в среду микроорганизмы быстро начинают расти и размножаться, обеспечивая накопление биомассы продуцента и биологически ценных метаболитов в культуральной жидкости. Способы ферментации мы рассматривали ранее в разделе 2.4.
|
|
|
Для культивирования микроорганизмов в промышленных масштабах применяют ферментеры (или ферментаторы) – реакционные емкости, в которых при определенных условиях находятся микроорганизмы. Основное назначение ферментатора – своевременно обеспечить микробные клетки необходимыми питательными веществами и кислородом (при необходимости) и отвести продукты обмена веществ, создать однородный состав среды при условии слабого потока культуральной жидкости (при непрерывном культивировании). Для поддержания кислородного режима ферментатор снабжается устройством подвода воздуха, для лучшего перемешивания среды – мешалками различной конструкции. Для поддержания температуры среды предусмотрены системы охлаждения.
3.4. Выделение целевого продукта
Стадия выделения продукта существенно зависит от того, накапливается продукт в клетках или он выделяется в культуральную жидкость, или же продуктом является сама клеточная масса. Разделение биомассы и культуральной жидкости - сепарация - осуществляется несколькими методами.
Если целевым продуктом является биомасса клеток, применяют следующие методы выделения: отстаивание, фильтрация, флотирование, сепарирование и т.д. (механические способы); выпаривание и сушка (физические способы).
Фильтрация – простой и широко применяемый процесс разделения твердых частиц и жидкости, скорость которого зависит от пористости фильтрующего материала и давления. Фильтрование при помощи вакуумных насосов существенно ускоряет процесс.
Флотирование применимо для выделения дрожжевых клеток. Процесс флотирования клеток осуществляется путем вспенивания культуральной жидкости. Вместе с пеной из культуральной жидкости удаляется и основная масса дрожжей.
Сепарирование осуществляют в сепараторах, в которых на клетки действует центробежная сила, отбрасывающая клетки к периферии сосуда, а культуральная жидкость будет собираться в центре сепаратора. Этот процесс протекает гораздо быстрее, чем отстаивание клеток под действием силы тяжести.
|
|
|
Если целевой продукт содержится в самих клетках, то проводят разрушение клеток - дезинтеграцию – физическими, химическими и ферментативными методами.
К физическим методам можно отнести разрушение клеток под действие ультразвука, замораживания-оттаивания, баллистическую дезинтеграцию. Баллистическая дезинтеграция клеток осуществляется в мельницах, куда помещают суспензию клеток и вспомогательные мелющие вещества: песок, стеклянные или полимерные шарики.
К химическим методам дезинтеграции относят разрушение клеток с помощью толуола, бутанола и других химических соединений.
При использовании ферментативной дезинтеграции клеток используют ферменты, способные разрушать определенные структурные компоненты клеточных стенок микроорганизмов. Например, для разрушения бактериальных клеток применяют лизоцимы яиц, бактерий, актиномицетов или грибов. Для разрушения дрожжей и плесневых грибов используются фосфоманназа и бета-глюконаза или применяют автолиз. Автолиз – разрушение клеток дрожжей или плесневых грибов под действием собственных гидролитических ферментов. Для этого суспензию клеток инкубируют при 35-45 ˚С.
Выделение продукта из культуральной жидкости или гомогената разрушенных клеток проводят путем его осаждения, экстракции, кристаллизации или сорбции.
Осаждение в виде нерастворимых солей производят путем добавления химического осадителя в эквимолярных количествах. Применяют при получении лимонной, молочной кислоты.
Экстракция – добавление к раствору экстрагента (растворителя), который поглощает целевой продукт. Затем эмульсию разделяют и выделяют целевое вещество. Используют при получении витаминов, антибиотиков.
Кристаллизация – после предварительной обработки культуральной жидкости и выпаривания при охлаждении осуществляют кристаллизацию. Данный метод выделения и очистки используется при получении глутаминовой, итаконовой и других кислот.
|
|
|
Затем выделенный продукт концентрируют центрифугированием, ультрафильтрацией, выпариванием или обратным осмосом.
Центрифугирование – расслоение раствора с частицами бόльшей плотности на осадок и надосадочную жидкость при воздействии центробежной силы.
Ультрафильтрация – обработка раствора на мембранных фильтрах с определенным размером пор (то есть разделение веществ на фракции по размерам их молекул). Применяется для ферментов и других белков.
3.5. Очистка целевого продукта
Эта стадия необходима при получении очищенного целевого продукта, например, ферментных препаратов степени очистки более двухкратной. Эта стадия приводит к росту себестоимости получаемого целевого продукта.
Для очистки ферментов применяют избирательную сорбцию (связывание) каолином, трифосфатом кальция, гидроксидом алюминия и другими адсорбентами. Таким образом проводят сорбцию либо фермента, либо балластных белков, которые затем разделяют центрифугированием. Фермент из сорбента отделяют раствором фосфатного буфера.
На последнем этапе продукт отделяют от примесей, концентрируют и стабилизируют. После стабилизации продукта в зависимости от того, каким должен быть конечный продукт: сухим или жидким, его обезвоживают или сразу упаковывают и отправляют на хранение и далее - потребителю.
Вопросы для самопроверки
1. Перечислите основные стадии биотехнологической схемы получения продуктов микробного синтеза.
2. Как определить физиологические потребности микроорганизмов в питательных веществах?
3. Какие методы применяют для обеззараживания питательных сред в биотехнологическом производстве?
4. Опишите последовательность получения посевного материала для промышленного производства целевого продукта.
5. Основное назначение ферментера.
6. От чего зависит проведение стадии выделения целевого продукта?
7. Какие методы применяют для отделения биомассы клеток от культуральной жидкости?
8. Что такое дезинтеграция, в каких случаях ее осуществляют?
9. Расскажите об основных методах дезинтеграции клеток.
10. В чем отличие сепарирования от центрифугирования?
11. В каких случаях выполняется стадия очистки целевого продукта?
12. Что такое сорбция?
ТЕМА 4. БИОТЕХНОЛОГИЧЕСКОЕ ПРОИЗВОДСТВО
ВЕЩЕСТВ И СОЕДИНЕНИЙ, ИСПОЛЬЗУЕМЫХ
В ПИЩЕВОЙ ПРОМЫШЛЕННОСТИ
Как говорилось ранее (п. 2.2), продуктами микробного брожения и метаболизма являются первичные метаболиты, вторичные метаболиты, ферменты и сама клеточная биомасса. Рассмотрим более подробно получение полезных для человека веществ с помощью биотехнологии.
4.1. Получение пищевых кислот с помощью микроорганизмов
Пищевыми принято называть 4 органические кислоты: лимонную, молочную, уксусную и винную. Иногда к ним причисляют яблочную и глутаминовую. Первые три пищевые кислоты получают с помощью микробного синтеза. Винную кислоту также можно получать этим способом, однако до сих пор эту органическую кислоту выгодно получать химическим путем из винного камня.
Получение органических кислот с помощью микроорганизмов началось в 20-30 гг. ХХ века. Пищевые кислоты до этого выделяли в ограниченном количестве из естественных источников. Лимонную кислоту – из сока лимонов, винную – из винного камня (отхода винодельческого производства).
Современное производство органических кислот, существующее в большинстве развитых стран, основано на использовании в качестве продуцентов различных штаммов плесневых грибов, чаще всего рода Aspergillus. С помощью микроорганизмов возможно получение более 50 различных органических кислот: лимонной, уксусной, итаконовой, глюконовой (аэробной ферментацией), молочной и пропионовой (анаэробным способом). Все органические кислоты являются промежуточными или конечными продуктами катаболизма углеводов. Основным механизмом регуляции их образования является лимитация роста продуцента факторами среды.
Лимонная кислота (С6Н8О7) - трехосновная оксикислота, широко распространена в природе, относительно много ее содержится в некоторых ягодах, фруктах, особенно в цитрусовых (в лимоне 5-10 %), в листьях и стеблях некоторых растений.
Ранее лимонную кислоту выделяли в виде лимоннокислого кальция из продуктов переработки листьев хлопчатника, стеблей махорки, хвои ели и в значительных количествах из плодов лимонов. Однако это производство является крайне дорогим и небольшим по объему. Поэтому лимонная кислота была дефицитным и дорогим продуктом.
В настоящее время лимонная кислота по объему производства является одним из главных продуктов микробного синтеза, ее общий выпуск в разных странах достигает до 400 тыс. тонн в год.
В начале нашего столетия рядом исследователей было замечено, что некоторые плесневые грибы обладают способностью образовывать заметные количества органических кислот. В дальнейшем путем отбора и направленной селекции были выделены активные продуценты органических кислот.
Для получения лимонной кислоты используют микроскопические грибы родов Aspergillus, Penicillium, Mucor, Ustina и др. В настоящее время основными продуцентами лимонной кислоты являются различные штаммы гриба Aspergillus niger, которые отличаются большой скоростью роста, легкостью культивирования и высоким выходом лимонной кислоты по отношению к массе окисляемого углевода. Они устойчивы к внешним воздействиям и имеют обильное конидиеношение. Споры грибов для получения лимонной кислоты хранят только в сухом виде.
Образование лимонной кислоты осуществляется в цикле трикарбоновых кислот в результате конденсации оксалоацетата и ацетил КоА при участии фермента цитрат-синтетазы (рис. 4.1.).
С6Н12О6
 Глюкоза
Глюкоза
 | |||||
 |  |
СН3 - СО - СООН СН3 - СО - СООН

 Пируват Пируват
Пируват Пируват
- СО2 + СО2
СН3 - СО - S - КоА + НООС - СН2 - СО - СООН

 Ацетил КоА Оксалоацетат
Ацетил КоА Оксалоацетат
 | |||
 |
 Н2С - СООН
Н2С - СООН
 НО - С - СООН
НО - С - СООН
Н2С - СООН
Лимонная кислота
Рис. 4.1. Схема синтеза лимонной кислоты
Необходимые для реакции оксалоацетат и ацетил КоА образуются из двух молекул пирувата: одна молекула пирувата подвергается декарбо-ксилированию с образованием ацетил КоА, вторая - карбоксилируется, давая оксалоацетат. Пируват образуется по фруктозо-бифосфатному пути (пути гликолиза, Эмбдена, Майергофа-Парнаса). Все ферменты этого пути, а также пируватдегидрогеназа, пируваткарбоксилаза и цитрат-синтетаза обнаружены у A. niger. В результате рассмотренной реакции одна молекула сахара (С6Н12О6) превращается в одну молекулу лимонной кислоты (С6Н8О7).
Сверхсинтез лимонной кислоты происходит при лимитировании роста грибов-продуцентов минеральными компонентами среды и одновременном избыточным содержанием источника углерода. В условиях лимитирования роста гриба недостатком железа и марганца после полного поглощения из среды дефицитного элемента он прекращает расти, однако продолжает потреблять имеющийся в среде источник углерода. При этом в клетках гриба начинает накапливаться лимонная кислота, которая в дальнейшем выделяется в среду.
Общая технологическая схема производства лимонной кислоты включает следующие этапы:
1. Подготовка питательной среды. Мелассу загружают в варочный котел, разбавляют водой до определенной концентрации углеводов (16 %), добавляют источники азота, фосфора и микроэлементы. Устанавливают необходимое значение рН среды (6,8-7,2) добавлением кислоты или щелочи. Для осаждения солей тяжелых металлов (железа, магния и т.д.), находящихся в мелассе, ее раствор обрабатывают желтой кровяной солью. Затем среду стерилизуют и охлаждают до температуры ферментации.
2. В отдельном цехе выращивают посевной материал в виде спор (конидий) Aspergillus niger. Затем размножают его в три стадии: в пробирках, колбах и алюминиевых кюветах. Длительность каждой стадии – 2-4 сут при 32 °С. Для выращивания в пробирках используют твердую агаризованную питательную среду, а в колбах и кюветах – жидкую.
3. Ферментация может осуществляться поверхностным или глубинным способом. Заводы небольшой или средней мощности используют поверхностный способ. Глубинный способ экономически выгоден тогда, когда мощность завода превышает 2500 т лимонной кислоты в год.
3.1. При поверхностном способе ферментация проводится на открытых металлических кислотоустойчивых кюветах высотой 7-20 см, в которых мицелий продуцента развивается на поверхности среды. Кюветы размещаются на многоярусных стеллажах в специальных камерах при температуре 34-36 °С. В камеры подают стерильный кондиционированный воздух. Цикл брожения заканчивается через 8-9 сут.
3.2. При глубинном способе мицелий гриба погружен в питательную среду в ферментаторах, туда же подается стерильный воздух. Длительность культивирования - 5-9 суток.
4. По окончании ферментации мицелий отделяют от культуральной жидкости. При глубинной ферментации - фильтрованием на фильтрах, при поверхностной – вручную, предварительно слив жидкость с кювет.
5. Мицелий промывают, высушивают и направляют для использования в качестве добавки к животным кормам. Фильтрованная культуральная жидкость (фильтрат) представляет собой водный раствор лимонной кислоты. В 1 литре фильтрата содержится 40-50 г лимонной кислоты.
6. Лимонную кислоту выделяют из культуральной жидкости в виде плохо растворимой соли – цитрата кальция, которая образуется при добавлении мела. Перевод лимонной кислоты в свободное состояние достигается при добавлении строго определенного количества Н2SO4:
 Цитрат кальция + Н2SO4 Цитрат + Гипс
Цитрат кальция + Н2SO4 Цитрат + Гипс
Гипс удаляют фильтрованием. Раствор лимонной кислоты осветляют активным углем, упаривают, сливают в кристаллизаторы, в которых постепенно снижают температуру. Выделившиеся кристаллы центрифугируют, промывают водой, сушат, фасуют.
Лимонная кислота используется в кондитерской промышленности для подкисления карамели, пастилы, вафель, так как она хорошо подчеркивает фруктовый вкус. Данную органическую кислоту в целях подкисления добавляют в мороженое, пищевые концентраты, маргарин, некоторые сорта колбас и сыра.
Лимонную кислоту применяют для торможения образования меланоидинов в сгущенном молоке с сахаром, раствором ее промывают и дезодорируют жировое сырье, обрабатывают перед холодным хранением свежее мясо, рыбу, фрукты с целью стабилизации их цвета, вкуса и запаха. Соли лимонной кислоты используют для изготовления шампуней и других моющих средств, так как они стимулируют вспенивание и обеспечивают механическую устойчивость пен.
Получение молочной кислоты
Молочная кислота с 1881 г. производится промышленным способом с помощью молочнокислых бактерий. В СССР было организовано производство молочной кислоты в 1923 г. Для промышленного изготовления молочной кислоты пригодны только гомоферментативные молочнокислые бактерии, образующие до 98 % молочной кислоты. Применяемые штаммы Lactobacillus delbrueckii (дельбрюкки), L. bulgaricus не предъявляют высоких требований к питательной среде и за короткое время дают высокий выход молочной кислоты.
Молочнокислые бактерии преобразуют в молочную кислоту самые разные углеводы, поэтому для промышленного получения этой кислоты используют мелассу, молочную сыворотку, глюкозу, мальтозу, сахарозу, лактозу, осахаренный крахмал и пр. В каждом случае подбирают наиболее подходящий продуцент. Для сбраживания глюкозы или мальтозы обычно применяют штаммы Lactobacillus delbrueckii, L. leichmannii или L. bulgaricus. Для сбраживания осахаренного крахмала используют смесь молочнокислых бактерий L. delbrueckii или с L. bulgaricus, или со Streptococcus lactis. При сбраживании мальтозы выход молочной кислоты выше при использовании L. bulgaricus или L. casei.
В качестве основного сырья используют мелассу, картофельный осахаренный затор, которые разбавляют водой до определенной концентрации (12 %), вносят дополнительные источники аминного азота (свободные аминокислоты), витаминов и других биологически активных веществ в виде кукурузного или дрожжевого экстракта, или вытяжку солодовых ростков (так как на молочнокислое брожение биологически активные вещества оказывают положительное влияние).
Молочную кислоту в промышленных условиях получают методом анаэробной глубинной ферментации. Концентрация сахара в среде должна быть 5-20 %, температура 44-50 оС, рН 6,3-6,5. Во время ферментации рН среды поддерживают, добавляя мел. Через 6-7 суток культивирования в среде остается 0,5-0,1 % сахаров и 11-14 % лактата кальция. Из 100 г сахаров получают 80-90 г лактата. Осадок мела и коллоиды отделяют фильтрацией. Фильтрат упаривают до концентрации 27-30 %, затем охлаждают до 25-30 оС и выдерживают в кристаллизаторах 36-48 ч. Кристаллы лактата отделяют центрифугированием. Молочную кислоту из лактата получают при помощи серной кислоты. Реакция идет при 60-70 оС в соответствии с уравнением:
 Ca (C3H5O3)2 + H2SO4 CaSO4 + 2C3H6O3
Ca (C3H5O3)2 + H2SO4 CaSO4 + 2C3H6O3
Для отделения ионов железа молочную кислоту (сырец) при температуре 65 оС обрабатывают желтой кровяной солью. Тяжелые металлы осаждают сульфатом натрия. Молочную кислоту обрабатывают активированным углем, фильтруют и фасуют. Конечный продукт - в виде жидкого концентрата молочной кислоты.
Молочную кислоту применяют для приготовления джемов, в которых она способствует хорошей консистенции. Молочная кислота как регулятор рН, улучшитель вкуса применяется в производстве многих сыров, квашении капусты, в сухом концентрате кваса. В хлебобулочном производстве молочная кислота и лактаты увеличивают объем мякиша и улучшают корку хлеба при использовании муки низкого качества. Способность лактатов удерживать влагу применяют в производстве колбас, сыров, детского питания. Молочную кислоту также используют для ускорения получения молочно-белкового сгустка при производстве творога.
Получение уксусной кислоты
Продуцентами уксусной кислоты являются уксуснокислые бактерии рода Acetobacter. Эти бактерии приспособлены к сахаристым и спиртовым субстратам, растут при сильно кислых условиях (рН = 4,0). К быстроокисляющим бактериям относят высокопроизводственный штамм Acetobacter curvum (курвум). Недостатком этого продуцента является то, что он может терять свойство образовывать уксусную кислоту, поэтому его постоянно поддерживают в среде с высокой концентрацией спирта и уксусной кислоты и низкой концентрацией питательных веществ.
В качестве сырья для получения пищевого уксуса используют виноградное вино, пивное сусло, мед, соки различных фруктов и ягод после спиртового брожения или водный раствор этилового спирта для получения белого уксуса. Кроме спирта среда содержит уксусную кислоту и минеральные соли N, P, S, Mn, K. Иногда добавляют источники витаминов в виде различных экстрактов. Уксусная кислота служит источником углерода и энергии для бактерий.
Уксусная кислота стала первым микробиологическим продуктом, полученным с помощью иммобилизованных клеток. Этот способ может быть непрерывным и периодическим. В течение длительного времени применяется адсорбирование уксуснокислых бактерий на древесной стружке, древесном угле, коксе и других субстратах. Пропуская раствор этанола через генераторы с иммобилизованными бактериями, получают 10-15 %-ный раствор уксусной кислоты. Из 100 л безводного спирта теоретически должно быть получено 103 л уксусной кислоты. На практике выход уксуса из 100 л этанола редко превышает 90 л, что связано с переокислением и неполным окислением этанола бактериями, а также с его испарением.
В столовом уксусе содержится 5-9 % уксусной кислоты. Уксус с концентрацией кислоты 20-30 % получают путем вымораживания исходного раствора. Путем перегонки получают 70-80 %-ную уксусную кислоту, называемую уксусной эссенцией. Ледяная уксусная кислота содержит 98,0-99,8 % кислоты.
Уксус, полученный при брожении, имеет приятные аромат и вкус, которые обусловливают побочные продукты брожения: сложные эфиры (этилацетат и другие), высшие спирты, органические кислоты.
Уксусную кислоту или уксус широко используют в пищевой промышленности. Уксус, полученный микробиологическим путем (пищевая уксусная кислота, столовый уксус), различается по сортам в зависимости от характера сбраживаемого субстрата. Известен яблочный, виноградный, грушевый и другие сорта уксуса.
Уксус также применяют для растворения органических красителей, при получении медикаментов, пластмасс и т.д.
4.2. Получение и использование аминокислот
Существует несколько способов получения аминокислот. При производстве аминокислот могут быть использованы отходы мясоперерабатывающей промышленности (отходы обработки животного сырья, кровь и т.д.), яичный белок, казеин молока, клейковина пшеницы, соевый шрот и т.д. При переработке этого сырья все аминокислоты переходят в гидролизат, и для выделения отдельных аминокислот необходима сложная многостадийная очистка. Кроме того, само сырье считается дефицитным и дорогим, поэтому аминокислоты имеют высокую себестоимость.
Химический синтез аминокислот достаточно эффективен, однако его недостатком является то, что в процессе синтеза образуется смесь из биологически активной L-формы и D-изомера аминокислоты. D-форма является балластом, так как не усваивается животными и человеком, а некоторые D-формы аминокислот обладают токсическими свойствами. Разделение изомеров – дорогая и трудоемкая процедура. Синтетически производится незаменимая аминокислота метионин.
В настоящее время большую часть аминокислот производят с помощью микробного синтеза, причем микроорганизмы синтезируют только L-форму. Это значительно облегчает выделение и очистку аминокислот и позволяет получать препараты с низкой себестоимостью. Микроорганизмы, образующие аминокислоты, не накапливают их в клетке, а постоянно выделяют в питательную среду. Поэтому аминокислоты выделяют из фильтрата культуральной жидкости.
Глутаминовая кислота – первая аминокислота, полученная микробным синтезом. Глутаминовая кислота относится к заменимым кислотам, обладает приятными органолептическими свойствами и находит самое широкое применение. Ее продуцентами являются бактерии, относящиеся к различным родам. В промышленном производстве используют бактерии Corinebacterium glutamicum и Brevibacterium flavum и др. Условия сверхсинтеза глутамата натрия следующие. Когда Corinebacterium glutamicum растет в среде с меньшей, чем оптимальная, концентрацей биотина (витамина Н), нарушается синтез мембранных фосфолипидов, в результате чего глутамат натрия проходит через мембрану и накапливается в культуральной жидкости. То же самое происходит при добавлении в питательную среду пенициллина: этот антибиотик подавляет синтез клеточной стенки и тем самым способствует выделению аминокислоты.
|
|
|
|
|
Дата добавления: 2015-06-26; Просмотров: 550; Нарушение авторских прав?; Мы поможем в написании вашей работы!