
КАТЕГОРИИ:
Архитектура-(3434)Астрономия-(809)Биология-(7483)Биотехнологии-(1457)Военное дело-(14632)Высокие технологии-(1363)География-(913)Геология-(1438)Государство-(451)Демография-(1065)Дом-(47672)Журналистика и СМИ-(912)Изобретательство-(14524)Иностранные языки-(4268)Информатика-(17799)Искусство-(1338)История-(13644)Компьютеры-(11121)Косметика-(55)Кулинария-(373)Культура-(8427)Лингвистика-(374)Литература-(1642)Маркетинг-(23702)Математика-(16968)Машиностроение-(1700)Медицина-(12668)Менеджмент-(24684)Механика-(15423)Науковедение-(506)Образование-(11852)Охрана труда-(3308)Педагогика-(5571)Полиграфия-(1312)Политика-(7869)Право-(5454)Приборостроение-(1369)Программирование-(2801)Производство-(97182)Промышленность-(8706)Психология-(18388)Религия-(3217)Связь-(10668)Сельское хозяйство-(299)Социология-(6455)Спорт-(42831)Строительство-(4793)Торговля-(5050)Транспорт-(2929)Туризм-(1568)Физика-(3942)Философия-(17015)Финансы-(26596)Химия-(22929)Экология-(12095)Экономика-(9961)Электроника-(8441)Электротехника-(4623)Энергетика-(12629)Юриспруденция-(1492)Ядерная техника-(1748)
Ішемія мозку та енергетичний дефіцит олігодендроцитів
|
|
|
|
Різні форми церебральної ішемії корелюють з фазними змінами вмісту ATФ та ключових енергозалежних процесів в клітинах олігодендроглії [45]. Лише на останніх етапах кисневого голодування рівень енергетичного дефіциту стає достатнім для запуску основних механізмів, що призводять до порушення життєдіяльності та загибели клітин. Стрімке збільшення концентрації аденозинмонофосфату (AMФ) супроводжується активацією протеїнкіназної системи, яка є додатковим механізмом руйнування клітинних мембран, особливо мієліну. Найбільш повно пошкоджується зона юкстапаранодального сегменту [46].
В олігодендроцитах гліколіз не запобігає зниженню рівня АТФ на пізніх стадіях кисневого голодування. Однак існує велика кількість експериментальних даних, що вказують на те, що збільшення утилізації глюкози олігодендроглією та астроцитами внаслідок глутаматіндукованої активації Na+/K+-ATФази призводить до її метаболізації за гліколітичним шляхом до лактату, який, вивільняючись, трансформується нейронами в піруват і використовується як адекватний енергетичний субстрат, Експериментальні дослідження на моделях гострої церебральної ішемії виявили різну ступінь зменшення концентрації креатинфосфату, АТФ і аденозиндифосфату (АДФ) в тканині мозку поряд зі збільшенням вмісту неорганічного фосфату і лактату [47, 48].
Встановлено, що протягом декількох хвилин після початку гострої фокальної церебральної ішемії розвивається дефіцит макроергічних сполук (ATФ, креатинфосфату) в олігодендроглії мозку. У тварин з меншою чутливістю до гіпоксії достовірно знижується лише вміст ATФ і AДФ, тоді як рівень креатинфосфату короткочасно змінюється в перші хвилини ішемії і швидко відновлюється до норми. Градієнт падіння рівня ATФ в мозку низькорезистентних до гіпоксії тварин при малих значеннях парціального тиску кисню виражений набагато сильніше, ніж у мозку резистентних до гіпоксії тварин [48].
|
|
|
Особливості енергетичних змін у тканині мозку залежать й від локалізації ішемічного процесу. У більшості областей мозку реперфузія супроводжується повним або частковим поверненням енергетичного метаболізму до нормальних показників: збільшуються концентрації ATФ та креатинфосфату, знижується рівень лактату. У той же час в селективно чутливих до ішемії олігодендроцитах і нейронах (CA1 зона гіпокампу, дорсолатеральній відділ стріатуму) зміни енергетичного метаболізму мають двофазний характер: слідом за короткочасною нормалізацією відзначається його вторинне гальмування [49].
Розвиток "постішемічної гіпоксії" призводить до значного порушення структурно-функціонального статусу мітохондрій, зменшення продукції нікотинамідаденіндинуклеотидфосфату (НAДФ) в синаптосомах, що здійснює додатковий вплив на процеси незворотного пошкодження тканини мозку [48].
Вивчення кореляційних зв'язків між параметрами ядерної магнітно-резонансної спектроскопії ішемізованої тканини мозку, що відображають різні ланки енергетичного метаболізму, виявило достовірно вищий рівень сумарної сили зв'язку при більш низьких значеннях дисперсії елементів кореляційної матриці. Це дозволяє зробити висновок про більш жорстку організацію енергетичної системи в умовах навіть помірно вираженою ішемії мозку. Неадекватна впорядкованість енергетичної системи, можливо, є компенсаторною на початкових стадіях ішемії. Однак, за теорією "хаосу", більш впорядковані системи менш стійкі, а в певних умовах і більш уразливі. У зв'язку з цим при довготривалій ішемії менша пластичність енергетичної системи стає одним з факторів, що сприяють формуванню інфаркту мозку і детермінують можливість виживання нейронів [48, 50].
|
|
|
Олігодендроцити та нейрони, які мають високу схильність до хронічної ішемії (мозковий кровотік менше 10-15 мл / 100 г за 1 хв), характеризуються підвищеною вразливістю до порушень енергетичного метаболізму, оскільки не здатні підтримувати іонний градієнт мембран за рахунок "знеструмлення" Na+/K+-ATФaзної ферментної системи. Швидкість розвитку аноксичної деполяризації мембран нейронів залежить від глибини і тривалості ішемії і веде до некротичної смерті клітини. Ймовірно, енергетичний дефіцит є чільним механізмом загибелі нейронів в області центрального інфаркту (ядерній зоні ішемії) [48].
У зоні пенумбри (напівтіні, яка оточує зону інфаркту) більш "м'яка" ішемія ініціює розвиток комплексу біохімічних перетворень, підтримуваних реакцією геному і молекулярними наслідками ішемічного процесу: включенням генів раннього реагування з вторинною експресією генів, що кодують цитокіни, молекули адгезії, інші прозапальні і трофічні фактори, а також гени апоптозу. В олігодендроцитах зростає експресія транскрипційного фактору NF-κB, проте зменшується експресія Olig-2 (рис. 2. 10), необхідного для мієлінізації аксонів. Проте це явище є зворотним, оскільки при реперфузії та відновленні парціального тиску кисню рівень Olig-2 знову зростає [48]. Доведено, що білковий фактор нейрегулін 1β підвищує резистентність клітинних попередників олігодендроцитів, впливаючи на експресію Olig-2 [49].
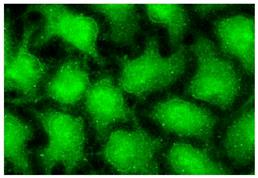
Рис. 2. 10. Скупчення олігодендроцитів, які продукують фактор Olig-2 (виявлений за допомогою специфічних моноклональних антитіл з імунофлуоресцентною міткою)
Енергетичний дефіцит і лактатацидоз є тригерами каскаду патобіохімічних реакцій, що протікають у всіх основних клітинних пулах ЦНС і призводять до формування інфаркту мозку за двома основними механізмами: некрозу та апоптозу [48].
|
|
|
|
|
Дата добавления: 2015-06-27; Просмотров: 366; Нарушение авторских прав?; Мы поможем в написании вашей работы!