
КАТЕГОРИИ:
Архитектура-(3434)Астрономия-(809)Биология-(7483)Биотехнологии-(1457)Военное дело-(14632)Высокие технологии-(1363)География-(913)Геология-(1438)Государство-(451)Демография-(1065)Дом-(47672)Журналистика и СМИ-(912)Изобретательство-(14524)Иностранные языки-(4268)Информатика-(17799)Искусство-(1338)История-(13644)Компьютеры-(11121)Косметика-(55)Кулинария-(373)Культура-(8427)Лингвистика-(374)Литература-(1642)Маркетинг-(23702)Математика-(16968)Машиностроение-(1700)Медицина-(12668)Менеджмент-(24684)Механика-(15423)Науковедение-(506)Образование-(11852)Охрана труда-(3308)Педагогика-(5571)Полиграфия-(1312)Политика-(7869)Право-(5454)Приборостроение-(1369)Программирование-(2801)Производство-(97182)Промышленность-(8706)Психология-(18388)Религия-(3217)Связь-(10668)Сельское хозяйство-(299)Социология-(6455)Спорт-(42831)Строительство-(4793)Торговля-(5050)Транспорт-(2929)Туризм-(1568)Физика-(3942)Философия-(17015)Финансы-(26596)Химия-(22929)Экология-(12095)Экономика-(9961)Электроника-(8441)Электротехника-(4623)Энергетика-(12629)Юриспруденция-(1492)Ядерная техника-(1748)
Материальный баланс приготовления магнезиальной добавки с использованием магнезита
|
|
|
|
Расчеты материальных балансов
Расчеты химико-технологических процессов
Очистка отработанного воздуха, выбрасываемого в атмосферу
Загрязнённый примесями аммиачной селитры и аммиака воздух из грануляционной башни и промывателя паровоздушной смеси, а также соковый пар из аппаратов ИТН и скруббера поступают на очистку в промывной скруббер.
Скруббер выполнен в виде двух блоков, расположенных вдоль длинных сторон башни в верхней её части. В каждом блоке имеется по три параллельно работающие секции. Каждая секция имеет две ситчатые тарелки с отбойными элементами, над верхней тарелкой размещены четыре фильтрующих элемента.
Отработанный воздух и соковый пар поступает под промывные тарелки. На верхнюю тарелку каждой секции скруббера насосом из бака непрерывно подаётся закисленный раствор с массовой долей амселитры не более 25% и массовой концентрацией азотной кислоты не более 20 г/дм3. Закисление раствора необходимо для улавливания аммиака, содержащегося в воздухе [8].
Промывной раствор, пройдя тарелки скруббера, возвращается в бак, откуда насосом вновь подаётся в скруббер.
Массовая доля амселитры в растворе поддерживается за счёт непрерывного поступления в бак слабого раствора с 3-их тарелок аппаратов ИТН. Сюда же поступает также раствор из промывателя.
Часть циркулирующего раствора амселитры непрерывно отводится из напорной линии насоса в аппараты ИТН на переработку. Уровень в баке регулируется автоматически клапаном подачей в бак конденсата сокового пара от напорной линии насосов. Кислотность раствора в баке (рН не менее 1,1) поддерживается подачей азотной кислоты в скруббер.
Воздух после очистки на тарелках скруббера проходит фильтрующие элементы, со средней массовой концентрацией амселитры не более 0,10 г/м3 и аммиака не более 0,05 г/м3 выбрасывается в атмосферу на высоте 73 м вентиляторами, установленными по одному на каждую секцию скруббера. Одновременно вентиляторы служат для создания в гранбашне потока воздуха, охлаждающего гранулы амселитры.
|
|
|
Температура воздуха на выходе в каждый блок скруббера (50-90 °С) и на выходе из каждой секции (30-70°С) контролируется в ЦПУ [8].
Исходные данные:
Состав каустического магнезита:
MgO - 83%
CaO – 2,5%
SiO2 – 2,5%
Fe2O3 – 1,1%
Al2O3 – 1,1%
SO42- - 1%
C – 0,2%
H2O – 1,5%
Прочее – 8,09%
Производительность предприятия – 450 000 т/год
1. В процесс вводиться 3% магнезиальной добавки, то есть:
4,5·108 кг/год – 100%
х т/год - 3%
х = 1,35·104 кг/год
2. Определим количество MgO в 1,35·104 кг Mg(NO3)2:
х кг/год 1,35·104 кг/год
MgO + 2HNO3 = Mg(NO3)2 + H2O
40,3 кг/моль 148 кг/год
х = 3,67·103 кг/год
3. Определим количество MgOтех. :
1,35·104 кг Mg(NO3)2 - 3,67·103 кг/год
4,5·108 кг/год - х кг/год MgOтех.
х = 1,22·108 кг/год
4. Определим количество MgO с учетом, что его содержание составляет 83% от 100% сырья:
1,22·108 кг/год MgOтех. – 100%
х кг/год - 83%
х = 1,01·108 кг/год чистого MgO
5. Определим количество CaO в сырье :
1,22·108 кг/год MgOтех. – 100%
х кг/год - 2,5%
х = 3,05·106 кг/год чистого CaO
6. Определим количество SiO2 в сырье:
1,22·108 кг/год MgOтех. – 100%
х кг/год - 2,5%
х = 3,05·106 кг/год чистого SiO2
7. Определим количество Fe2O3 в сырье:
1,22·108 кг/год MgOтех. – 100%
х кг/год - 1,1%
х = 1,34·106 кг/год чистого Fe2O3
8. Определим количество Al2O3 в сырье:
1,22·108 кг/год MgOтех. – 100%
х кг/год - 1,1%
х = 1,34·106 кг/год чистого Al2O3
9. Определим количество SO42- в сырье:
1,22·108 кг/год MgOтех. – 100%
х кг/год - 1%
х = 1,22·106 кг/год чистого SO42-
10. Определим количество C в сырье:
1,22·108 кг/год MgOтех. – 100%
х кг/год - 0,2%
х = 2,44·105 кг/год чистого C
11. Определим количество H2O в сырье:
1,22·108 кг/год MgOтех. – 100%
х кг/год - 1,5%
х = 1,83·106 кг/год чистого H2O
12. Определим количество прочих примесей в сырье:
|
|
|
1,22·108 кг/год MgOтех. – 100%
х кг/год - 8,09%
х = 9,86·106 кг/год примесей
13. Определим количество азотной кислоты, которое взаимодействует с MgO по реакции:
1,01·108 кг/год A1
MgO + 2HNO3 = Mg(NO3)2 + H2O
40,3кг/моль 2·63кг/моль
А1 = 3,15·108 кг/год
14. Определим количество серной кислоты, которое взаимодействует с CaO по реакции:
3,05·106 кг/год A2
CaO + 2HNO3 = Ca(NO3)2 + H2O
56кг/моль 2·63кг/моль
А2 = 6,86·106 кг/год
15. Определим общее количество серной кислоты, которое участвует в процессе:
А = А1+А2
А = 3,15·108 + 6,86·106 = 3,22·108 кг/год
16. Определим количество 57%-ой азотной кислоты, участвующей в реакции по формуле (4.4.1):
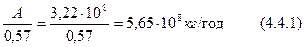
17. Определим количество 36%-ой азотной кислоты, участвующей в реакции:
57% HNO3 – х кг/год
36% HNO3 – 5,65·108 кг/год
х = 8,94·108 кг/год
18. Определим количество воды, необходимое для разбавления 57%-ой азотной кислоты, до ее концентрации 36%:
8,94·108 – 5,65·108 = 3,29·108 кг/год
19. Определим количество воды, необходимое для разбавления 100%-ой азотной кислоты, до ее концентрации 57%:
5,65·108 – 3,22·108 = 2,43·108 кг/год
Получаем, что в реакции участвует следующее количество азотной кислоты:
HNO3 (57%) = 5,65·108 кг/год
HNO3 (36%) = 8,94·108 кг/год
HNO3 (100%) = 3,22·108 кг/год
20. Определим количество Mg(NO3)2, образующееся в результате взаимодействия MgO c HNO3:
1,01·108 кг/год x кг/год
MgO + 2HNO3 = Mg(NO3)2 + H2O
40,3кг/моль 148кг/моль
А1 = 3,7·108 кг/год
21. Определим количество Са(NO3)2, образующееся в результате взаимодействия СаO c HNO3:
3,05·106 кг/год х кг/год
CaO + 2HNO3 = Ca(NO3)2 + H2O
56кг/моль 164кг/моль
А2 = 8,93·106 кг/год
22. Так как массовая доля Mg(NO3)2 составляет 37%, определим количество воды, необходимое для приготовления магнезиальной добавки:

(3,7·108 + х)·0,37 = 3,7·108
1,37·108 + 0,37х = 3,7·108
0,37х = 2,33·108
х = 6,29·108 кг/год
23. Конденсат сокового пара, подающийся в реактор, содержит в своем составе 5,17·107 кг воды.
Таким образом, общее количество воды, необходимое для приготовления магнезиальной добавки, составит:
В = 1,83·106 + 2,43·108 + 3,29·108 + 5,17·107 + 6,29·108 = 1,25·109 кг/год
24. Так как в конденсат сокового пара входит азотная кислота, общее количество азотной кислоты составит:
3,22·108 – 2,05·105 = 3,21·108 кг/год HNO3
Сводим материальный баланс процесса приготовления магнезиальной добавки.
Таблица 4.4.1.1
| Приход | Расход | ||||||||
| Статья | кг/год | кг/ч | % мас. | моль/ч | Статья | кг/год | кг/ч | % мас. | моль/ч |
| 1)Магнезит, в т.ч. MgO CaO SiO2 Fe2O3 Al2O3 SO4 C H2O Прочее | 1,23·108 1,01·108 3,05·106 3,05·106 1,34·106 1,34·106 1,22·106 2,44·105 1,83·106 9,86·106 | 15530,3 12752,5 385,1 385,1 169,2 169,2 154,0 30,8 234,8 1244,9 | 2,5 2,5 1,1 1,1 1,0 0,2 1,5 8,09 | 316,4 6,87 6,42 1,06 1,66 1,6 2,56 13,04 | 1)Раствор Mg(NO3)2, в т.ч. Mg(NO3)2 Ca(NO3)2 SiO2 Fe2O3 Al2O3 SO4 C H2O Прочее | 1,64·109 3,7·108 8,93·106 3,05·106 1,34·106 1,34·106 1,22·106 2,44·105 1,25·109 9,86·106 | 2,07·105 46717,2 1127,52 385,1 169,2 169,2 154,0 30,8 1,57·105 1244,9 | 22,5 0,5 0,2 0,08 0,08 0,07 0,01 76,2 0,6 | 315,6 6,87 6,42 1,06 1,66 1,6 2,56 8722,2 |
| 2)Азотная кислота(36%), в.т.ч. HNO3(100%) H2O(100%) HNO3(57%) H2O(57%) | 1,44·109 3,21·108 3,29·108 5,65·108 2,43·108 | 181818,2 40530,3 41540,4 71338,4 30681,2 | 22,3 22,85 39,24 15,61 | 5787,9 643,3 2307,8 1132,3 1704,5 | |||||
| 3) КСП, в т.ч. H2O NH4NO3 HNO3 | 5,22·107 5,17·107 2,05·105 2,05·105 | 6590,9 6527,7 26,0 26,0 | 99,0 0,5 0,5 | 363,33 362,6 0,32 0,41 | |||||
| Всего | 1,64·109 | 2,07·105 | 1,64·109 | 2,07·105 |
|
|
|
|
|
|
|
|
Дата добавления: 2015-06-28; Просмотров: 1336; Нарушение авторских прав?; Мы поможем в написании вашей работы!