
КАТЕГОРИИ:
Архитектура-(3434)Астрономия-(809)Биология-(7483)Биотехнологии-(1457)Военное дело-(14632)Высокие технологии-(1363)География-(913)Геология-(1438)Государство-(451)Демография-(1065)Дом-(47672)Журналистика и СМИ-(912)Изобретательство-(14524)Иностранные языки-(4268)Информатика-(17799)Искусство-(1338)История-(13644)Компьютеры-(11121)Косметика-(55)Кулинария-(373)Культура-(8427)Лингвистика-(374)Литература-(1642)Маркетинг-(23702)Математика-(16968)Машиностроение-(1700)Медицина-(12668)Менеджмент-(24684)Механика-(15423)Науковедение-(506)Образование-(11852)Охрана труда-(3308)Педагогика-(5571)Полиграфия-(1312)Политика-(7869)Право-(5454)Приборостроение-(1369)Программирование-(2801)Производство-(97182)Промышленность-(8706)Психология-(18388)Религия-(3217)Связь-(10668)Сельское хозяйство-(299)Социология-(6455)Спорт-(42831)Строительство-(4793)Торговля-(5050)Транспорт-(2929)Туризм-(1568)Физика-(3942)Философия-(17015)Финансы-(26596)Химия-(22929)Экология-(12095)Экономика-(9961)Электроника-(8441)Электротехника-(4623)Энергетика-(12629)Юриспруденция-(1492)Ядерная техника-(1748)
Общая характеристика белков
ЛЕКЦИЯ 2.1.
ТЕМА: ХАРАКТЕРИСТИКА БЕЛКОВ КАК КОМПОНЕНТОВ СЫРЬЯ ДЛЯ ПРОИЗВОДСТВА ПРОДУКЦИИ СОБСТВЕННОГО ПРОИЗВОДСТВА ПРХ.
1. Общая характеристика белков.
2. Изменение белков в технологическом процессе.
3. Белки мяса.
4. Белки молока.
5. Белки яиц.
6. Белки зернобобовых.
Литература
1.Гницевич В.А. Теоретические основы пищевых технологий. Раздел: Изменение составных частей пищевых продуктов в процессе тепловой обработки: Уч.пос.-Д.:ДГУЭТ,2002.-136с.
2. Баранов В.С. Технология производства продукции общественного питания: Уч./В.С. Баранов, А.И. Мглинец, Л.М. Алешина.-М.:Экономика,1986.-400с.
Белки – это высокомолекулярные органические соединения, являющиеся сополимерами аминокислот. В природе существует примерно от 1010 до 1012 различных белков, составляющих основу всех видов живых организмов. Огромное многообразие белков обусловлено способностью 20 α-аминокислот взаимодействовать друг с другом с образованием полимерных соединений с молекулярной массой от 6 тысяч и до 1 миллиона (и более) дальтон. Поэтому белки отличаются длиной цепи, количеством каждой из 20-ти аминокислоты, порядком их очередности. Отсюда очевидно, что число вероятных аминокислотных последовательностей практически неисчерпаемо. Аминокислотный состав белков не одинаков и является важнейшей их характеристикой, определяется наследственной информацией, закодированной в ДНК.
Аминокислоты, входящие в состав белков, являются амфотерными электролитами, обладают свойствами как кислот, так и оснований.
Аминокислоты, входящие в состав белков, могут быть заменимыми и незаменимыми (не синтезируемыми в организме). Поэтому белки, содержащие все 8 незаменимых аминокислот, называют полноценными, лишенные (лимитированные) одной или нескольких - неполноценными. Степень полноценности зависит также от оптимального их соотношения в белке.
В связи с огромным разнообразием белков, различием их химических, физических и биологических функций классификация и номенклатура белков разработаны далеко не полностью. На сегодняшний день наиболее удачной считается классификация по структурным признакам с определенным сочетанием характерных физико-химических свойств белков.
Все белки по составу подразделяются на:
Ø простые (протеины);
Ø сложные (протеиды), в состав которых входят:
Ø глюкоза – гликопротеиды;
Ø липиды – липопротеиды;
Ø пигменты – хромопротеиды.
Ø нуклеиновые кислоты – нуклеопротеиды.
По пространственному расположению:
Ø фибриллярные (склеропротеины) – состоят из вытянутых или спирализованных полипептидных цепей, расположенных параллельно, полипептидные цепи объединены в волокна (фибриллы). Нерастворимы в воде.
Ø глобулярные (сферопротеины) – состоят из одной или нескольких полипептидных цепей, плотно свернутых за счет ковалентных и нековалентных связей в компактную частицу, называемую глобулой. Обычно хорошо растворимы в воде.
По количеству цепей в молекуле:
Ø олигомеры (больше, чем 1 цепь);
Ø протомеры (1 отдельная цепь).
По растворимости:
Ø альбумины – в воде и разведенных солях в интервале рН = 4-8,5;
Ø глобулины – в нейтральных растворах солей сильных кислот, нерастворимы в воде;
Ø глутелины – в разведенных щелочах и кислотах (содержат 45% глутаминовой кислоты);
Ø проламины – в 50-90%м этаноле (до 45% глутаминовой кислоты и 15% пролина);
Ø гистоны – низкомолекулярные, основные, растворимые в воде и кислотах.
Все белки имеют определенную пространственную структуру, которая очень сложная, но построена по определенным закономерностям. Основными уровнями строения белковой молекулы приняты:
Ø первичная;
Ø вторичная;
Ø третичная;
Ø четвертичная.
В молекуле белка линейная последовательность размещения аминокислот строго определена, характерна только для данного вида белка и определяет его природную структуру. Эта последовательность является уникальной и называется первичной структурой. В основе образования первичной структуры лежит пептидная связь, разрушаемая только при жестком химическом, физическом или термическом воздействии.
R1 – СО – NН - R2 – СО – NН - R3 - …….- СО – NН - Rn
Вторичная структура образуется в результате взаимодействия атома водорода одной цепи и атома кислорода другой или той же самой цепи с образованием водородной связи NH…O=CH-
Из-за большого количества образовавшихся водородных связей цепь белковой молекулы скручивается в спираль. Когда образование водородной связи невозможно из-за возникновения дисульфидных связей или наличия аминокислоты пролина, образуется изгиб или петля.
Кроме спиралевидной образуется еще и складчатая вторичная структура, характерная для коллагена – фибриллярного белка. Особенностями вторичной структуры объясняется различное отношение белков к внешним воздействиям. Так, спираль разрушается легко, тогда как коллаген очень стоек.
Полипептидные цепочки в белке определенным образом группируются и фиксируются в пространстве с помощью взаимодействия белковых групп одной цепи или нескольких. Такая структура также уникальная для каждого вида белка, называется третичной. В ее образовании принимают участие:
Ø дисульфидная связь R1-S-S-R2 (между группами -SH соседних участков);
Ø водородные мостики R1-C=O…H-N-R2;
Ø ионная связь R1-CО;
Ø O-H3N-R2;
Ø солевые мостики;
Ø эфирные связи.
Для многих белков характерна четвертичная структура – это объединение нескольких одинаковых по первичной, вторичной, третичной структуре белковых молекул. Четвертичную структуру имеет, например, гемоглобин.
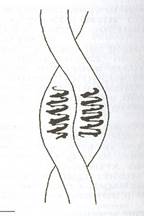

а) б) в)
Рис. 2.1. Схема структуры белка
а – вторичная, б - третичная; в - четвертичная
Каждая из перечисленных структур определяет свойства белковой молекулы. Суммарные свойства неизменного белка называется нативными свойствами.
С другой стороны, каждая из форм очень чувствительна к воздействию внешних факторов и может изменяться под их влиянием, вследствие свойства белка также изменяются.
|
|
Дата добавления: 2017-01-13; Просмотров: 397; Нарушение авторских прав?; Мы поможем в написании вашей работы!