
КАТЕГОРИИ:
Архитектура-(3434)Астрономия-(809)Биология-(7483)Биотехнологии-(1457)Военное дело-(14632)Высокие технологии-(1363)География-(913)Геология-(1438)Государство-(451)Демография-(1065)Дом-(47672)Журналистика и СМИ-(912)Изобретательство-(14524)Иностранные языки-(4268)Информатика-(17799)Искусство-(1338)История-(13644)Компьютеры-(11121)Косметика-(55)Кулинария-(373)Культура-(8427)Лингвистика-(374)Литература-(1642)Маркетинг-(23702)Математика-(16968)Машиностроение-(1700)Медицина-(12668)Менеджмент-(24684)Механика-(15423)Науковедение-(506)Образование-(11852)Охрана труда-(3308)Педагогика-(5571)Полиграфия-(1312)Политика-(7869)Право-(5454)Приборостроение-(1369)Программирование-(2801)Производство-(97182)Промышленность-(8706)Психология-(18388)Религия-(3217)Связь-(10668)Сельское хозяйство-(299)Социология-(6455)Спорт-(42831)Строительство-(4793)Торговля-(5050)Транспорт-(2929)Туризм-(1568)Физика-(3942)Философия-(17015)Финансы-(26596)Химия-(22929)Экология-(12095)Экономика-(9961)Электроника-(8441)Электротехника-(4623)Энергетика-(12629)Юриспруденция-(1492)Ядерная техника-(1748)
Примеры оценивания выполнения заданий
Инструкции по оцениванию
Модуль 2. Методические рекомендации по оцениванию выполнения заданий с развёрнутым ответом
В системе КИМ ЕГЭ по химии важная роль отведена заданиям с развернутым ответом, которые предусматривают комплексную проверку усвоения на высоком уровне сложности нескольких (двух и более) элементов содержания из различных содержательных блоков курса по общей, неорганической и органической химии.
Проверка выполнения таких заданий может быть осуществлена только путем независимой экспертизы и на основе специально разработанной стандартизированной системы оценивания, позволяющей свести до минимума расхождения в мнениях экспертов по оценке выполнения одной и той же работы.
Задание 36
| № п/п | Выявление элемента ответа (шаги оценивания) | Оценка | Примечание |
| Выявить наличие в ответе экзаменуемого запись электронного баланса: а) верно определены степени окисления элементов; б) верно записан процесс окисления; в) верно записан процесс восстановления. | 1 балл | Если допущены ошибки при: а) указании степени окисления элемента; б) указании знака (+/-) процесса, то элемент ответа оценивается в 0 баллов | |
| Выявить наличие в ответе экзаменуемого запись, указывающую окислитель и восстановитель | 1 балл | Любое из обозначений: · окислитель и восстановитель · «В» и «О» · «в-ль» и «ок-ль»; · «восст.» и «окисл.» считать верным, поскольку по условию задания не выдвигается требование указания процессов окисления и восстановления. | |
| Выявить наличие в ответе экзаменуемого запись уравнения реакции. | 1 балл | Если допущена ошибка хотя бы в одном коэффициенте, то элемент ответа оценивается в 0 баллов. |
Используя метод электронного баланса, составьте уравнение реакции:
K2MnO4 + …  MnBr2 + Br2 + … + H2O
MnBr2 + Br2 + … + H2O
Определите окислитель и восстановитель.
Элементы ответа:
1) Составлен электронный баланс:
| ||
| 2) Указано, что бромоводород (за счёт брома в степени окисления –1) является восстановителем, а манганат калия (за счёт марганца в степени окисления +6) – окислителем. | ||
| 3) Определены недостающие вещества, и расставлены коэффициенты в уравнении реакции: K2MnO4 + 8HBr = MnBr2 + 2Br2 + 4H2O + 2KBr |
Пример 1

Все элементы ответа выполнены верно, оценка 3 балла.
Пример 2

Верно выполнены первый и второй элементы ответа. В записи уравнения реакции допущена ошибка – гидроксид калия не может образоваться в присутствии бромоводородной кислоты. Оценка – 2 балла.
Контрольные вопросы
1) На проверку усвоения каких элементов содержания ориентированы задания на позиции № 36 экзаменационной работы 2016 года?
2) Сформированность каких важнейших умений должен установить эксперт в процессе проверки выполнения задания № 36 экзаменационной работы 2016 года?
Практические задания
Оцените выполнение задания.
Используя метод электронного баланса, составьте уравнение реакции:
Na2SO3 + … + H2SO4  … + MnSO4 + K2SO4 + H2O
… + MnSO4 + K2SO4 + H2O
Определите окислитель и восстановитель.
| Содержание верного ответа и указания по оцениванию(допускаются иные формулировки ответа, не искажающие его смысла) | Баллы | ||
Элементы ответа:
1) Составлен электронный баланс:
2) Указано, что Na2SO3 (за счёт серы в степени окисления +4) является восстановителем, а KMnO4 (за счёт марганца в степени окисления +7) – окислителем. 3) Определены недостающие вещества, и расставлены коэффициенты в уравнении реакции: 5Na2SO3 + 2KMnO4 + 3H2SO4 = 5Na2SO4 + 2MnSO4 + K2SO4 + 3H2O | |||
| Ответ правильный и полный, содержит все названные выше элементы | |||
| Правильно записаны только два из названных выше элементов ответа | |||
| Правильно записан один из названных выше элементов ответа | |||
| Все элементы ответа записаны неверно | |||
| Максимальный балл | 3 |
Ответ 1

Ответ 2
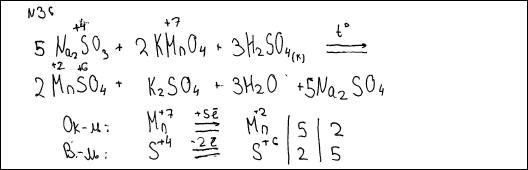
Ответ 3

Ответ 4

Ответ 5

Ответ 6

Ответ 7

Задание 37
|
|
Дата добавления: 2017-01-14; Просмотров: 362; Нарушение авторских прав?; Мы поможем в написании вашей работы!
