
КАТЕГОРИИ:
Архитектура-(3434)Астрономия-(809)Биология-(7483)Биотехнологии-(1457)Военное дело-(14632)Высокие технологии-(1363)География-(913)Геология-(1438)Государство-(451)Демография-(1065)Дом-(47672)Журналистика и СМИ-(912)Изобретательство-(14524)Иностранные языки-(4268)Информатика-(17799)Искусство-(1338)История-(13644)Компьютеры-(11121)Косметика-(55)Кулинария-(373)Культура-(8427)Лингвистика-(374)Литература-(1642)Маркетинг-(23702)Математика-(16968)Машиностроение-(1700)Медицина-(12668)Менеджмент-(24684)Механика-(15423)Науковедение-(506)Образование-(11852)Охрана труда-(3308)Педагогика-(5571)Полиграфия-(1312)Политика-(7869)Право-(5454)Приборостроение-(1369)Программирование-(2801)Производство-(97182)Промышленность-(8706)Психология-(18388)Религия-(3217)Связь-(10668)Сельское хозяйство-(299)Социология-(6455)Спорт-(42831)Строительство-(4793)Торговля-(5050)Транспорт-(2929)Туризм-(1568)Физика-(3942)Философия-(17015)Финансы-(26596)Химия-(22929)Экология-(12095)Экономика-(9961)Электроника-(8441)Электротехника-(4623)Энергетика-(12629)Юриспруденция-(1492)Ядерная техника-(1748)
Лекция 3. Основные понятия равновесной термодинамики
|
|
|
|
Основные понятия равновесной термодинамики
В дополнение к понятиям, описывающим состояние системы в молекулярной физике (п. 2.1), приведем еще ряд основных понятий, которые используются при описании процессов в термодинамике.
Уравнение состояния. В связи с тем, что макропараметры системы не являются независимыми, между ними существует вполне определенная формула связи, которая называется уравнением состояния. В самом простом случае, в отсутствие внешних полей (гравитационного, магнитного, электрического полей), такое уравнение связывает такие параметры, как 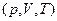
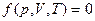 . (2.33)
. (2.33)
В более сложных случаях для характеристики равновесного состояния требуются и другие параметры (например, концентрация компонентов смеси газов, напряженность электрического поля, магнитная индукция и т.д.).
Функция состояния системы -это любая функция параметров системы, которая принимает одно и то же значение в данном состоянии системы независимо от способа перехода в это состояние.
Неравновесное состояние -состояние, в котором хотя бы один из термодинамических параметров не имеет определенного значения.
Процесс релаксации – процесс перехода предоставленной самой себе системы из неравновесного состояния в равновесное состояние.
Изолированная (замкнутая) система – система, которая не обменивается с внешними телами энергией и веществом.
Закрытая система -система, которая обменивается энергией и не обменивается частицами с окружающими ее внешними телами.
Открытая система – система, которая обменивается энергией и частицами с окружающими внешними телами.
Равновесный процесс (квазистатический процесс). В равновесной термодинамике изучают равновесные процессы. Под ними понимают процессы, в каждой точке которых макропараметры системы принимают определенные значения. Такие процессы являются идеализацией, они протекают бесконечно медленно в отсутствие разности давлений и температур.
|
|
|
Примером такого процесса является процесс бесконечно медленного сжатия газа под поршнем (рис. 2.7,а). В этом случае давление и температура газа будут одинаковыми во всех точках занимаемого газом объема. Если же перемещать поршень с конечной скоростью, то тогда непосредственно под поршнем образуется область газа (воздушная подушка), в которой его давление превышает давление в остальных точках объема (рис. 2.7,а). Следовательно, этот параметр для газа будет неопределенным и процесс не будет равновесным.
Равновесные процессы можно изображать на диаграммах состояниях, а неравновесные процессы нельзя из-за неопределенности параметров состояния в каждой точке процесса (их протекание можно обозначить пунктирной линией).
Все равновесные процессы являются обратимыми. Равновесный процесс, представляя собой непрерывную цепь равновесных состояний, является обратимым, т.е. обратимый процесс можно совершить в обратном направлении и при этом в окружающей среде не останется никаких изменений.
Круговой процесс - это процесс, при котором система возвращается в исходное состояние
Нулевое начало термодинамики. Его еще называют принципом термодинамического равновесия. Он утверждает следующее. Если система 1 находится в состоянии теплового равновесия по отдельности с системами 2 и 3, то эти две последние системы находятся в состоянии теплового равновесия между собой. Этот принцип приводит к понятию температуры, она будет одинаковой для систем, находящихся в состоянии теплового равновесия друг с другом. Для отдельной системы все ее части в равновесном состоянии также имеют одинаковую температуру.
Эта формулировка нулевого начала термодинамики эквивалентна той, которая была дана в п. 2.4.
|
|
|
|
|
Дата добавления: 2013-12-13; Просмотров: 567; Нарушение авторских прав?; Мы поможем в написании вашей работы!