
КАТЕГОРИИ:
Архитектура-(3434)Астрономия-(809)Биология-(7483)Биотехнологии-(1457)Военное дело-(14632)Высокие технологии-(1363)География-(913)Геология-(1438)Государство-(451)Демография-(1065)Дом-(47672)Журналистика и СМИ-(912)Изобретательство-(14524)Иностранные языки-(4268)Информатика-(17799)Искусство-(1338)История-(13644)Компьютеры-(11121)Косметика-(55)Кулинария-(373)Культура-(8427)Лингвистика-(374)Литература-(1642)Маркетинг-(23702)Математика-(16968)Машиностроение-(1700)Медицина-(12668)Менеджмент-(24684)Механика-(15423)Науковедение-(506)Образование-(11852)Охрана труда-(3308)Педагогика-(5571)Полиграфия-(1312)Политика-(7869)Право-(5454)Приборостроение-(1369)Программирование-(2801)Производство-(97182)Промышленность-(8706)Психология-(18388)Религия-(3217)Связь-(10668)Сельское хозяйство-(299)Социология-(6455)Спорт-(42831)Строительство-(4793)Торговля-(5050)Транспорт-(2929)Туризм-(1568)Физика-(3942)Философия-(17015)Финансы-(26596)Химия-(22929)Экология-(12095)Экономика-(9961)Электроника-(8441)Электротехника-(4623)Энергетика-(12629)Юриспруденция-(1492)Ядерная техника-(1748)
Лекція №13. Основи електрохімії
|
|
|
|
Основні питання:
1. Електрична провідність розчинів електролітів.
2. Фізико-хімічні методи дослідження: кондуктометрія, потенціометрія, вольтамперометрія.
3. Електрофізичні методи обробки харчових продуктів.
Електрохімія – розділ хімії, що вивчає закономірності хімічних перетворень при взаємодії електричного поля з речовиною та електричних явищ при хімічних реакціях. Електрохімія встановлює механізми процесів і явищ, що відбуваються на межі поділу фаз за участю заряджених частинок, у тому числі електричних явищ у живих організмах.
Класифікація електрохімічних процесів:
8 виникнення різниці потенціалів і одержання електричної енергії за рахунок хімічних реакцій (гальванічні елементи, корозія, нанесення електрохімічних покрить);
8 виникнення хімічних реакцій під дією електричного струму (електроліз).
Типи носіїв електричного струму (провідники):
1. Провідники першого роду. Носіями електрики є електрони. Належать метали.
2. Провідники другого роду. Носіями електрики є іони (іонна провідність) – катіони та аніони. Належать розчини і розплави електролітів.
Закон Ома: сила струму І в провіднику обернено пропорційна його опору R.
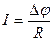 ,
,
де І – сила струму, А;
Δφ – різниця потенціалів, В;
R – опір провідника, Ом.
Електрична провідність – величина, що характеризує здатність речовини проводити електричний струм. Позначається α. Одиниці вимірювання в системі СИ: сименс (См) або Ом-1.
Якщо опір провідника R, електрична провідність провідника дорівнює: 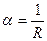 .
.
Опір однорідного провідника пропорційний його довжині і обернено пропорційний площі його розрізу:
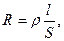
де l – довжина провідника, м;
S – площа розрізу, м2;
ρ – питомий опір матеріалу провідника, Ом·м.
|
|
|
Питома електрична провідність – величина, обернена до питомого опору провідника:
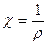
Питома електрична провідність характеризує матеріал провідника, численно дорівнює провідності речовини, заключеної в об’ємі між двома електродами, що знаходяться на відстані 1м і площею 1м2.
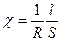 ,
,
де S – площа електродів, м2;
l – відстань між електродами, м;
R – опір речовини між електродами, Ом.
Електрична провідність розчину залежить від концентрації речовини у розчині. Тому для порівняння здатності різних електролітів проводити електричний струм використовують молярну електричну провідність.
Молярна електрична провідність розчину – величина, вимірювана електричною провідністю об’єму розчину, що містить 1 моль еквівалента речовини і заключного між електродами, що знаходяться на відстані 1м.
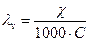 ,
,
де λv – молярна електрична провідність розчину, Ом-1·м-2·моль-1;
χ – питома електрична провідність, Ом-1 ·м-2·моль-1;
C –концентрація кількості речовини еквівалента, моль/л.
Зв’язок молярної електричної провідності з питомою електричною провідністю виражається рівнянням:
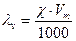 ,
,
де Vm – розведення розчину, чисельно дорівнює його об’єму в літрах, в якому міститься 1 моль речовини еквівалента електроліту: 
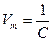 .
.
|
|
|
|
Дата добавления: 2013-12-14; Просмотров: 508; Нарушение авторских прав?; Мы поможем в написании вашей работы!