
КАТЕГОРИИ:
Архитектура-(3434)Астрономия-(809)Биология-(7483)Биотехнологии-(1457)Военное дело-(14632)Высокие технологии-(1363)География-(913)Геология-(1438)Государство-(451)Демография-(1065)Дом-(47672)Журналистика и СМИ-(912)Изобретательство-(14524)Иностранные языки-(4268)Информатика-(17799)Искусство-(1338)История-(13644)Компьютеры-(11121)Косметика-(55)Кулинария-(373)Культура-(8427)Лингвистика-(374)Литература-(1642)Маркетинг-(23702)Математика-(16968)Машиностроение-(1700)Медицина-(12668)Менеджмент-(24684)Механика-(15423)Науковедение-(506)Образование-(11852)Охрана труда-(3308)Педагогика-(5571)Полиграфия-(1312)Политика-(7869)Право-(5454)Приборостроение-(1369)Программирование-(2801)Производство-(97182)Промышленность-(8706)Психология-(18388)Религия-(3217)Связь-(10668)Сельское хозяйство-(299)Социология-(6455)Спорт-(42831)Строительство-(4793)Торговля-(5050)Транспорт-(2929)Туризм-(1568)Физика-(3942)Философия-(17015)Финансы-(26596)Химия-(22929)Экология-(12095)Экономика-(9961)Электроника-(8441)Электротехника-(4623)Энергетика-(12629)Юриспруденция-(1492)Ядерная техника-(1748)
Окислительно-восстановительные реакции
ОКИСЛИТЕЛЬНО-ВОССТАНОВИТЕЛЬНЫЕ ПРОЦЕССЫ
Лекция № 7
Окислительно-восстановительные процессы обуславливают многие явления в природе, жизни людей, технологических производствах, например: дыхание, горение, окисление, получение металлов из руд, коррозия и т.д.
На основе окислительно-восстановительных реакций созданы технологии очистки сточных вод, например, биологическая очистка, каталитическое разрушение органических загрязнений окислителями, удаление из воды кислорода, железа, марганца, озонирование воды и т.д.
На окислительно-восстановительных реакциях основан анализ природных вод (О2, БПК, ХПК, Fe2+, Fe3+, Mn и т.д.).
Ионные реакции, сопровождающиеся, изменением степени окисления атомов в молекулах реагирующих веществ называются окислительно-восстановительными реакциями.
Примером может служить реакция взаимодействия растворов KMnO4 (розовый) и KNO2 (бесцветный) в кислой среде, через определенное время раствор обесцвечивается.
В результате реакции




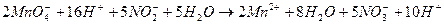
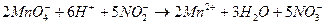
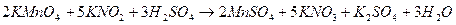
Вещество (ион), которое отдает электроны, окисляется и является восстановителем.
Вещество (ион), которое принимает электроны, восстанавливается и является окислителем.
Для составления уравнений удобно пользоваться методом электронно-ионного баланса.
Этот метод не требует обязательного знания степени окисления атомов и используется для написания реакций, проходящих в водных растворах.
|
Дата добавления: 2014-01-05; Просмотров: 351; Нарушение авторских прав?; Мы поможем в написании вашей работы!