
КАТЕГОРИИ:
Архитектура-(3434)Астрономия-(809)Биология-(7483)Биотехнологии-(1457)Военное дело-(14632)Высокие технологии-(1363)География-(913)Геология-(1438)Государство-(451)Демография-(1065)Дом-(47672)Журналистика и СМИ-(912)Изобретательство-(14524)Иностранные языки-(4268)Информатика-(17799)Искусство-(1338)История-(13644)Компьютеры-(11121)Косметика-(55)Кулинария-(373)Культура-(8427)Лингвистика-(374)Литература-(1642)Маркетинг-(23702)Математика-(16968)Машиностроение-(1700)Медицина-(12668)Менеджмент-(24684)Механика-(15423)Науковедение-(506)Образование-(11852)Охрана труда-(3308)Педагогика-(5571)Полиграфия-(1312)Политика-(7869)Право-(5454)Приборостроение-(1369)Программирование-(2801)Производство-(97182)Промышленность-(8706)Психология-(18388)Религия-(3217)Связь-(10668)Сельское хозяйство-(299)Социология-(6455)Спорт-(42831)Строительство-(4793)Торговля-(5050)Транспорт-(2929)Туризм-(1568)Физика-(3942)Философия-(17015)Финансы-(26596)Химия-(22929)Экология-(12095)Экономика-(9961)Электроника-(8441)Электротехника-(4623)Энергетика-(12629)Юриспруденция-(1492)Ядерная техника-(1748)
Топливные элементы. Характеристики аккумулятора Эдисона и свинцового аккумулятора Аккумулятор Эдисона Свинцовый аккумулятор Окислитель Ni2O3
|
|
|
|
Характеристики аккумулятора Эдисона и свинцового аккумулятора
| Аккумулятор Эдисона | Свинцовый аккумулятор | |
| Окислитель | Ni2O3 | PbO2 |
| Восстановитель | Fe | Pb |
| Электролит | КОН | H2SO4 |
| Напряжение (одного элемента) | 1,35 В | 2,0 В |
| Особенности | Легкий Постоянное напряжение Дорогой Необходимость перезарядки установить трудно (концентрация электролита постоянна) | Тяжелый Переменное напряжение при разрядке Недорогой Необходимость перезарядки легко установить по напряжению и плотности H2SO4 |
Гальванические источники тока одноразового действия представляют собой унифицированный контейнер, в котором находятся электролит, абсорбируемый активным материалом сепаратора, и электроды (анод и катод), поэтому они называются сухими элементами. Этот термин используется применительно ко всем элементам, не содержащим жидкого электролита. К обычным сухими элементам относятся углеродно-цинковые элементы или элементы Лекланше, напряжение которых составляет 1,5 В.
Сухие элементы применяются при малых токах и прерывистых режимах работы. Поэтому такие элементы широко используются в телефонных аппаратах, игрушках, системах сигнализации и др.
В последнее время ведутся исследования направленные на создание элементов, при работе которых расходовались бы дешевые вещества, такие как природный газ, керосин, водород и др. Такие химические элементы называются топливными.
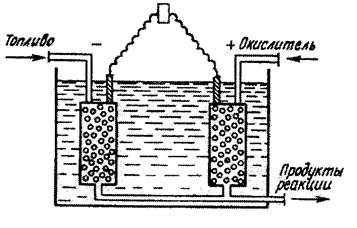
Схема топливного элемента
Топливные элементы осуществляют превращение энергии топлива в электрическую, минуя малоэффективные, идущие с большими потерями, процессы горения. Это электрохимические устройства в результате высокоэффективного «холодного» горения топлива непосредственно вырабатывает электроэнергию. В топливных элементах химическая энергия восстановителя (топлива) и окислителя превращаются в электрическую. Открытие в 1838 г. водородно-кислородного топливного элемента принадлежит английскому ученому В. Грову.
|
|
|
|
На отрицательном электроде протекает реакция 2H2 + 4OH- - 4е = 4H2O,
на положительном O2 + 2H2O + 4 e = 4OH-.
Суммарное уравнение реакции: O2 + 2H2 = 2H2O. Электроны перемещаются от анода к катоду, а в растворе происходит движение ионов ОН- от катода к аноду.
Биохимики установили, что биологический водородно-кислородный топливный элемент «вмонтирован» в каждую живую клетку. Источником водорода в организме служит пища – жиры, белки и углеводы. В желудке, кишечнике, клетках она в конечном итоге превращается до мономеров, которые, в свою очередь, после ряда химических превращений дают водород, присоединенный к молекуле–носителю. Кислород из воздуха попадает в кровь через легкие, соединяется с гемоглобином и разносится по всем тканям. Процесс соединения водорода с кислородом составляет основу биоэнергетики организма. Здесь, в мягких условиях (комнатная температура, нормальное давление, водная среда), химическая энергия с высоким КПД преобразуется в тепловую, механическую (движение мышц), электричество (электрический скат), свет (насекомые, излучающие свет).
Для большинства топливных элементов э.д.с. составляет 1,0 - 1,5 В. Топливные элементы уже сейчас используются в спутниках и космических кораблях, перспективно их использование вместо двигателей внутреннего сгорания на транспорте, в большой энергетике и т.п. Человек, в который раз повторил созданное природой устройство для получения энергии. Топливные элементы вселяют надежду на энергетическое будущее.
|
|
|
|
|
|
|
|
Дата добавления: 2014-01-05; Просмотров: 498; Нарушение авторских прав?; Мы поможем в написании вашей работы!