
КАТЕГОРИИ:
Архитектура-(3434)Астрономия-(809)Биология-(7483)Биотехнологии-(1457)Военное дело-(14632)Высокие технологии-(1363)География-(913)Геология-(1438)Государство-(451)Демография-(1065)Дом-(47672)Журналистика и СМИ-(912)Изобретательство-(14524)Иностранные языки-(4268)Информатика-(17799)Искусство-(1338)История-(13644)Компьютеры-(11121)Косметика-(55)Кулинария-(373)Культура-(8427)Лингвистика-(374)Литература-(1642)Маркетинг-(23702)Математика-(16968)Машиностроение-(1700)Медицина-(12668)Менеджмент-(24684)Механика-(15423)Науковедение-(506)Образование-(11852)Охрана труда-(3308)Педагогика-(5571)Полиграфия-(1312)Политика-(7869)Право-(5454)Приборостроение-(1369)Программирование-(2801)Производство-(97182)Промышленность-(8706)Психология-(18388)Религия-(3217)Связь-(10668)Сельское хозяйство-(299)Социология-(6455)Спорт-(42831)Строительство-(4793)Торговля-(5050)Транспорт-(2929)Туризм-(1568)Физика-(3942)Философия-(17015)Финансы-(26596)Химия-(22929)Экология-(12095)Экономика-(9961)Электроника-(8441)Электротехника-(4623)Энергетика-(12629)Юриспруденция-(1492)Ядерная техника-(1748)
Многоэлектронные атомы и периодический закон Менделеева
|
|
|
|
Четыре квантовых числа  полностью характеризуют состояние одного электрона в поле атомного ядра. В многоэлектронном атоме нужно учитывать еще и взаимодействие электронов друг с другом.
полностью характеризуют состояние одного электрона в поле атомного ядра. В многоэлектронном атоме нужно учитывать еще и взаимодействие электронов друг с другом.
Для того, чтобы качественно разобраться в строении и свойствах сложных атомов необходимо упомянуть следующие положения:
– согласно принципу Паули, в одном и том же атоме не может быть двух электронов, у которых были бы одинаковыми все четыре квантовых числа;
– в основном состоянии атом и электрон в нем обладают наименьшей энергией.
Учитывая это, можно установить связь между строением электронных оболочек атома и его местом в периодической системе Менделеева.
Наименьшее значение главного квантового числа  , следовательно,
, следовательно,  . Согласно определению, величина
. Согласно определению, величина 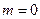 , а
, а 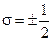 . В соответствии со схемой, рассмотренной нами ранее, можно сказать, что электрон в атоме водорода находится в состоянии
. В соответствии со схемой, рассмотренной нами ранее, можно сказать, что электрон в атоме водорода находится в состоянии 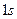 .
.
В атоме гелия (порядковый номер 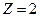 ) его второй электрон также может находиться в состоянии
) его второй электрон также может находиться в состоянии 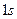 , то есть иметь такие же квантовые числа
, то есть иметь такие же квантовые числа  , но спин второго электрона должен быть ориентирован противоположно спину первого (для одного из них
, но спин второго электрона должен быть ориентирован противоположно спину первого (для одного из них  , для другого
, для другого  ). Группа состояний с
). Группа состояний с  образует заполненную
образует заполненную  -оболочку атома, соответствующую завершению первого периода системы Менделеева.
-оболочку атома, соответствующую завершению первого периода системы Менделеева.
Следующий за гелием элемент – литий – содержит три электрона. По принципу Паули третий электрон атома лития уже не может разместиться в заполненной  -оболочке и занимает низшее состояние в оболочке с
-оболочке и занимает низшее состояние в оболочке с  или
или 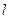 - оболочке. Таким состоянием является состояние
- оболочке. Таким состоянием является состояние 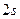 (
( ). Литием начинается второй период системы Менделеева.
). Литием начинается второй период системы Менделеева.
Четвертый элемент – бериллий. В бериллии четвертый электрон отличается от третьего только значением спина. Он тоже попадает в состояние 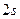 .
.
|
|
|
В атоме бора пять электронов. Пятый электрон уже не может попасть в состояние 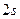 , он оказывается в состоянии
, он оказывается в состоянии  . Таким образом, у бора два электрона находятся в состоянии
. Таким образом, у бора два электрона находятся в состоянии 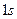 , 2 электрона - в состоянии
, 2 электрона - в состоянии 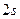 и один – в состоянии
и один – в состоянии  , так как при
, так как при 
 , а в каждом из этих состояний
, а в каждом из этих состояний 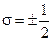 .
.
В последующих четырех элементах C, N, O, F электроны заполняют постепенно все  состояния. У неона вся оболочка с
состояния. У неона вся оболочка с  заполнена. У натрия одиннадцатый электрон должен находиться в оболочке с
заполнена. У натрия одиннадцатый электрон должен находиться в оболочке с  (M - оболочка). Так как по определению
(M - оболочка). Так как по определению 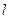 принимает только целочисленные значения, лежащие в интервале от 0 до
принимает только целочисленные значения, лежащие в интервале от 0 до  , то при
, то при  квантовое число
квантовое число  может иметь три разных значения
может иметь три разных значения  . При l=0 в состоянии
. При l=0 в состоянии 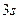 могут быть два электрона с противоположными спинами. При l=1 в состоянии
могут быть два электрона с противоположными спинами. При l=1 в состоянии 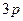 может быть 6 электронов. При l=2 в состоянии
может быть 6 электронов. При l=2 в состоянии  квантовое число
квантовое число 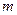 имеет пять значений
имеет пять значений  . В каждом из них могут находиться по два электрона с противоположными спинами, то есть всего в состоянии
. В каждом из них могут находиться по два электрона с противоположными спинами, то есть всего в состоянии  могут быть 10 электронов.
могут быть 10 электронов.
Изложенное выше, позволяет понять, чем определяется периодичность свойств установленная Менделеевым.
У атомов гелия, неона и аргона (строка в таблице Менделеева) оболочки целиком заполнены и свойства этих элементов схожи. У атомов Li, Na, K (столбец в таблице Менделеева) имеется по одному электрону сверх заполненных оболочек. Эти элементы также обладают схожими свойствами. Таким образом, сходство физических и химических свойств есть следствие сходства строения электронных оболочек атомов.
Создание периодической системы Менделеева и ее теоретическое объяснение явилось величайшим достижением современной физики. Оно оказалось возможным лишь на основе квантовой механики.
|
|
|
|
Дата добавления: 2014-01-05; Просмотров: 901; Нарушение авторских прав?; Мы поможем в написании вашей работы!