
КАТЕГОРИИ:
Архитектура-(3434)Астрономия-(809)Биология-(7483)Биотехнологии-(1457)Военное дело-(14632)Высокие технологии-(1363)География-(913)Геология-(1438)Государство-(451)Демография-(1065)Дом-(47672)Журналистика и СМИ-(912)Изобретательство-(14524)Иностранные языки-(4268)Информатика-(17799)Искусство-(1338)История-(13644)Компьютеры-(11121)Косметика-(55)Кулинария-(373)Культура-(8427)Лингвистика-(374)Литература-(1642)Маркетинг-(23702)Математика-(16968)Машиностроение-(1700)Медицина-(12668)Менеджмент-(24684)Механика-(15423)Науковедение-(506)Образование-(11852)Охрана труда-(3308)Педагогика-(5571)Полиграфия-(1312)Политика-(7869)Право-(5454)Приборостроение-(1369)Программирование-(2801)Производство-(97182)Промышленность-(8706)Психология-(18388)Религия-(3217)Связь-(10668)Сельское хозяйство-(299)Социология-(6455)Спорт-(42831)Строительство-(4793)Торговля-(5050)Транспорт-(2929)Туризм-(1568)Физика-(3942)Философия-(17015)Финансы-(26596)Химия-(22929)Экология-(12095)Экономика-(9961)Электроника-(8441)Электротехника-(4623)Энергетика-(12629)Юриспруденция-(1492)Ядерная техника-(1748)
Титриметрический (волюмометрический) анализ
|
|
|
|
Титриметрический (волюмометрический) анализ – совокупность методов количественного химического анализа, заключающихся в измерении объема раствора реагента известной концентрации (титрант) расходуемого на реакцию с некоторым количеством определяемого вещества, находящегося в растворе.
Анализ осуществляется путем титрования – регулируемого прибавления контролируемого количества титранта к анализируемому раствору.
В ходе титрования вещества (титрант и определяемое вещество) реагируют друг с другом в эквивалентных соотношениях.
Титрант – раствор реагента с известной концентрацией (стандартный, а чаще рабочий стандартизированный раствор), находящийся, как правило, в бюретке и при титровании добавляемый небольшими порциями к раствору титруемого вещества.
Когда количество эквивалента добавленного титранта равно количеству эквивалента титруемого вещества достигается момент эквивалентности (соответствующий точке эквивалентности) и описываемый законом эквивалентов:
| Вещества реагируют в эквивалентных количествах. nх = nтэ | ||
В математическом написании закон эквивалентов существует в двух видах:
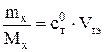 или
или
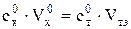
|
Главной задачей на практике является прекращение титрования в момент эквивалентности (или в момент максимально приближенный к моменту эквивалентности – ошибка не должна превышать 1 %).
Известны три способа фиксирования точки эквивалентности:
1) индикаторный – с применением вспомогательных веществ – индикаторов – не участвующих в реакции, но изменяющие свой цвет при изменении различных (в зависимости от метода) свойств титруемого раствора;
2) безиндикаторный –вспомогательные вещества не применяются, в ходе титрования изменяется окраска участников реакции;
|
|
|
3) инструментальный – точку эквивалентности устанавливают по резкому изменению какого-либо физико-химического свойства раствора, которое фиксируют с помощью прибора.
Инструментальный способ фиксирования точки эквивалентности наиболее точный, но требуют определенного оборудования.
В пищевом анализе основные показатели качества согласно ГОСТам (кислотность, окисляемость, общая жесткость) определяют титрованием с применением индикаторов. Поэтому основная задача таких анализов сводится к выбору индикаторов, позволяющих закончить титрование как можно ближе к точке эквивалентности.
|
|
|
|
|
Дата добавления: 2014-01-06; Просмотров: 2684; Нарушение авторских прав?; Мы поможем в написании вашей работы!