
КАТЕГОРИИ:
Архитектура-(3434)Астрономия-(809)Биология-(7483)Биотехнологии-(1457)Военное дело-(14632)Высокие технологии-(1363)География-(913)Геология-(1438)Государство-(451)Демография-(1065)Дом-(47672)Журналистика и СМИ-(912)Изобретательство-(14524)Иностранные языки-(4268)Информатика-(17799)Искусство-(1338)История-(13644)Компьютеры-(11121)Косметика-(55)Кулинария-(373)Культура-(8427)Лингвистика-(374)Литература-(1642)Маркетинг-(23702)Математика-(16968)Машиностроение-(1700)Медицина-(12668)Менеджмент-(24684)Механика-(15423)Науковедение-(506)Образование-(11852)Охрана труда-(3308)Педагогика-(5571)Полиграфия-(1312)Политика-(7869)Право-(5454)Приборостроение-(1369)Программирование-(2801)Производство-(97182)Промышленность-(8706)Психология-(18388)Религия-(3217)Связь-(10668)Сельское хозяйство-(299)Социология-(6455)Спорт-(42831)Строительство-(4793)Торговля-(5050)Транспорт-(2929)Туризм-(1568)Физика-(3942)Философия-(17015)Финансы-(26596)Химия-(22929)Экология-(12095)Экономика-(9961)Электроника-(8441)Электротехника-(4623)Энергетика-(12629)Юриспруденция-(1492)Ядерная техника-(1748)
Реакции электрофильного замещения в ароматическом ряду
|
|
|
|
План
5.1. Реакции SE для бензоидных ароматических соединений
5.2. Ориентирующее влияние заместителей
5.3. Реакции SE в гетероциклических соединениях
5.1. Реакции SE для бензоидных ароматических соединений
Электрофильное замещение при атоме углерода в sp2-гибридизации наиболее характерно для ароматических соединений, т.к. соединения с двойными связями неароматического характера гораздо легче вступают в реакции электрофильного присоединения, чем замещения.
Большинство реакций электрофильного замещения (SE) протекают по общему механизму.
 Электрофильное замещение в ароматическом ряду начинается с атаки π-электронной системы ароматического кольца электрофильной частицей (для этого нужны сильные электрофилы, которые, как правило, генерируются с помощью катализатора). При этом вначале образуется так называемый π-комплекс, в котором электрофил еще не связан ни с каким атомом углерода, а удерживается всей π-электронной системой. Затем π-комплекс превращается в σ-комплекс (ион карбония), при этом электрофил уже связан с определенным атомом углерода ароматического кольца, образуя связь за счет двух электронов π-электронной системы, но при этом нарушается ароматичность (т.к. один атом углерода становится sp3-гибридным. Существование σ-комплекса доказано экспериментально. В дальнейшем происходит стабилизация σ-комплекса путем высвобождения протона.
Электрофильное замещение в ароматическом ряду начинается с атаки π-электронной системы ароматического кольца электрофильной частицей (для этого нужны сильные электрофилы, которые, как правило, генерируются с помощью катализатора). При этом вначале образуется так называемый π-комплекс, в котором электрофил еще не связан ни с каким атомом углерода, а удерживается всей π-электронной системой. Затем π-комплекс превращается в σ-комплекс (ион карбония), при этом электрофил уже связан с определенным атомом углерода ароматического кольца, образуя связь за счет двух электронов π-электронной системы, но при этом нарушается ароматичность (т.к. один атом углерода становится sp3-гибридным. Существование σ-комплекса доказано экспериментально. В дальнейшем происходит стабилизация σ-комплекса путем высвобождения протона.
Примеры реакций SE для бензола:
1) галогенирование
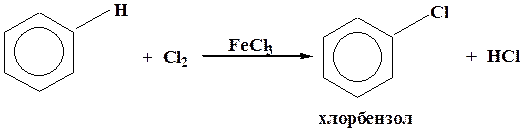
В качестве электрофила выступает либо комплекс галогена с кислотой Льюиса (FeCl3), либо катион, образующийся в результате диссоциации этого комплекса.
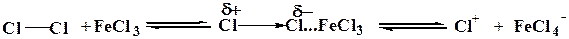
В организме протекает очень важная реакция иодирования.
|
|
|
Гормоны щитовидной железы имеют в своем составе иодпроизводное одной из α-аминокислот – тирозина.
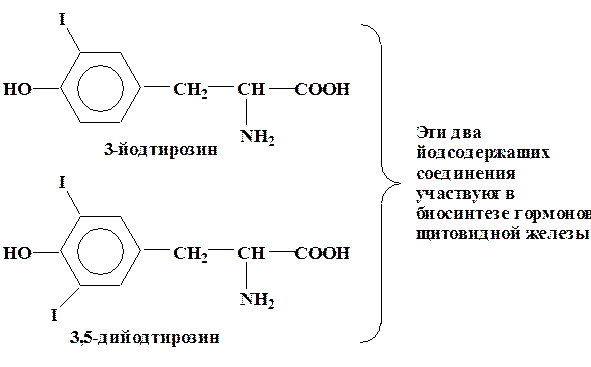
С помощью меченого йода было доказано экспериментально, что вначале образуется 3-йодтирозин, затем 3,5-дийодтирозин, а конечным продуктом иодирования является тироксин – гормон щитовидной железы.
2) нитрование

Азотная кислота по отношению к серной (более сильной) ведет себя как основание.
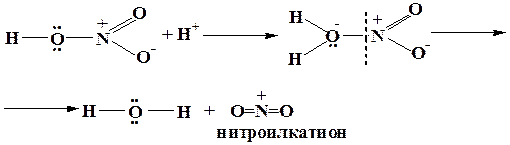
Либо в общем виде:
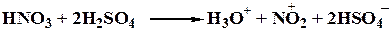

3) сульфирование.
Сульфирующим агентом является дымящая Н2SО4 с растворенным в ней SO3, который и служит электрофилом.
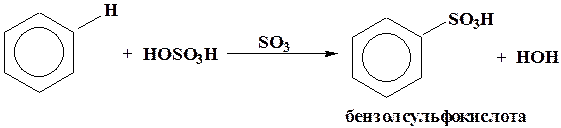

4) алкилирование (реакция Фриделя-Крафтса)
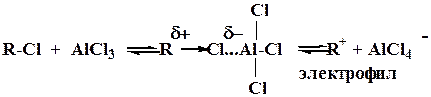

При алкилировании пропеном в кислой среде образуется изопропилбензол (кумол). Реакция имеет значение при промышленном получении фенола.
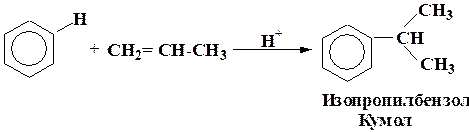
5) ацилирование

|
|
|
|
Дата добавления: 2014-01-06; Просмотров: 1116; Нарушение авторских прав?; Мы поможем в написании вашей работы!