
КАТЕГОРИИ:
Архитектура-(3434)Астрономия-(809)Биология-(7483)Биотехнологии-(1457)Военное дело-(14632)Высокие технологии-(1363)География-(913)Геология-(1438)Государство-(451)Демография-(1065)Дом-(47672)Журналистика и СМИ-(912)Изобретательство-(14524)Иностранные языки-(4268)Информатика-(17799)Искусство-(1338)История-(13644)Компьютеры-(11121)Косметика-(55)Кулинария-(373)Культура-(8427)Лингвистика-(374)Литература-(1642)Маркетинг-(23702)Математика-(16968)Машиностроение-(1700)Медицина-(12668)Менеджмент-(24684)Механика-(15423)Науковедение-(506)Образование-(11852)Охрана труда-(3308)Педагогика-(5571)Полиграфия-(1312)Политика-(7869)Право-(5454)Приборостроение-(1369)Программирование-(2801)Производство-(97182)Промышленность-(8706)Психология-(18388)Религия-(3217)Связь-(10668)Сельское хозяйство-(299)Социология-(6455)Спорт-(42831)Строительство-(4793)Торговля-(5050)Транспорт-(2929)Туризм-(1568)Физика-(3942)Философия-(17015)Финансы-(26596)Химия-(22929)Экология-(12095)Экономика-(9961)Электроника-(8441)Электротехника-(4623)Энергетика-(12629)Юриспруденция-(1492)Ядерная техника-(1748)
Основные понятия. Законы термодинамики
|
|
|
|
Законы термодинамики
Теплота, температура и внутренняя энергия. Теплоемкость. Передача теплоты. Теплопроводность. Конвекция. Излучение. Первое начало термодинамики. Закон сохранения и превращения энергии в термодинамике. Изотермический, изобарный, изохорный и адиабатический процессы. Тепловой двигатель. Цикл Карно. Работа и теплота как форма изменения внутренней энергии. Понятие об энтропии. Второе начало термодинамики. Различные формулировки второго НТД. Третье начало термодинамики. Термодинамические потенциалы.
Чайник с водой, находящийся на газовой плите, нагревается. Предметы, имеющие разную температуру, при соприкосновении приходят к состоянию, когда их температуры выравниваются. Причем более теплое тело становится холодней, а холодное нагревается. С давних времен ученые пытались понять, что такое тепло. Много тысяч лет назад наши предки добывали огонь трением друг о друга двух деревянных предметов. Не осознавая этого, они превращали механическую работу в теплоту, которая приводили к возгоранию деревянных предметов.
К ранним теориям теплоты относится теория теплорода – перетекание невесомой жидкости от одного тела к другому. Теорию теплорода опроверг английский физик Б. Томпсон.
Пытаясь объяснить, почему при высверливании стволов пушек тупыми сверлами перетекание теплорода может продолжаться бесконечно долго. Сначала он полагал, что теплород выделяется при разрушении металла. Но оказалось, что при использовании тупых сверл разрушения металла не происходило, а тепло продолжало выделяться в течение длительного времени. Это противоречило представлению о содержании в веществе ограниченного количества теплорода. Им была высказана мысль о том, что теплота является особым видом движения. Она возникает при совершении механической работы, например, при трении тел друг о друга.
|
|
|

Рис.7.1. Бенжамин Томпсон (1753-1814).
Введенное понятие теплового потока позволило объяснить ряд физических явлений, например, переход тепла от горячего тела к холодному. Это понятие сохранилось и в современных представлениях о теплоте.
Единица измерения теплоты называется калорией (в переводе латинского calor — тепло). Она определяется как количество теплоты, необходимое для повышения температуры одного грамма воды на один градус Цельсия от температуры 14.50С до 15.50С. Конкретное указание температуры обусловлено небольшой (в пределах 1%) зависимостью количества теплоты, требуемой для нагрева, от температуры.
В экспериментах, выполненных в дальнейшем Джеймсом Джоулем[1], был установлен механический эквивалент теплоты (Джоуль):
4.184 Дж = 1 кал, 4.184 кДж=1 ккал.
Таким образом, было установлено: теплота - это способ передачи энергии. Теплота Q – это энергия, которая переходит от одного тела к другому между телами с разной температурой или, другими словами, мера переноса энергии от одного тела к другому при разнице температур.
Следуетразличать понятия теплоты и внутренней энергии. Под внутренней или тепловой энергией W понимают полную сумму всех видов энергии всех молекул, принадлежащих телу. Она включает в себя кинетическую энергию поступательного движения молекул, потенциальную энергию их взаимодействия, энергию межатомных и межмолекулярных связей, наличие вращательных и колебательных степеней свободы у атомов и молекул и т.д. Температура характеризует только часть внутренней энергии тела. Под температурой T понимают среднюю кинетическую энергию всех молекул. Рассмотренное выше распределение молекул по скоростям (распределение Максвелла, представленное на рис.6.6) свидетельствует о том. что при одинаковой температуре скорости молекул распределены в широком интервале скоростей. Температуру характеризует среднеквадратичная скорость молекул, описываемая соотношением (6.6.3).
|
|
|
. Отметим, что газ называют идеальным, когда размерами и взаимодействием молекул можно пренебречь. Примером такого газа может служить разряженный идеальный газ. Внутренняя энергия идеального одноатомного газа является суммой кинетических и потенциальных энергий поступательного движения всех атомов. Потенциальной энергией взаимодействия атомов идеального газа можно пренебречьДля одноатомного идеального газа понятия внутренней энергии и температуры совпадают. Она равна средней кинетической энергии одной молекулы умноженной на полное число молекул N:
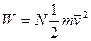 , (7.1.1)
, (7.1.1)
или
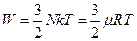 , (7.1.2)
, (7.1.2)
где N и μ – соответственно число молекул и молей газа.
У многоатомного идеального газа при данной температуре внутренняя энергия больше, чем у одноатомного идеального газа, но остается функцией температуры. У реальных газов в областях, где их поведение отличается от идеального газа, внутренняя энергия зависит еще от объема и давления. Функция, описывающая внутреннюю энергию жидкостей и твердых тел, имеет очень сложный вид, поскольку энергия электростатического взаимодействия атомов и молекул велика.
В этом заключаются различия между понятиями теплоты Q, температуры T и внутренней энергии W.
|
|
|
|
|
Дата добавления: 2014-01-07; Просмотров: 256; Нарушение авторских прав?; Мы поможем в написании вашей работы!