
КАТЕГОРИИ:
Архитектура-(3434)Астрономия-(809)Биология-(7483)Биотехнологии-(1457)Военное дело-(14632)Высокие технологии-(1363)География-(913)Геология-(1438)Государство-(451)Демография-(1065)Дом-(47672)Журналистика и СМИ-(912)Изобретательство-(14524)Иностранные языки-(4268)Информатика-(17799)Искусство-(1338)История-(13644)Компьютеры-(11121)Косметика-(55)Кулинария-(373)Культура-(8427)Лингвистика-(374)Литература-(1642)Маркетинг-(23702)Математика-(16968)Машиностроение-(1700)Медицина-(12668)Менеджмент-(24684)Механика-(15423)Науковедение-(506)Образование-(11852)Охрана труда-(3308)Педагогика-(5571)Полиграфия-(1312)Политика-(7869)Право-(5454)Приборостроение-(1369)Программирование-(2801)Производство-(97182)Промышленность-(8706)Психология-(18388)Религия-(3217)Связь-(10668)Сельское хозяйство-(299)Социология-(6455)Спорт-(42831)Строительство-(4793)Торговля-(5050)Транспорт-(2929)Туризм-(1568)Физика-(3942)Философия-(17015)Финансы-(26596)Химия-(22929)Экология-(12095)Экономика-(9961)Электроника-(8441)Электротехника-(4623)Энергетика-(12629)Юриспруденция-(1492)Ядерная техника-(1748)
Властивості бензолу
|
|
|
|
Властивості. Бензол - безбарвна рідина що має характерний запах. Легко переходить у твердий стан: температура плавлення бензолу становить +5,5°С, температура кипіння +80,1°С. У воді бензол практично не розчиняється але є хорошим розчинником багатьох органічних речовин.
Хімічні властивості бензолу та інших ароматичних сполук характеризуються рядом особливостей.
Для бензолу характерні реакції заміщення атомів водню в бензольному кільці. Ці реакції відбуваються за механізмом електрофільного заміщення. Електрофільна частинка Х+ взаємодіє з p - електронами молекули бензолу, утворюючи p-комплекс, який переходить у s- комплекс. В s- комплексі частинка Х+ сполучена з одним з атомів вуглецю, в результаті ароматичний характер молекули порушується. Далі від s- комплексу відщеплюється протон і відновлюється ароматичний характер ядра. Механізм цієї реакції можна проілюструвати такою схемою:

p - комплекс s - комплекс
На відміну від ненасичених сполук типу алкенів і алкінів, бензол дуже стійкий проти окислення, важко вступає в реакції приєднання. Розглянемо найбільш характерні для ароматичних вуглеводнів реакції.
1. Нітрування. При дії на бензол нітруючої суміші (суміш концентрованих азотної і сірчаної кислот) відбувається заміщення водню в ядрі бензолу на групу NO2; цей процес називається нітруванням:

Реакція відбувається за механізмом електрофільного заміщення. Роль електрофільної частинки відіграє іон NO2+, який утворюється в результаті реакції:

2. Сульфування. Водень в бензольному ядрі може бути заміщений на сульфогрупу SO3H під дією концентрованої сірчаної кислоти; цей процес називається сульфуванням:
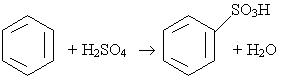
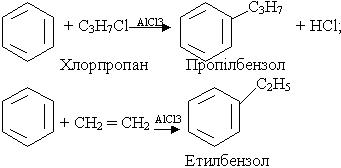
3. Алкілування. В молекулу бензолу замість водню можна ввести алкільний радикал. Процес алкілування можна здійснити дією на бензол галагенопохідної алкану чи олефіну при наявності каталізатора (хлорид алюмінію AlCl3):
|
|
|
4. Галогенування. Заміщення водню в бензольному ядрі на хлор чи бром здійснюється при взаємодії бензолу з галогенами за участю каталізатора. Реакцію можуть каталізувати FeCl3 (або FeBr3) і AlCl3, при цьому утворюються різні продукти:
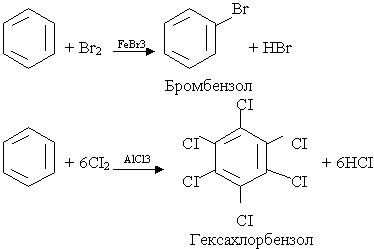
Під час інтенсивного опромінення реакційної системи світлом бензол може приєднувати хлор:
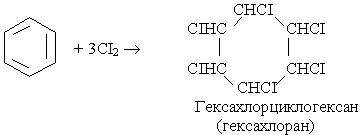
На відміну від наведених вище реакцій галогенування, в яких атом хлору чи брому заміщує водень в бензольному ядрі, в цій реакції атоми хлору приєднуються до всіх атомів вуглецю. В результаті руйнується p- електронна система бензолу і утворюється галагенопохідна циклоалкану
5. Гідрування. Одна з не багатьох реакцій приєднання, в яку може вступати бензол, - реакція гідрування при наявності платинових або нікелевих каталізаторів:
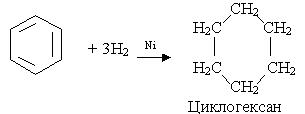
Добування. Бензол виділяють переважно з нафти та кам'яного вугілля при виробництві коксу.
Бензол можна добути з циклогексану за реакцією дегідрування з участю платини як каталізатора або шляхом циклізації і дегідрування нормального гексану при наявності Cr2O3:

Бензол утворюється також під час пропускання ацетилену над розжареним активним вугіллям:

Застосування. Бензол є важливою сировиною для органічного синтезу його використовують при добуванні багатьох інших ароматичних сполук. Бензол застосовують в виробництві барвників, пластмас, пестицидів, вибухових речовин, ліків; його використовують як розчинник лаків, фарб.
Бензол входить до складу палива, яке використовується в двигунах внутрішнього згоряння.
|
|
|
|
|
Дата добавления: 2014-01-07; Просмотров: 6345; Нарушение авторских прав?; Мы поможем в написании вашей работы!