
КАТЕГОРИИ:
Архитектура-(3434)Астрономия-(809)Биология-(7483)Биотехнологии-(1457)Военное дело-(14632)Высокие технологии-(1363)География-(913)Геология-(1438)Государство-(451)Демография-(1065)Дом-(47672)Журналистика и СМИ-(912)Изобретательство-(14524)Иностранные языки-(4268)Информатика-(17799)Искусство-(1338)История-(13644)Компьютеры-(11121)Косметика-(55)Кулинария-(373)Культура-(8427)Лингвистика-(374)Литература-(1642)Маркетинг-(23702)Математика-(16968)Машиностроение-(1700)Медицина-(12668)Менеджмент-(24684)Механика-(15423)Науковедение-(506)Образование-(11852)Охрана труда-(3308)Педагогика-(5571)Полиграфия-(1312)Политика-(7869)Право-(5454)Приборостроение-(1369)Программирование-(2801)Производство-(97182)Промышленность-(8706)Психология-(18388)Религия-(3217)Связь-(10668)Сельское хозяйство-(299)Социология-(6455)Спорт-(42831)Строительство-(4793)Торговля-(5050)Транспорт-(2929)Туризм-(1568)Физика-(3942)Философия-(17015)Финансы-(26596)Химия-(22929)Экология-(12095)Экономика-(9961)Электроника-(8441)Электротехника-(4623)Энергетика-(12629)Юриспруденция-(1492)Ядерная техника-(1748)
Электронное строение атома. Закономерности изменения свойств элементов и их соединений
Система четырех квантовых чисел позволяет определить число возможных состояний электрона в атоме в зависимости от уровня и подуровня, на котором он находится.
Согласно принципа (запрета) Паули в атоме не может быть двух и более электронов с четырьмя одинаковыми квантовыми числами.
Электроны, имеющие одинаковые значения n, ℓ и mℓ отличающиеся спиновым квантовым числом ms, образуют орбиталь, которая условно обозначается символом . Орбиталь—это область пространства, в которой пребывание электрона является наиболее вероятным, а следовательно, электронное облако отличается максимальной плотностью.
Правило Гунда заключается в том, что при заполнении орбиталей с одинаковой энергией электроны располагаются так, чтобы суммарный спин их был максимальным.
При переходе от одного элемента к следующему в периодической системе электрон стремится занять состояние с минимальной энергией. Последовательность заполнения электронами энергетических уровней и подуровней в порядке возрастания их энергии подчиняется правилу М. В. Клечковского и имеет
следующий вид:
1s < 2s < 2p < зs < Зp < 4s < 3d< 4р < 5s < 4d< 5р < 6s < 5d (или 4f) <6p
Атом не имеет строго определенных границ. За его радиус принимается расстояние от ядра до главного максимума плотности внешних электронных оболочек. С увеличением заряда ядра в периодах атомный радиус немонотонно уменьшается, а в группах увеличивается.
Энергия ионизации Еi — это энергия, необходимая для отрыва наиболее
слабо связанного электрона от атома, количественно выражается в кДж/моль
или эВ. Чем меньше энергия ионизации, тем легче атом отдает электрон при
образовании химической связи, т.е. элемент является более сильным восстановителем. Поэтому восстановительная способность нейтральных атомов с ростом заряда ядра в периоде уменьшается, а в главных подгруппах растет.
Энергия сродства к электрону Еср — энергия, выделяющаяся при присоединении электрона к нейтральному атому, количественно выражается в кДж/моль или эВ. Она определяет окислительные свойства несвязанных атомов. Чем больше электронное сродство, тем более сильным окислителем является данный элемент. Окислительной способностью не обладают нейтральные атомы с устойчивыми конфигурациями s2, s2p6. У остальных элементов в таблице Д.И. Менделеева окислительная способность нейтральных атомов повышается слева направо и снизу вверх.
Электроотрицательностью элемента (ЭО) называют меру относительной
способности атомов оттягивать на себя электроны при образовании химической связи. Она пропорциональна как энергии ионизации, так и энергии сродства к электрону. С ростом заряда в периодах электроотрицательность в общем растет, а в подгруппах уменьшается.
Периоды. Таблица состоит из 7 периодов. Первые три периода малые, последние четыре периода большие. Физический смысл номера периода заключается в том, что номер периода соответствует главному квантовому числу или количеству электронных уровней у всех элементов данного периода.
Ёмкость первого энергетического уровня равна двум электронам (N=2), следовательно, первый период состоит из двух элементов:
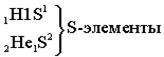
| S-элементами называют элемен- ты, у которых заполняются электронами S-подуровни. |
Ёмкость второго энергетического уровня N = 8. Длина второго периода составляет 8 элементов.
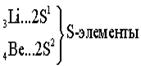
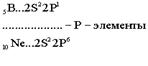
В силу первого закона Клечковского длина и строение третьего периода в точности повторяют второй: два s - элемента, шесть p - элементов. Каждый период начинается с двух s – элементов, которые, за исключением водорода и гелия, являются самыми активными металлами. Каждый период заканчивается активными неметаллами, за исключением благородных газов - химически инертых веществ.
Четвёртый период – первый большой период (18 элементов)
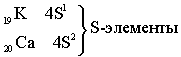
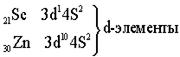
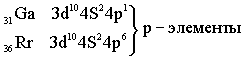
Пятый период. Длина и строение пятого периода в точности повторяет длину и строение четвёртого периода.
Шестой период. Лантан принимает первый электрон на подуровень 5d, затем, в соответствии со вторым законом Клечковского, заполнение электронами подуровня 5d приостанавливается, и начинает заполнятся электронами подуровень 4f.
| 58Сe | 4S1 5S2 5p6 5d1 6S2 | |
| 71Lu | 4f14 5S2 5p6 5d1 6S2 | |
| 72Hf | 5d2 6S2 | После заполнения электронами подуровня 4f продолжается заполнение подуровня 5d, снова появляются d-элементы. |
| 80Hg | 5d10 6S2 |
Заканчивается период шестью p-элементами. Таким образом, 6-й период имеет следующее строение: s – элементы – 2, d – элементы – 1, f – элементы – 14,d – элементы – 9, p – элементы – 6 / Всего 32 элемента. Седьмой период в точности повторяет длину и строение шестого периода. Все трансурановые элементы, начиная с 93Np, являются искусственными. В больших периодах характер изменения свойств элементов тот же, что и в малых, только замедленный. Все s – элементы, кроме Н и Не, - самые активные металлы. Все d и f – элементы тоже металлы, p – элементы частично металлы, частично неметаллы.
Группы периодической таблицы
Таблица Д.И. Менделеева состоит из 8 групп. Физический смысл номера группы заключается в том, что номер группы соответствует валентности входящих в него элементов. Если элемент обладает переменной валентностью, то номер группы соответствует наивысшей валентности данного элемента. Каждая группа делится на главную (А) и побочную (В) подгруппу.
Главная подгруппа содержит элементы и малых, и больших периодов (s и p - элементы). Побочные подгруппы включают в себя d и f – элементы, т.е. элементы только больших периодов. Элементы, составляющие одну подгруппу, имеют близкие химические свойства, т.к. имеют сходные валентные окончания. Химические свойства элементов обуславливаются их валентными окончаниями. Валентное окончание элемента зависит от его положения в таблице Менделеева. Все элементы одной подгруппы имеют одинаковую конфигурацию валентных окончаний, но разные квантовые числа.
С увеличением главного квантового числа у элементов данной подгруппы усиливаются металлические свойства, что обусловлено, в первую очередь, увеличением промежуточных электронных слоёв между ядром атома и его валентным слоем. Элементы, составляющие одну группу, но разные подгруппы, имеют различные валентные окончания и различные химические свойства.
| 17Cl | 3S23p5 | 25Mn | 3d54S1 |
| активный неметалл | металл средней активности |
Элементы, составляющие одну группу, имеют одинаковую валентность. В случае переменности валентности общей является наивысшая валентность.
| 1, 3, 5, 7 | 2, 3, 4, 5,6, 7 |
| +7 | +7 |
| HClO4 | HMnO4 |
| хлорная кислота | марганцовая кислота |
Периодичность изменения свойств элементов.
Следующие свойства элементов являются периодическими:
- металличность и связанная с ней восстановительная способность;
- энергия ионизации;
- неметалличность и связанная с ней окислительная способность;
- сродство к электрону;
- электроотрицательность;
- атомные радиусы.
Свойства, не имеющие периодичности:
- заряд ядра;
- атомная масса.
Периодический характер изменения имеют не только элементы, но и их соединения. Оксиды элементов, расположенных в начале периодов (Li2O; Na2O; MgO), имеют основный характер. Затем идут амфотерные оксиды (BeO, Al2O3). Элементы, расположенные во второй половине, имеют кислотный характер (CO2, NO2, SiO2).
ЛЕКЦИЯ 3
|
|
Дата добавления: 2014-01-07; Просмотров: 560; Нарушение авторских прав?; Мы поможем в написании вашей работы!