
КАТЕГОРИИ:
Архитектура-(3434)Астрономия-(809)Биология-(7483)Биотехнологии-(1457)Военное дело-(14632)Высокие технологии-(1363)География-(913)Геология-(1438)Государство-(451)Демография-(1065)Дом-(47672)Журналистика и СМИ-(912)Изобретательство-(14524)Иностранные языки-(4268)Информатика-(17799)Искусство-(1338)История-(13644)Компьютеры-(11121)Косметика-(55)Кулинария-(373)Культура-(8427)Лингвистика-(374)Литература-(1642)Маркетинг-(23702)Математика-(16968)Машиностроение-(1700)Медицина-(12668)Менеджмент-(24684)Механика-(15423)Науковедение-(506)Образование-(11852)Охрана труда-(3308)Педагогика-(5571)Полиграфия-(1312)Политика-(7869)Право-(5454)Приборостроение-(1369)Программирование-(2801)Производство-(97182)Промышленность-(8706)Психология-(18388)Религия-(3217)Связь-(10668)Сельское хозяйство-(299)Социология-(6455)Спорт-(42831)Строительство-(4793)Торговля-(5050)Транспорт-(2929)Туризм-(1568)Физика-(3942)Философия-(17015)Финансы-(26596)Химия-(22929)Экология-(12095)Экономика-(9961)Электроника-(8441)Электротехника-(4623)Энергетика-(12629)Юриспруденция-(1492)Ядерная техника-(1748)
Последовательные
|
|
|
|
Реакции нулевого порядка
Такой порядок получается при постоянной скорости реакции, что возможно при поддержании постоянной концентрации исходных веществ. Нулевой порядок встречается главным образом в гетерогенных и фотохимических реакциях.
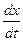 = k, dx = k dt, x = kt + const.
= k, dx = k dt, x = kt + const.
При t = 0 x = 0, следовательно, x = kt.
Лекция 32
Сложные реакции: обратимые, параллельные,
Как уже говорилось ранее, большинство химических реакций состоит из нескольких стадий, называемых элементарными реакциями. Под элементарной реакцией обычно понимают единичный акт образования или разрыва химической связи. Для элементарных реакций общий порядок равен молекулярности, а порядки по веществам равны коэффициентам в уравнении реакции.
Изучение сложных реакций основано на принципе независимости (принципе сосуществования) реакций. Согласно этому принципу, если в системе одновременно протекает несколько реакций, то каждая из них независима от остальных и скорость ее прямо пропорциональна концентрациям реагирующих веществ. Конечное изменение концентрации данного вещества является результатом всех независимых изменений. Этот принцип был проверен экспериментально.
Применение принципа независимости сильно упрощает задачу составления уравнений для скоростей реакций. Однако принцип независимости различных реакций не выполняется, если химические реакции в системе протекают с настолько большими скоростями, что происходит нарушение закона распределения скоростей молекул Максвелла или если в результате образования продуктов реакции сильно изменяются свойства среды.
|
|
|
|
|
Дата добавления: 2014-01-07; Просмотров: 437; Нарушение авторских прав?; Мы поможем в написании вашей работы!