
КАТЕГОРИИ:
Архитектура-(3434)Астрономия-(809)Биология-(7483)Биотехнологии-(1457)Военное дело-(14632)Высокие технологии-(1363)География-(913)Геология-(1438)Государство-(451)Демография-(1065)Дом-(47672)Журналистика и СМИ-(912)Изобретательство-(14524)Иностранные языки-(4268)Информатика-(17799)Искусство-(1338)История-(13644)Компьютеры-(11121)Косметика-(55)Кулинария-(373)Культура-(8427)Лингвистика-(374)Литература-(1642)Маркетинг-(23702)Математика-(16968)Машиностроение-(1700)Медицина-(12668)Менеджмент-(24684)Механика-(15423)Науковедение-(506)Образование-(11852)Охрана труда-(3308)Педагогика-(5571)Полиграфия-(1312)Политика-(7869)Право-(5454)Приборостроение-(1369)Программирование-(2801)Производство-(97182)Промышленность-(8706)Психология-(18388)Религия-(3217)Связь-(10668)Сельское хозяйство-(299)Социология-(6455)Спорт-(42831)Строительство-(4793)Торговля-(5050)Транспорт-(2929)Туризм-(1568)Физика-(3942)Философия-(17015)Финансы-(26596)Химия-(22929)Экология-(12095)Экономика-(9961)Электроника-(8441)Электротехника-(4623)Энергетика-(12629)Юриспруденция-(1492)Ядерная техника-(1748)
Ход работы. Определение содержания азота аммиака
|
|
|
|
Определение содержания азота аммиака
Общие положения
Теоретические сведения
Тесты итогового контроля
1. Предельно допустимая концентрация железа в питьевой воде:
А – 2 мг/л
Б – 0,5 мг/л
В – 0,3 мг/л
Г – 1 мг/л
2. Главными источниками соединений железа в природных водах являются:
А – процессы химического выветривания
Б – сточные воды предприятий
В – коммунальные воды
Г – растворения горных пород
3. Средняя усвояемость железа из продуктов питания составляет около:
А – 10 %
Б – 0,3 %
В – 1 %
Г – 15 %
4. Всасыванию железа способствует:
А – витамин С
Б – витамины группы В,
В – медь и кобальт
Г – жиры
5. Препятствуют усвоению железа:
А – высокое содержание в пище кальция и фосфатов
Б – чай
В – избыток жиров
Г – лимонная кислота
6. Железо входит в состав:
А – нервных клеток
Б – гемоглобина
В – дыхательных ферментов
Г – костной ткани
7. Гемоглобин выполняет функции:
А – транспорта кислорода
Б – запаса питательных веществ
В – защитную
Г – транспорта углекислого газа
8. Резерв железа в организме сосредоточен:
А – в печени
Б – сердечной мышце
В – селезенке
Г – почках
9. Содержание железа в воде определяют колориметрически на основании реакции ионов Fе3+:
А – с роданидом калия
Б – нитритом азота
В – роданидом аммония
Г – хлористым калием
10. Для определения оптической плотности растворов, содержащих ионы железа, используют светофильтр:
А – красный
Б – зеленый
В – синий
Г – желтый
Лабораторная работа № 5
Определение загрязненности воды
по содержанию в ней азотсодержащих
веществ (аммиак, нитриты, нитраты)
с использованием фотометра
фотоэлектрического КФК–3–01–«ЗОМЗ»
Цель работы: освоить методику определения содержания азота аммиака, азота нитритов и азота нитратов в растворах с использованием прибора фотометра фотоэлектрического КФК–3–01–«ЗОМЗ».
Азот необходим всем живым организмам для синтеза азотсодержащих строительных блоков – аминокислот, из которых образуются белки. Сине-зелёные водоросли усваивают газообразный азот из атмосферного воздуха. Растения добывают азот из почвы, в виде растворимых нитратов и соединений аммиака. Содержание азота в организме взрослого человека составляет около 3 % от массы тела.
Азот поступает в организм с пищевыми продуктами, в состав которых входят белки и другие азотсодержащие вещества. Эти вещества расщепляются в желудочно-кишечном тракте и затем всасываются в виде аминокислот и низкомолекулярных пептидов, из которых организм строит собственные аминокислоты и белки. Вместе с тем, организм человека не способен синтезировать некоторые необходимые аминокислоты и получать их с пищей.
Азот (в виде аминогруппы – NH2) входит в состав различных биолигандов, играющих огромную роль в процессах жизнедеятельности. Одним из конечных продуктов метаболизма этих веществ является аммиак NH3. Из организма азот выводится вместе с мочой, калом, выдыхаемым воздухом, а также с потом, слюной.
Физиологическая роль азота в организме ассоциируется, прежде всего, с белками и аминокислотами, их метаболизмом, участием в жизненно-важных процессах и влиянием на эти процессы. Аминокислоты являются исходными соединениями при биосинтезе гормонов, витаминов, медиаторов, пигментов, пуриновых и пиримидиновых оснований и т. д. Белки в пересчёте на сухой вес 44 % от массы тела.
Изменения в содержании белков и аминокислот, расстройства их метаболизма могут быть вызваны различными причинами. Среди этих причин – их недостаточное (или избыточное) поступление, нарушение переваривания и всасывания белка в желудочно-кишечном тракте, расстройство процессов экскреции азота и его соединений.
Функции оксида азота в организме весьма многообразны. NO участвует в поддержании системной и локальной гемодинамики, способствует снижению повышенного тонуса гладкой мускулатуры сосудов и обеспечивает поддержание нормального уровня артериального давления. NO выступает в роли нейротрансмиттера в желудочно-кишечном тракте, мочевыводящей и половой системе, активируя циклический гуанозинмонофосфат (цГМФ). При иммунном ответе NO является стимулятором фагоцитоза и киллинга внутриклеточных паразитов. При сепсисе, под влиянием цитокинов, происходит высвобождение NO в больших количествах, что способствует развитию септического шока. Оксид азота играет важнейшую роль медиатора, в патогенезе бронхиальной астмы, хронического гломерулонефрита, туберкулеза, рассеянного склероза, болезни Крона, различных опухолей, а также СПИДа.
NO участвует в деструкции и метаболизме ферментов, содержащих железо, кобальт, марганец, цинк. Именно благодаря способности NO инактивировать Fe-содержащие ферменты происходит гибель внутриклеточных микроорганизмов, жизнедеятельность которых зависит от присутствия железа и других биоэлементов. Очевидно, что эта функция NO является универсальной и отводит NO решающую роль в элиминации «стареющих» молекул цитохромов, каталазы, гемоглобина.
Азот в форме аммиака и соединений аммония, получающихся в процессах биогенной азотфиксации, быстро окисляется до нитратов и нитритов (этот процесс носит название нитрификации). Последние, не связанные тканями растений (и далее по пищевой цепи травоядными и хищниками), недолго остаются в почве. Большинство нитратов и нитритов хорошо растворимы, поэтому они смываются водой и в конце концов попадают в мировой океан.
Азот, включённый в ткани растений и животных, после их гибели подвергается аммонификации (разложению содержащих азот сложных соединений с выделением аммиака и ионов аммония) и денитрификации, т. е. выделению атомарного азота, а также его оксидов. Эти процессы целиком происходят благодаря деятельности микроорганизмов в аэробных и анаэробных условиях.
Азотсодержащие вещества (аммиак, нитраты, нитриты) образуются в воде главным образом в результате разложения белковых соединений, попадающих в нее с бытовыми сточными водами, а также со сточными водами содовых, коксобензольных, азотнотуковых и других заводов.
Белковые соединения под воздействием микроорганизмов подвергаются разложению, конечным продуктом которого является аммиак. Поэтому наличие его всегда вызывает подозрение о загрязнении воды бытовыми сточными водами. Такая вода не пригодна для питья.
В болотистых и торфяных водах аммиак образуется вследствие гниения растительных остатков, поэтому иногда в воде содержится аммиак растительного или минерального происхождения. В этом случае наличие аммиака в санитарном отношении не опасно. Не опасно оно в санитарном отношении и при попадании аммиака со сточными водами.
Растворенный в воде аммиак при окислении кислородом воздуха под воздействием бактерий Nitrosomonas и Nitrobacter постепенно превращается в азотистую, а затем в азотную кислоту:
2NH3 + 3О2 = 2HNО2 + 2Н2О;
2HNО2 + О2 = 2HNО3.
Первая стадия окисления протекает значительно быстрее, чем вторая. Процесс сильно замедляется с понижением температуры, а при О° С почти прекращается.
По наличию того или иного азотсодержащего вещества можно судить о моменте загрязнения воды: наличие в воде аммиака и отсутствие нитритов свидетельствуют о недавнем загрязнении. Совместное их наличие – о том, что с момента загрязнения прошел некоторый промежуток времени. Отсутствие аммиака при наличии нитритов и особенно нитратов – что загрязнение воды произошло давно, и за это время вода самоочистилась.
По ГОСТу 2874–82 пригодной для питья считается вода, содержащая следы аммиака и азотистой кислоты и не более 30–40 мг/л азотной кислоты.
Азот аммонийный – повышение обычно указывает на свежее загрязнение. Основными источниками поступления в водоёмы ионов аммония являются животноводческие фермы, хозяйственно бытовые сточные воды, сточные воды предприятий пищевой и химической промышленности. Лимитирующий показатель вредности – токсикологический.
Оборудование: бюксы с водой для анализа, химические стаканы, фотометр фотоэлектрический КФК–3–01–«ЗОМЗ» (см. прил. 2), кварцевые кюветы, 50 % раствор сегнетовой соли, реактив Несслера, растворы азота аммиака, колбы.
1. В колбу вместимостью 100 мл наливают 50 мл исследуемой воды, 1 мл 50 %-го раствора сегнетовой соли и 1 мл реактива Несслера, смесь тщательно перемешивают.
2. Через 10 мин определяют оптическую плотность раствора в кювете на фотометре КФК с толщиной поглощающего слоя 30 мм при синем светофильтре № 4.
3. Затем определяют оптические плотности D1ст и D2ст стандартных растворов с концентрацией азота аммиака 0,1 и 0,2 мг/л, к которым прибавлены такие же реактивы.
4. Содержание азота аммиака Храссчитывают по формуле
X = 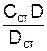 , (1)
, (1)
используя данные для двух стандартных растворов.
5. Затем определяют среднее значение содержания азота аммиака в растворе.
Отчет о работе: представить тетрадь с рассчитанными показателями содержания азота аммиака в исследуемых водоемах.
|
|
|
|
|
Дата добавления: 2014-11-06; Просмотров: 1381; Нарушение авторских прав?; Мы поможем в написании вашей работы!