
КАТЕГОРИИ:
Архитектура-(3434)Астрономия-(809)Биология-(7483)Биотехнологии-(1457)Военное дело-(14632)Высокие технологии-(1363)География-(913)Геология-(1438)Государство-(451)Демография-(1065)Дом-(47672)Журналистика и СМИ-(912)Изобретательство-(14524)Иностранные языки-(4268)Информатика-(17799)Искусство-(1338)История-(13644)Компьютеры-(11121)Косметика-(55)Кулинария-(373)Культура-(8427)Лингвистика-(374)Литература-(1642)Маркетинг-(23702)Математика-(16968)Машиностроение-(1700)Медицина-(12668)Менеджмент-(24684)Механика-(15423)Науковедение-(506)Образование-(11852)Охрана труда-(3308)Педагогика-(5571)Полиграфия-(1312)Политика-(7869)Право-(5454)Приборостроение-(1369)Программирование-(2801)Производство-(97182)Промышленность-(8706)Психология-(18388)Религия-(3217)Связь-(10668)Сельское хозяйство-(299)Социология-(6455)Спорт-(42831)Строительство-(4793)Торговля-(5050)Транспорт-(2929)Туризм-(1568)Физика-(3942)Философия-(17015)Финансы-(26596)Химия-(22929)Экология-(12095)Экономика-(9961)Электроника-(8441)Электротехника-(4623)Энергетика-(12629)Юриспруденция-(1492)Ядерная техника-(1748)
Контроль усвоения темы занятия. Узловые вопросы, необходимые для усвоения темы занятия
|
|
|
|
Лабораторная работа
Узловые вопросы, необходимые для усвоения темы занятия
Типовой билет входного контроля
1. Общее определение кислот Бренстеда;
1) содержат карбоксильную группу;
2) окрашивают лакмус в красный цвет;
3) отщепляют протон в присутствии оснований;
4) взаимодействуют с растворами щелочей.
2. Установите соответствие:
Кислота Формула
1) ОН-кислота Бренстеда А) СН3СООН В) С2H5SC2H5
2) кислота Льюиса Б) FeCl3 Г) C2H5Br
3. Наиболее сильная кислота в растворе
1) СН3ОН;
2) С2Н5ОН;
3) (СН3)2СНОН;
4) Н2О.
4. Факторы, оказывающие влияние на стабильность сопряженных оснований (анионов)
1) влияние растворителя;
2) электронные эффекты заместителей;
3) электроотрицательность элемента в кислотном центре;
4) стабилизация аниона за счет сопряжения.
5. Соединения, образующие межмолекулярные водородные связи
1) С6Н13ОН;
2) С6Н5SН;
3) СН3СН2ОСН3;
4) СН3СН2СООН.
1. Кислотность органических соединений по Бренстеду-Лоури (ОН, SH, NH, CH-кислоты). Примеры.
2. Основность органических соединений по Бренстеду-Лоури (аммониевые, оксониевые, сульфониевые и p-основания).
3. Кислотность и основность по Льюису.
4. Принцип жестких и мягких кислот и оснований (ЖМКО).
Опыт 1. Образование фенолята натрия и разложение его кислотой
В пробирку поместите несколько капель воды, кристалл фенола и встряхните. К возникшей мутной эмульсии добавьте по каплям 10% раствор гидроксида натрия до образования прозрачного раствора. Напишите уравнение реакции получения фенолята натрия. Добавьте несколько капель соляной кислоты к раствору фенолята натрия. Что при этом наблюдается? Напишите уравнение происходящей реакции.
Опыт 2. Основность алифатических и ароматических аминов
|
|
|
В две пробирки внесите по 2 капли воды. Затем в первую поместите каплю анилина, а во вторую – каплю диэтиламина, и взболтайте. Сравните растворимость этих аминов в воде. По 1 капле содержимого каждой пробирки нанесите на полоску универсальной индикаторной бумаги или красного лакмуса. Определите рН растворов анилина и диэтиламина.
Образец билета выходного контроля
1. Дайте определение понятий «кислотность» и «основность» по Бренстеду-Лоури.
2. Расположите следующие спирты в ряд по уменьшению кислотности: метиловый, трет -бутиловый, изопропиловый. Обоснуйте свой ответ, основываясь на стабильности соответствующих анионов.
Вопросы и упражнения для аудиторной работы
1. Расположите в ряд по уменьшению кислотности следующие соединения:
а) этанол, этантиол, этиламин;
б) фенол, п -нитрофенол, п -аминофенол;
в) этанол, пропанол-2, метанол, 2-метилпропанол-2.
Обоснуйте решение, исходя из стабильности анионов.
2. Глицерин взаимодействует с гидроксидом меди (II), а пропанол-1 – нет. Дайте объяснение различию в кислотности и напишите схему реакции.
3. Сравните основность каждой из следующих групп соединений:
а) аммиак, анилин, дифениламин, трифениламин;
б) анилин, п -аминофенол, п -аминобензойная кислота;
4. Чем больше основность простых эфиров, тем легче они расщепляются под действием сильных минеральных кислот. Какое соединение расщепляется легче – диэтиловый эфир или фенилэтиловый эфир (фенетол)?
5. Укажите в молекуле α-аминокислоты тирозине кислотные центры и определите порядок уменьшения их кислотности.
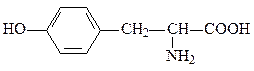
6. В качестве первого антидота при отравлениях соединениями мышьяка был предложен 2,3-димеркаптопропанол. Какие кислотные центры в его молекуле преимущественно участвуют в образовании солей мышьяка?
7. Ощущение сладкого вкуса возникает при одновременном наличии в соединении слабых кислотного и основного центров, находящихся на определенном расстоянии друг от друга и образующих водородные связи с вкусовыми рецепторами. Укажите кислотные и основные центры в молекуле 5-нитро-2-пропоксианилина, который слаще свекловичного сахара в 3100 раз.
|
|
|
7.5 Подведение итогов занятия
7.6 Задание на дом: Биологически важные реакции карбонильных соединений
Место проведения самоподготовки: читальный зал и др.
Литература: [1], [2], [3].
Занятие №4
Биологически важные реакции карбонильных соединений
1. Актуальность темы. Альдегиды и кетоны(карбонильные соединения) широко распространены в природе, многие используются при синтезе лекарственных средств и лечебных препаратов (ретиналь, камфора). Изучение механизмов нуклеофильного присоединения в оксосоединениях дает возможность прогнозировать химические превращения альдегидов и кетонов в организме человека. Так, имины (продукты взаимодействия аминов с альдегидами и кетонами) являются промежуточными продуктами во многих ферментативных процессах, например в биосинтезе α-аминокислот.
2. Учебные цели. Сформировать знания о биологически важных реакциях карбонильных соединений.
3. Материалы для самоподготовки к усвоению данной темы.
Вопросы для самоподготовки
1. Электронное строение карбонильной группы.
2. Реакционные центры в молекулах альдегидов и кетонов.
3. Химические свойства альдегидов и кетонов: присоединение спиртов, тиолов, воды, циановодородной кислоты, аминов, гидразинов и их производных.
4. Реакции конденсации, общий механизм альдольного присоединения. Кротоновая конденсация.
5. Окисление альдегидов гидроксидом диамминсеребра и гидроксидом меди (II). Восстановление альдегидов и кетонов гидридами металлов
6. Реакции диспропорционирования (Канниццаро).
4. Вид занятия: практическое занятие.
5. Продолжительность занятия: 2 академических часа.
6. Оснащение рабочего места:
6.1Посуда и приборы:
| Штатив с пробирками, пипетки, спиртовка, спички, держатель для пробирок. | на группу |
6.2. Объекты исследования:
| Формалин, 1% раствор ацетона. | на группу |
6.3. Реактивы:
| 10% Раствор NaOH, 0,2% раствор CuSO4, разбавленный раствор нитропруссида натрия, раствор йода. | на группу |
7. Содержание занятия
|
|
|
|
|
|
|
|
Дата добавления: 2014-10-31; Просмотров: 1247; Нарушение авторских прав?; Мы поможем в написании вашей работы!