
КАТЕГОРИИ:
Архитектура-(3434)Астрономия-(809)Биология-(7483)Биотехнологии-(1457)Военное дело-(14632)Высокие технологии-(1363)География-(913)Геология-(1438)Государство-(451)Демография-(1065)Дом-(47672)Журналистика и СМИ-(912)Изобретательство-(14524)Иностранные языки-(4268)Информатика-(17799)Искусство-(1338)История-(13644)Компьютеры-(11121)Косметика-(55)Кулинария-(373)Культура-(8427)Лингвистика-(374)Литература-(1642)Маркетинг-(23702)Математика-(16968)Машиностроение-(1700)Медицина-(12668)Менеджмент-(24684)Механика-(15423)Науковедение-(506)Образование-(11852)Охрана труда-(3308)Педагогика-(5571)Полиграфия-(1312)Политика-(7869)Право-(5454)Приборостроение-(1369)Программирование-(2801)Производство-(97182)Промышленность-(8706)Психология-(18388)Религия-(3217)Связь-(10668)Сельское хозяйство-(299)Социология-(6455)Спорт-(42831)Строительство-(4793)Торговля-(5050)Транспорт-(2929)Туризм-(1568)Физика-(3942)Философия-(17015)Финансы-(26596)Химия-(22929)Экология-(12095)Экономика-(9961)Электроника-(8441)Электротехника-(4623)Энергетика-(12629)Юриспруденция-(1492)Ядерная техника-(1748)
Соединения с
|
|
|
|
Химические свойства С
Получение С
| |||
 | |||
| С – окислитель | С – восстановитель |
| 1) 4Al + 3C = Al4C3 (карбид Al) 2) CaO + 3C = CO + CaC2 (карбид кальция) 3) Ca + 2C = CaC2 4) 2H2 + C =CH4 | 1) C + O2 = CO2 ниже 500˚С 2С + O2 = 2CO выше 900˚С 2) C + H2O = CO + H2 выше 1200˚С C+2H2O= CO2 + 2H2 ниже 1000˚С 3) C+2ZnO=2Zn+ CO2 (Cu, Fe, Pb…) 4) 3C+4HNO3 = 3CO2 + 4NO + 2H2O |
| Оксид углерода (II):С=О: | Оксид углерода (VI) O=С=О |
| I. Получение. 1) В промышленности СО2 +С = 2СО 2) В лаборатории HCOOH=H2O+CO↑ II. Физические свойства:газ без цвета и запаха, очень ядовитый, так как соединяется с гемоглобином крови, плохо растворим в воде. III. Химические свойства: CO – восстановитель. 1) CO + CuO = Cu + CO2 2) 2CO + O2 = 2CO2 ΔH = -572 кДж – горит синим пламенем | I. Получение.
1) В промышленности
CaСО3 = CaO + СО2↑
2) В лаборатории
CaСО3+2HCl=CaCl2+CO2↑+ H2O
II. Физические свойства:
бесцветный газ, тяжелее воздуха, не поддерживает дыхание; растворим в воде, при t = –76˚С – сухой лед.
III. Химические свойства:
1) CO2 – кислый оксид.
а) CO2 + H2O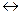 H2CO3
б) CO2 + 2NaOH = Na2CO3 + H2O
2) CO2 – окислитель
а) CO2 + С = 2СО
б) CO2 + 2Mg = 2MgO + C
IV. Применение: в производстве соды, сахара, газированных напитков; в жидком виде – в огнетушителях; сухой лед – для хранения продуктов. H2CO3
б) CO2 + 2NaOH = Na2CO3 + H2O
2) CO2 – окислитель
а) CO2 + С = 2СО
б) CO2 + 2Mg = 2MgO + C
IV. Применение: в производстве соды, сахара, газированных напитков; в жидком виде – в огнетушителях; сухой лед – для хранения продуктов.
|
| Угольная кислота H2CO3 | |
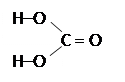 Существует только в растворе, в свободном виде не устойчив, слабый электролит.
H2CO3 = CO2↑ + 2H2О – при нагревании
Диссоциация:
H2CO3
Существует только в растворе, в свободном виде не устойчив, слабый электролит.
H2CO3 = CO2↑ + 2H2О – при нагревании
Диссоциация:
H2CO3 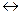 H+ + H+ + 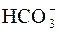
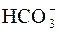 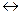 H+ + H+ + 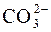
|
| Соли угольной кислоты | |
| Карбонаты | Гидрокарбонаты |
Карбонаты щелочных металлов и 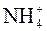 растворимы в воде; щелочноземельных металлов – мало растворимы.
CaCO3 растворимы в воде; щелочноземельных металлов – мало растворимы.
CaCO3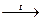 CaO + CO2↑ CaO + CO2↑
| Гидрокарбонаты щелочных, щелочноземельных металлов и 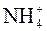 растворимы в воде.
Получение:
CaCO3+ СО2 + Н2О = Ca(НCO3)2
Ca(НCO3)2 растворимы в воде.
Получение:
CaCO3+ СО2 + Н2О = Ca(НCO3)2
Ca(НCO3)2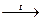 CaCO3+ СО2↑ + Н2О CaCO3+ СО2↑ + Н2О
|
| Na2CO3 – карбонат натрия: белый порошок; используется в производстве стекла, мыла, бумаги, моющих средств. K2CO3– поташ: белый порошок; используется в производстве жидкого мыла, оптического стекла пигментов. СaCO3 – мел, мрамор, известняк; используется в строительстве. | NaНCO3 – гидрокарбонат натрия или питьевая сода: белый порошок, плохо растворяется в воде; используется в пищевой промышленности, медицине. |
| Качественная реакция на карбонат-ион: 1) CaCO3+2НСl = СО2↑ + CaCl2 + Н2О – «вскипание» за счет выделения СО2, далее 2) пропускаем СО2 через Ca(OH)2: Ca(OH)2 + СО2 = CaCO3↓ + Н2О – раствор мутнеет 3) при избытке СО2: CaCO3+СО2+Н2О=Ca(НCO3)2 – помутнение исчезает. |
|
|
|
|
|
Дата добавления: 2014-10-31; Просмотров: 348; Нарушение авторских прав?; Мы поможем в написании вашей работы!