
КАТЕГОРИИ:
Архитектура-(3434)Астрономия-(809)Биология-(7483)Биотехнологии-(1457)Военное дело-(14632)Высокие технологии-(1363)География-(913)Геология-(1438)Государство-(451)Демография-(1065)Дом-(47672)Журналистика и СМИ-(912)Изобретательство-(14524)Иностранные языки-(4268)Информатика-(17799)Искусство-(1338)История-(13644)Компьютеры-(11121)Косметика-(55)Кулинария-(373)Культура-(8427)Лингвистика-(374)Литература-(1642)Маркетинг-(23702)Математика-(16968)Машиностроение-(1700)Медицина-(12668)Менеджмент-(24684)Механика-(15423)Науковедение-(506)Образование-(11852)Охрана труда-(3308)Педагогика-(5571)Полиграфия-(1312)Политика-(7869)Право-(5454)Приборостроение-(1369)Программирование-(2801)Производство-(97182)Промышленность-(8706)Психология-(18388)Религия-(3217)Связь-(10668)Сельское хозяйство-(299)Социология-(6455)Спорт-(42831)Строительство-(4793)Торговля-(5050)Транспорт-(2929)Туризм-(1568)Физика-(3942)Философия-(17015)Финансы-(26596)Химия-(22929)Экология-(12095)Экономика-(9961)Электроника-(8441)Электротехника-(4623)Энергетика-(12629)Юриспруденция-(1492)Ядерная техника-(1748)
ОПЫТ 5. Изучение влияния температуры на положение равновесия в гомогенной системе
|
|
|
|
Опыт 4. Изучение влияния концентраций веществ на положение химического равновесия
ОПЫТ 3. Изучение влияния сульфата меди(II) на скорость восстановления роданида железа(III).
В данном опыте вы изучите влияние сульфата меди(II) на скорость реакции восстановления роданида железа(III) тиосульфатом натрия:
2Fe(NCS)3 + 2Na2S2O3 = 2Fe(NCS)2 + 2NaNCS + Na2S4O6.
Окончанию данной реакции соответствует полное обесцвечивание раствора.
Выполнение:
Приготовьте исходный раствор роданида железа(III), смешав в пробирке примерно по 2 см3 разбавленных растворов FeCl3 и KNCS:
FeCl3 + 3KNCS ↔ Fe(NCS)3 + 3KCl.
Полученный раствор разделите на 2 части (в 2-х пробирках).
В первую пробирку с раствором роданида железа(III) добавьте 1 каплю раствора тиосульфата натрия, содержимое пробирки перемешайте. Обратите внимание на скорость обесцвечивания раствора.
В другую пробирку с раствором роданида железа(III) добавьте 1 каплю очень разбавленного раствора сульфата меди(II), а затем 1 каплю раствора тиосульфата натрия. Содержимое пробирки перемешайте. Что наблюдается?
Задания: Запишите наблюдаемые эффекты. Какова роль сульфата меди(II) в процессе восстановления роданида железа(III) тиосульфатом натрия? Сделайте вывод о влиянии катализаторов на скорость химических реакций.
В этом опыте вы изучите влияние концентраций исходных веществ и продуктов на положение химического равновесия в гомогенной системе:
FeCl3 + 3KNCS ↔ Fe(NCS)3 + 3KCl.
Смещению данного равновесия вправо соответствует усиление окраски раствора, а смещению влево – её ослабление.
Выполнение:
Приготовьте гомогенную равновесную систему, смешав в пробирке примерно по 2 см3 разбавленных растворов FeCl3 и KNCS. Полученный раствор разделите на 3 части (в пробирках). Одну из них оставьте в качестве контрольной.
|
|
|
В первую пробирку добавьте 1 каплю насыщенного раствора KNCS, во вторую – 2–3 шпателя кристаллов KCl. Содержимое пробирок перемешайте и сравните интенсивность окраски в них с интенсивностью в контрольной пробирке.
Задания:
Запишите наблюдаемые эффекты и объясните их. Сделайте вывод о направлении смещения равновесия при изменении концентраций исходных веществ и продуктов реакции. Запишите выражение константы химического равновесия изученного процесса.
В этом опыте вы изучите влияние температуры на положение равновесия процесса
2NO2 (г) ↔ N2O4 (г) + Q.
Смещению равновесия влево соответствует усиление бурой окраски газа, а вправо – ее ослабление.
Выполнение:
Одну из сообщающихся колб, наполненных смесью оксидов NO2 и N2O4, опустите в стакан с охладительной смесью (NaCl + лёд), а другую – в стакан с горячей водой. Через 1 – 2 минуты сравните интенсивность окраски газа в колбах. Теперь поменяйте колбы местами: охлажденную колбу опустите в стакан с горячей водой, а нагретую – в стакан с охладительной смесью. Наблюдайте за изменением интенсивности окраски газа в колбах.
Задания:
Запишите наблюдаемые явления и объясните их. Сделайте вывод о влиянии температуры на положение химического равновесия. Запишите выражение константы химического равновесия изученного процесса. Пользуясь справочными данными, определите температурные условия осуществления прямой реакции.
Когда и что сделать?
Дома перед занятием:
1. Изучите содержание лабораторной работы, подготовьтесь к опросу по данному материалу.
2. В тетради для лабораторных работ сделайте заготовку отчёта о выполнении работы. В начале отчёта укажите дату, номер работы и её название. После этого перепишите в тетрадь названия и методики выполнения опытов из вышеприведенной «Экспериментальной части», оставляя места для записи наблюдений, объяснений, расчётов, ответов на вопросы и выводов.
|
|
|
На занятии:
3. Выполните экспериментальную часть работы, строго следуя инструкции и тщательно записывая промежуточные результаты в отчёт.
4. Уберите своё рабочее место.
Дома после занятия:
5. Выполните необходимые расчёты и запишите их в отчёт. Постройте график.
6. Ответьте письменно в тетради для лабораторных работ на контрольные вопросы:
а) Дайте определение скорости гомогенной химической реакции. Каковы её физический смысл и единицы?
б) Перечислите факторы, влияющие на величину скорости химических реакций.
в) Какова зависимость скорости химических реакций от концентраций реагентов? Как называется соответствующий закон, определяющий эту зависимость? Как он формулируется?
г) Какова зависимость скорости химических реакций от температуры? Каков физический смысл коэффициента скорости реакции? От каких факторов зависит его величина?
д) Что такое катализаторы? Какие вещества могут выступать в роли катализаторов? Как можно объяснить их влияние на скорость реакций?
е) Какое состояние системы называется химическим равновесием? Сформулируйте принцип Ле Шателье.
ж) Каково влияние концентраций исходных веществ и продуктов реакции на состояние химического равновесия в системе?
з) Каково влияние температуры на состояние химического равновесия в гомогенной системе?
=======================================================================
ЛАБОРАТОРНАЯ РАБОТА № 4
«Приготовление раствора кислоты с заданным
значением молярной концентрации эквивалентов и определение её точного значения методом титрования»
Т е о р е т и ч е с к а я ч а с т ь
Молярная концентрация эквивалентов вещества в объёмном анализе. Титрование.
Молярная концентрация эквивалентов вещества Х – величина, равная отношению химического количества эквивалентов вещества Х к объёму раствора:
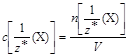 .
.
Она показывает, какое химическое количество эквивалентов вещества Х содержится в растворе объёмом 1 дм3. Например, запись 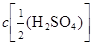 = 0,2 моль/дм3 обозначает, что в данном растворе объёмом 1 дм3 количество эквивалентов серной кислоты равно 0,2 моль. Часто молярную концентрацию эквивалента называют эквивалентной концентрацией и обозначают символом «с э». Раньше её называли нормальной концентрацией (или нормальностью) и обозначили символами «н» или «N».
= 0,2 моль/дм3 обозначает, что в данном растворе объёмом 1 дм3 количество эквивалентов серной кислоты равно 0,2 моль. Часто молярную концентрацию эквивалента называют эквивалентной концентрацией и обозначают символом «с э». Раньше её называли нормальной концентрацией (или нормальностью) и обозначили символами «н» или «N».
|
|
|
Согласно закону эквивалентов, вещества X и Y реагируют в таком соотношении, что количество эквивалентов вещества Х всегда равно количеству эквивалентов вещества Y, т. е.:
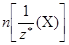 =
=  .
.
Поскольку 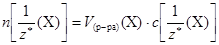 , а
, а 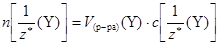 ,
,
то можно записать: 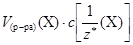 =
= 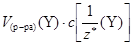
или в упрощенном виде:
| V р-ра(Х) × с э(Х) = V р-ра(Y) × с э(Y) |
Из этого уравнения видно, что при одинаковых концентрациях эквивалентов реагирующих веществ X и Y объёмы их растворов будут также одинаковыми. Так, например, для нейтрализации серной кислоты, содержащейся в растворе объёмом 50 см3 с концентрацией её эквивалентов, равной 0,1 моль/дм3, требуется такой же объём раствора гидроксида натрия с концентрацией его эквивалентов, равной 0,1 моль/дм3. Если же молярные концентрации эквивалентов веществ X и Y не равны между собой, то их отношение обратно пропорционально отношению объёмов растворов этих веществ:
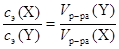
|
Это уравнение позволяет рассчитать значение эквивалентной концентрации вещества Х, если известно значение концентрации реагирующего с ним вещества Y. Данный тип расчетов очень широко используется в аналитической химии и лежит в основе метода объёмного анализа, основанного на измерении объёмов растворов реагирующих веществ.
На практике для определения эквивалентной концентрации веществ используют метод титровáния (от франц. «titre» – количество). Он заключается в том, что к определённому объёму раствора с неизвестной эквивалентной концентрацией вещества Х постепенно добавляют раствор с известной концентрацией вещества Y до момента окончания реакции, которому соответствует изменение окраски индикатора. Определив таким образом точный объём добавленного раствора вещества Y, рассчитывают эквивалентную концентрацию вещества Х в исходном растворе.
Пример 1.
На титрование раствора гидроксида калия объемом 10,0 см3 израсходован раствор объемом 12,8 см3 с эквивалентной концентрацией серной кислоты, равной 0,1200 моль/дм3. Вычислить эквивалентную концентрацию щёлочи в исходном растворе.
|
|
|
Решение:
Из уравнения V (кисл) × с э(кисл) = V (щёл) × с э(щёл)
выразим искомую концентрацию и найдем её значение:
с э(щёл) = 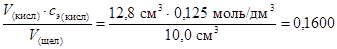 моль/дм3.
моль/дм3.
При приготовлении растворов с заданными значениями молярной концентрации эквивалентов необходимо помнить, что молярная масса эквивалента одного и того же вещества может иметь разные значения в зависимости от того, в какой реакции это вещество будет участвовать. Например, для реакции H2SO4 + NaOH ® NaHSO4 + H2O эквивалентом кислоты является её молекула и молярная масса эквивалентов равна 98 г/моль. В случае же другой реакции: H2SO4 + 2NaOH ® Na2SO4 + 2H2O эквивалентом кислоты является половина её молекулы и молярная масса эквивалентов в этом случае составляет:
M 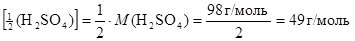 .
.
Э к с п е р и м е н т а л ь н а я ч а с т ь
ОПЫТ 1. Определение плотности исходного раствора и массовой доли кислоты в нём
Для быстрого определения плотности растворов используют специальные приспособления – ареόметры. Ареόметр представляет собой изготовленный в виде поплавка стеклянный сосуд со шкалой, градуированный в единицах плотности (кг/м3) (рис. 1).
 |
Выполнение:
1) Исходный раствор кислоты налейте в сухой цилиндр на 2/3 его объема. Осторожно опустите в этот раствор ареометр и следите за тем, чтобы он не касался дна и стенок цилиндра, а нижний мениск жидкости в цилиндре располагался бы в пределах шкалы ареометра (рис. 2).
 | |||
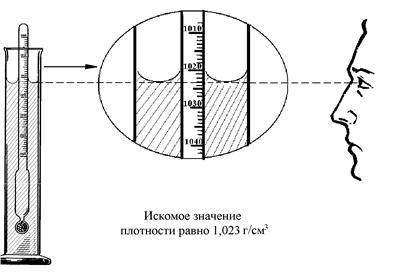 | |||
2) После того, как покачивания ареометра прекратятся, определите значение плотности, соответствующее нижнему мениску раствора, произведя отсчет по шкале ареометра сверху вниз. Запишите в отчет найденное значение. После этого аккуратно извлеките ареометр из раствора, промойте водопроводной водой, вытрите досуха фильтровальной бумагой и поместите в футляр.
3) Запишите найденное значение плотности в отчёт.Используя справочную таблицу 1, определите массовую долю кислоты, соответствующую найденному значению плотности.
Таблица 1.
Массовые доли кислот и соответствующие им значения плотности растворов (г/см3).
| Массовая доля кислоты, (%) | Плотность растворов кислот, г/см3 (20 оС) | ||
| H2SO4 | HNO3 | HCl | |
| 1,040 | 1,033 | 1,029 | |
| 1,045 | 1,037 | 1,037 | |
| 1,052 | 1,044 | 1,039 | |
| 1,059 | 1,049 | 1,043 | |
| 1,066 | 1,056 | 1,049 | |
| 1,080 | 1,068 | 1,059 | |
| 1,098 | 1,080 | 1,069 | |
| 1,112 | 1,093 | 1,079 | |
| 1,127 | 1,106 | 1,083 | |
| 1,143 | 1,119 | 1,100 | |
| 1,158 | 1,132 | 1,110 | |
| 1,174 | 1,145 | 1,121 | |
| 1,190 | 1,158 | 1,132 | |
| 1,205 | 1,171 | 1,142 | |
| 1,224 | 1,184 | 1,152 |
Если в таблице нет значения плотности, совпадающего с найденным, то искомую массовую долю кислоты определите методом интерполяции. Для этого используйте 2 ближайших табличных значения плотности, одно из которых больше, а другое меньше найденного вами значения. (При этом допускается, что в выбранном интервале значений плотности зависимость массовой доля вещества от плотности раствора является линейной). Рассмотрим конкретный пример.
Пример 2.
Определим с помощью справочной таблицы массовую долю серной кислоты в растворе с плотностью, равной 1,200 г/см3, если в таблице приведены значения плотности, равные 1,190 г/см3 и 1,205 г/см3, которым соответствуют массовые доли кислоты 26 % и 28 %.
Решение:
а) Находим разность между бóльшим и меньшим табличными значениями плотности, ближайшими к значению 1,200 г/см3:
Dr = r(больш) – r(меньш) = 1,205 – 1,190 = 0,015.
б) Находим разность между табличными значениями массовых долей кислоты, соответствующими данным значениям плотности:
D w = w (больш) – w (меньш) = 28 % – 26 % = 2 %.
в) Находим разность между измеренным значением плотности и меньшим её табличным значением:
Dr1 = r(измер) – r(меньш) = 1,200 – 1,190 = 0,010.
г) Составим пропорцию и находим значение D w 1, соответствующее найденному значению Dr1 :
если Dr = 0,015, то D w = 2 %,
если Dr1 = 0,010, то D w 1 = х %,
откуда х = 1,3 %.
д) Находим искомое значение массовой доли кислоты, добавив найденное D w 1 к меньшему табличному значению массовой доли:
w (кисл) = 26 % + 1,3 % = 27,3 %.
По приведенному образцу рассчитайте массовую долю кислоты в приготовленном растворе и запишите её в отчёт.
|
|
|
|
|
Дата добавления: 2014-11-25; Просмотров: 2587; Нарушение авторских прав?; Мы поможем в написании вашей работы!