
КАТЕГОРИИ:
Архитектура-(3434)Астрономия-(809)Биология-(7483)Биотехнологии-(1457)Военное дело-(14632)Высокие технологии-(1363)География-(913)Геология-(1438)Государство-(451)Демография-(1065)Дом-(47672)Журналистика и СМИ-(912)Изобретательство-(14524)Иностранные языки-(4268)Информатика-(17799)Искусство-(1338)История-(13644)Компьютеры-(11121)Косметика-(55)Кулинария-(373)Культура-(8427)Лингвистика-(374)Литература-(1642)Маркетинг-(23702)Математика-(16968)Машиностроение-(1700)Медицина-(12668)Менеджмент-(24684)Механика-(15423)Науковедение-(506)Образование-(11852)Охрана труда-(3308)Педагогика-(5571)Полиграфия-(1312)Политика-(7869)Право-(5454)Приборостроение-(1369)Программирование-(2801)Производство-(97182)Промышленность-(8706)Психология-(18388)Религия-(3217)Связь-(10668)Сельское хозяйство-(299)Социология-(6455)Спорт-(42831)Строительство-(4793)Торговля-(5050)Транспорт-(2929)Туризм-(1568)Физика-(3942)Философия-(17015)Финансы-(26596)Химия-(22929)Экология-(12095)Экономика-(9961)Электроника-(8441)Электротехника-(4623)Энергетика-(12629)Юриспруденция-(1492)Ядерная техника-(1748)
Далее для определения частного порядка реакции (или общего порядка, если в реакции участвует только одно вещество) используют один из описанных ниже методов
|
|
|
|
После интегрирования получим
k 11 = 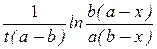 (14)
(14)
Методы определения порядка реакции
1) Метод изоляции или метод избытка
Если в исследуемой реакции участвуют несколько реагирующих веществ, то общий порядок реакции равен сумме частных (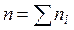 ). Частный порядок ni можно определить, взяв все вещества, кроме данного, в большом избытке. Так, в случае реакции
). Частный порядок ni можно определить, взяв все вещества, кроме данного, в большом избытке. Так, в случае реакции
А + В + С ® D
для определения порядка nA вещества В и С берут в таком большом избытке, чтобы их концентрации практически не изменялась
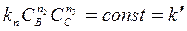 (15)
(15)
Тогда скорость реакции зависит только от концентрации А
W = 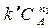 (16)
(16)
Так последовательно «выделяют» порядок реакции по каждому из реагирующих веществ.
2) Метод подстановки
Опытные результаты - текущие концентрации веществ Сi в моменты времени ti - последовательно подставляют в интегральные кинетические уравнения реакций нулевого, первого, второго порядков и определяют, какое из уравнений дает практически постоянную величину константы скорости. Именно это уравнение и определяет порядок исследуемой реакции.
Графический вариант метода подстановки предполагает построение линейных графиков в координатах f(C) - t,причем вид функции f(C) определяется порядком реакции.
3) Определение порядка реакции по времени полупревращения
Для определения порядка реакции необходимо провести хотя бы два опыта с различными начальными концентрациями -  и
и 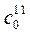 .
.
|
|
|
|
|
Дата добавления: 2014-11-16; Просмотров: 432; Нарушение авторских прав?; Мы поможем в написании вашей работы!