
КАТЕГОРИИ:
Архитектура-(3434)Астрономия-(809)Биология-(7483)Биотехнологии-(1457)Военное дело-(14632)Высокие технологии-(1363)География-(913)Геология-(1438)Государство-(451)Демография-(1065)Дом-(47672)Журналистика и СМИ-(912)Изобретательство-(14524)Иностранные языки-(4268)Информатика-(17799)Искусство-(1338)История-(13644)Компьютеры-(11121)Косметика-(55)Кулинария-(373)Культура-(8427)Лингвистика-(374)Литература-(1642)Маркетинг-(23702)Математика-(16968)Машиностроение-(1700)Медицина-(12668)Менеджмент-(24684)Механика-(15423)Науковедение-(506)Образование-(11852)Охрана труда-(3308)Педагогика-(5571)Полиграфия-(1312)Политика-(7869)Право-(5454)Приборостроение-(1369)Программирование-(2801)Производство-(97182)Промышленность-(8706)Психология-(18388)Религия-(3217)Связь-(10668)Сельское хозяйство-(299)Социология-(6455)Спорт-(42831)Строительство-(4793)Торговля-(5050)Транспорт-(2929)Туризм-(1568)Физика-(3942)Философия-(17015)Финансы-(26596)Химия-(22929)Экология-(12095)Экономика-(9961)Электроника-(8441)Электротехника-(4623)Энергетика-(12629)Юриспруденция-(1492)Ядерная техника-(1748)
Основные формулы. 160. Найти внутреннюю энергию массы 20 г кислорода при температуре 10оС
|
|
|
|
ЗАДАЧИ
160. Найти внутреннюю энергию массы 20 г кислорода при температуре 10оС. Какая часть этой энергии приходится на долю поступательного движения молекул и какая часть на долю вращательного движения?
[3,7 кДж]
161. Энергия поступательного движения молекул азота, находящегося в баллоне объемом 20 л, 5 кДж, а средняя квадратичная скорость его молекул 2Ч103м/с. Найти массу азота в баллоне и давление, под которым он находится.
[2,5 г; 167 кПа]
162. Масса 1 кг двухатомного газа находится под давлением 80 кПа и имеет плотность 4 кг/м3. Найти энергию теплового движения молекул газа при этих условиях.
[50 кДж]
163. Какое число молекул двухатомного газа содержит объем 10 см3 при давлении 5,3 кПа и температуре 27оС? Какой энергией теплового движения обладают эти молекулы?
[1,3×1019; 0,133 Дж]
164. Найти удельную теплоемкость c кислорода для: а) V = const; б) p = const.
[650; 910 Дж/кг×К]
165. Найти удельную теплоемкость при постоянном давлении: а) хлористого водорода; б) неона; в) окиси азота; г) окиси углерода; д) паров ртути.
[800; 1025; 970; 1040;103 Дж/кг×К]
166. Найти удельную теплоемкость при постоянном давлении газовой смеси, состоящей из 3 кмоль аргона и 2 кмоль азота.
[847 Дж/кг×К]
167. Найти отношение c p/ cV для газовой смеси, состоящей из 8 г гелия и 16 г кислорода.
[1,59]
168. Удельная теплоемкость газовой смеси, состоящей из 1 кмоль кислорода и некоторой массы аргона, c p = 430 Дж/(кгЧК). Какая масса аргона находится в газовой смеси?
[35,7 кг]
169. 10 г кислорода находится при давлении 300 кПа и температуре 10оС. После нагревания при постоянном давлении газ занял объем 10 л. Найти количество теплоты, полученной газом, изменение внутренней энергии газа и работу, совершенную газом при расширении.
|
|
|
[7,9 кДж; 5,6 кДж; 2,3 кДж]
170. 12 г азота находится в закрытом сосуде объемом 2 л при температуре 10оС. После нагревания давление в сосуде стало равным 1,33 МПа. Какое количество теплоты сообщено газу при нагревании?
[4,15 кДж]
171. В закрытом сосуде находится 14 г азота при давлении 0,1 МПа и температуре 27оС. После нагревания давление в сосуде повысилось в 5 раз. До какой температуры был нагрет газ? Найти объем сосуда и количество теплоты, сообщенное газу.
[1500 К; 12,4 л; 12,4 кДж]
172. Какое количество теплоты надо сообщить массе 12 г кислорода, чтобы нагреть его на 50оС при постоянном давлении?
[545 Дж]
173. Масса 6,5 г водорода, находящегося при температуре 27оС, расширяется вдвое при постоянном давлении за счет притока тепла извне. Найти работу расширения газа, изменение внутренней энергии газа и количество теплоты, сообщенное газу.
[8,1 кДж; 20,2 кДж; 28,3 кДж]
174. 10,5 г азота изотермически расширяется при температуре 250 К, причем его давление изменяется от 250 кПа до 100 кПа. Найти работу, совершенную газом при расширении.
[714 Дж]
175. При изотермическом расширении 10 г азота, находящегося при температуре 17оС, была совершена работа 860 Дж. Во сколько раз изменилось давление азота при расширении?
[2,72]
176. Гелий, находящийся при нормальных условиях, изотермически расширяется от объема 1 л до 2 л. Найти работу, совершенную газом при расширении, и количество теплоты, сообщенное газу.
[70 Дж; 70 Дж]
177. 7,5 л кислорода адиабатически сжимаются до объема 1 л, причем в конце сжатия установилась давление 1,6 МПа. Под каким давлением находился газ до сжатия?
[95 кПа]
178. При адиабатическом сжатии воздуха в цилиндрах двигателя внутреннего сгорания давление изменяется от 0,1 МПа до 3,5 МПа. Начальная температура воздуха 40оС. Найти температуру воздуха в конце сжатия.
[865 К]
179. Двухатомный газ, находящийся при давлении 2 МПа и температуре 27оС, сжимается адиабатически от объема V 1 до V 2 = 0,5 V 1. Найти температуру и давление газа после сжатия.
|
|
|
[396 К; 5,28 МПа]
180. Идеальная тепловая машина, работающая по циклу Карно, совершает за один цикл работу 2,94 кДж и отдает за один цикл холодильнику количество теплоты 13,4 кДж. Найти к.п.д. цикла.
[18 %]
181. Идеальная тепловая машина, работающая по циклу Карно, совершает за один цикл работу 73,5 кДж. Температура нагревателя 100оС, температура холодильника 0оС. Найти к.п.д. цикла, количество теплоты, получаемое машиной за один цикл от нагревателя, и количество теплоты, отдаваемое за один цикл холодильнику.
[26,8 %; 274 кДж; 200 кДж]
182. Найти изменение энтропии при превращении массы 10 г льда (при - 20оС) в пар (температура кипения 100оС).
[88 Дж/К]
183. Найти изменение энтропии при переходе 8 г кислорода от объема 10 л при температуре 80оС к объему 40 л при температуре 300оС.
[5,4 Дж/К]
184. Найти изменение энтропии при переходе 6 г водорода от объема 20 л под давлением 150 кПа к объему 60 л под давлением 100 кПа.
[71 Дж/К]
185. Найти изменение энтропии при изобарическом расширении 6,6 г водорода от объема V 1 до объема V 2 = 2 V 1.
[66,3 Дж/К]
186. Найти изменение энтропии при изотермическом расширении 6 г водорода от давления 100 кПа до давления 50 кПа.
[17,3 Дж/К]
187. Масса 10,5 г азота изотермически расширяется от объема 2 л до объема 5 л. Найти изменение энтропии в этом процессе.
[2,9 Дж/К]
188. 10 г кислорода нагревается от температуры 50оС до температуры 150оС. Найти изменение энтропии, если нагревание происходит: а) изохорически; б) изобарически.
[1,76 Дж/К; 2,46 Дж/К]
Глава 9. Реальные газы и жидкости
Контрольные вопросы
1. Чем отличается реальный газ от идеального?
2. Запишите уравнение состояния реального газа. Поясните смысл поправок а и b.
3. Газ находиться под давлением P o. Каково будет давление внутри газа, если: 1) газ идеальный; 2) газ реальный? Чему будут равны давления этих газов на стенки сосудов, в которых они находятся?
4. Начертите и проанализируйте экспериментальные изотермы Эндрюса для углекислого газа.
5. Начертите и проанализируйте изотермы Ван-дер-Ваальса.
6. Что значит критическое состояние вещества? Назовите критические температуры для некоторых газов.
7. Из чего складывается внутренняя энергия реального газа? Чему она равна для 1 моля реального газа?
|
|
|
8. В чем состоит эффект Джоуля – Томсона? От чего зависит его знак?
9. Какие методы сжижения газов Вы знаете? Объясните их суть.
10. Какими свойствами обладает жидкость?
11. Чему равна сила поверхностного натяжения? Где и как расположен вектор этой силы?
12. Как зависит поверхностное натяжение жидкостей от температуры? Чему равен коэффициент поверхностного натяжения при критической температуре?
13. Что значит смачивание и несмачивание?
14. Вычислите высоту поднятия (опускания) жидкости в капиллярах.
15. Чем объясняется тепловое расширение твердых тел?
16. Чему равна молярная теплоемкость твердых тел по классическим представлениям? Каким экспериментальным законом она определяется?
17. Каковы трудности классической теории теплоемкости твердых тел? Когда и каким образом эти трудности были устранены?
18. Запишите уравнение Клапейрона – Клаузиуса для парообразования и плавления. Начертите и поясните графики этих фазовых переходов в осях P – T.
19. Начертите диаграмму состояния вещества. Какое она имеет значение для науки и практики?
Уравнение Ван-дер-Ваальса для одного моля газа
 ,
,
для произвольной массы газа
 ,
,
где m - молярная масса, m/ m - число молей газа.
Поправки Ван-дер-Ваальса - a и b - даются в таблицах или определяются следующими соотношениями
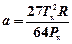 ;
; 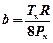 ,
,
где Т к – критическая температура, Р к – критическое давление.
Сила поверхностного натяжения жидкости
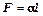 ,
,
где a - коэффициент поверхностного натяжения жидкости, l - длина контура, ограничивающего свободную поверхность жидкости.
Давление Лапласа
 ,
,
где r 1, r 2 - радиусы кривизны двух нормальных взаимно перпендикулярных сечений поверхности жидкости.
Работа при изменении площади свободной поверхности жидкости на DS
A=aDS.
Высота поднятия (опускания) жидкости в капилляре
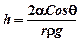 ,
,
где q - краевой угол, r - радиус капилляра, r - плотность жидкости.
|
|
|
|
|
Дата добавления: 2014-11-16; Просмотров: 1380; Нарушение авторских прав?; Мы поможем в написании вашей работы!