
КАТЕГОРИИ:
Архитектура-(3434)Астрономия-(809)Биология-(7483)Биотехнологии-(1457)Военное дело-(14632)Высокие технологии-(1363)География-(913)Геология-(1438)Государство-(451)Демография-(1065)Дом-(47672)Журналистика и СМИ-(912)Изобретательство-(14524)Иностранные языки-(4268)Информатика-(17799)Искусство-(1338)История-(13644)Компьютеры-(11121)Косметика-(55)Кулинария-(373)Культура-(8427)Лингвистика-(374)Литература-(1642)Маркетинг-(23702)Математика-(16968)Машиностроение-(1700)Медицина-(12668)Менеджмент-(24684)Механика-(15423)Науковедение-(506)Образование-(11852)Охрана труда-(3308)Педагогика-(5571)Полиграфия-(1312)Политика-(7869)Право-(5454)Приборостроение-(1369)Программирование-(2801)Производство-(97182)Промышленность-(8706)Психология-(18388)Религия-(3217)Связь-(10668)Сельское хозяйство-(299)Социология-(6455)Спорт-(42831)Строительство-(4793)Торговля-(5050)Транспорт-(2929)Туризм-(1568)Физика-(3942)Философия-(17015)Финансы-(26596)Химия-(22929)Экология-(12095)Экономика-(9961)Электроника-(8441)Электротехника-(4623)Энергетика-(12629)Юриспруденция-(1492)Ядерная техника-(1748)
Буферные растворы
|
|
|
|
ЗАДАЧИ ДЛЯ САМОСТОЯТЕЛЬНОГО РЕШЕНИЯ
1. Напишите уравнения протолитического равновесия и укажите сопряженные кислотно-основные пары в водных растворах:
а) азотистой кислоты Ко (HNO2) = 5,1×10-4;
б) аммиака Кo(NH3××H2O)= 1,76×10-5;
в) угольной кислоты Ко (Н2СО3 )= 4,5 • 10-7 Ко (НСО3-) = 4,8×10-11
От каких факторов зависит стандартная константа равновесия Ко ?
2.Вычислите концентрационную константу основности аммиака Кс(NH3×H2O) и рKc(NH3×H2O)в 0,02 н растворе КС1, если рКо (NH3×H2O)=4,75.
3. Напишите уравнения реакций автопротолиза воды и безводной уксусной кислоты.
4. Как связаны константы кислотности и основности сопряженной пары
NH4 + - NH3? Приведите вывод формулы.
5. Степень диссоциации уксусной кислоты равна 1,32 • 10-2,Ко= 1,75 • 10-5.
Определите концентрацию кислоты, концентрацию ацетат-иона и рН раствора.
Коэффициенты активностей ионов принять равными 1.
6. В О,1 М водном растворе аммиака рН=11,12. Вычислите степень диссоциации,
константу основности и концентрацию ионов аммония в данном растворе.
Коэффициенты активностей ионов принять равными 1.
7. К 50 мл 0,1 М раствора муравьиной кислоты (р=1,00 г/мл) добавили 50 мл
0,01 М раствора соляной кислоты (р=1,00 г/мл). Определите рН и степень диссоциации муравьиной кислоты в полученном растворе (р=1,00 г/мл),
если К о(НСООН)= 1,37×10-4? Коэффициенты активностей ионов считать равными 1.
8. Напишите уравнение протолитического равновесия в водном растворе нитрата аммония. Сколько граммов NH4NO3 содержится в 100 мл его водного раствора, если рН=5,12?
[Ко (NH3H2O) =1,76 •10-5 ]. Коэффициенты активностей ионов принять равными 1.
9. Рассчитайте рН раствора, полученного при смешивании 10 мл 0,1 М HNO2 и 20 мл 0,05 М КОН, если плотности растворов равны 1,00 г/мл [К о (HNO2). =5,1×10-4]. Коэффициенты активностей ионов принять равными 1.
|
|
|
Буферные растворы – сложные протолитические системы, способные сохранять примерное постоянство рН при добавлении в такую систему небольших количеств сильных кислот или щелочей. Буферные растворы широко распространены в химической и биохимической практике.
Все буферные системы содержат минимум два вещества, кроме воды. Эти вещества - сопряженная слабая кислота и соответствующее ей сопряженное основание - образуют в водном растворе протолитическую буферную систему.
Виды основных буферных водных растворов:
- слабая кислота и ее соль (СH3COOH- CH3COONa)
- слабое основание и его соль (NH3 – NH4Cl)
-средняя и кислая соль (Na2CO3 – NaHCO3)
- две кислых соли (NaH2PO4 – Na2HPO4)
- аминокислотные и белковые системы (гемоглобин - оксигемоглобин)
Компоненты буферной системы, представляющие собой сопряженную кислотно-основную пару, реагируют с водой, создавая буферные равновесия. В общем виде, если НА – слабая кислота, а А-- анион этой кислоты (т.е. анионное основание), то буферные равновесия запишутся в следующем виде:
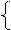 НА +Н2О ↔ А- + Н3О+
НА +Н2О ↔ А- + Н3О+
А- + Н2О ↔ НА + ОН-.
Оба этих равновесия по принципу Ле Шателье сильно смещены влево, поэтому равновесные концентрации сопряженных кислоты и основания практически равны исходным концентрациям.
Так как буферная система образована одной и той же кислотно-основной парой, то из выражения для константы кислотности можно вывести уравнения для расчета рН в буферных растворах, которое называется уравнением Гендерсона-Хассельбальха:
a (А-)
pH = pKa + lg-----------
а (НА),
где а – активности соответствующих компонентов буферной системы.
|
|
|
|
|
Дата добавления: 2014-12-27; Просмотров: 591; Нарушение авторских прав?; Мы поможем в написании вашей работы!