
КАТЕГОРИИ:
Архитектура-(3434)Астрономия-(809)Биология-(7483)Биотехнологии-(1457)Военное дело-(14632)Высокие технологии-(1363)География-(913)Геология-(1438)Государство-(451)Демография-(1065)Дом-(47672)Журналистика и СМИ-(912)Изобретательство-(14524)Иностранные языки-(4268)Информатика-(17799)Искусство-(1338)История-(13644)Компьютеры-(11121)Косметика-(55)Кулинария-(373)Культура-(8427)Лингвистика-(374)Литература-(1642)Маркетинг-(23702)Математика-(16968)Машиностроение-(1700)Медицина-(12668)Менеджмент-(24684)Механика-(15423)Науковедение-(506)Образование-(11852)Охрана труда-(3308)Педагогика-(5571)Полиграфия-(1312)Политика-(7869)Право-(5454)Приборостроение-(1369)Программирование-(2801)Производство-(97182)Промышленность-(8706)Психология-(18388)Религия-(3217)Связь-(10668)Сельское хозяйство-(299)Социология-(6455)Спорт-(42831)Строительство-(4793)Торговля-(5050)Транспорт-(2929)Туризм-(1568)Физика-(3942)Философия-(17015)Финансы-(26596)Химия-(22929)Экология-(12095)Экономика-(9961)Электроника-(8441)Электротехника-(4623)Энергетика-(12629)Юриспруденция-(1492)Ядерная техника-(1748)
Cинтез a - аминокислот
Стереохимия a - аминокислот.
Все природные a - аминокислоты, кроме простейшей аминокислоты - глицина, содержат хотя бы один хиральный центр и могут существовать в виде пары энантиомеров.
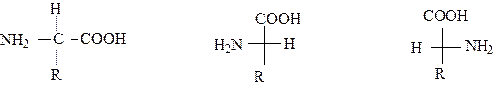 |
a -Аминокислота L -a - Аминокислота D- a- Аминокислота
Почти все природные a- аминокислоты принадлежат к L-ряду. Использование для построения белков человеческого организма только одного вида стереоизомеров a- аминокислот имеет важнейшее значение для формирования пространственной структуры белков и проявления ими биологической активности.
Из приведенного выше материала видно, что аминокислоты имеют разнообразное строение и способы синтеза их также различны. Мы остановимся на наиболее общих, включающих введение одной амино- или карбоксильной группы.
1.Замена галогена в a- галогензамещенной кислоте на аминогруппу.
При действии на бромуксусную кислоту аммиаком получают глицин
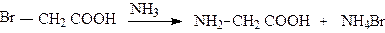 |
изб.
2. Циангидридный метод.
a - Аминокислоты получаются при действии на альдегиды и кетоны цианистым аммонием с последующим гидролизом промежуточно образующихся соединений:
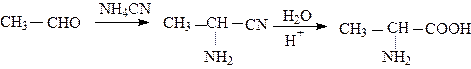
3. Восстановительное аминирование оксокислот.
a - Аминокислоты получают при каталитическом восстановлении оксокарбоновых кислот водородом в присутствии аммиака:
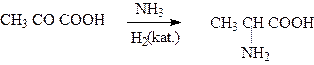 |
Наиболее удобным способом получения a- аминокислот L -ряда служат белки, которые подвергают гидролизу. Синтетическим путем получают только рацемические смеси a- аминокислот. Для получения нужного энантиомера рацемическую смесь, полученную синтезом, подвергают расщеплению. Один из способов расщепления a- аминокислот описан ранее (см.раздел 1.3.3.).
a - Аминокислоты представляют собой бесцветные кристаллические вещества, большинство из них легко растворимы в воде.
a - Аминокислоты плавятся с разложением при высоких и довольно близких температурах. Определение температуры плавления недостаточно для их идентификации и поэтому для этой цели используют данные хроматографии.
a - Аминокислоты содержат одновременно основную, аминную, и кислую, карбоксильную группы, которые взаимодействуют между собой, образуя внутреннюю соль - биполярный ион
(цвиттер – ион)
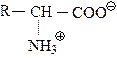 |
В водном растворе внутренняя соль, как соль слабой кислоты и слабого основания, гидролизуется, при этом образуются катионы и анионы аминокислоты.
 |
Иными словами, a - аминокислоты являются амфотерными соединениями и в зависимости от рН среды образуются катионы и анионы, которые под действием электрического тока могут передвигаться к катоду или аноду. Если этот процесс проводят на хроматографической бумаге или в гелях, то такой процесс называется электрофорезом. Этот метод используется для идентификации или разделения аминокислот.
 |
сопряженная нейтральный биполярный ион сопряженное кислота глицина глицин основание глицина
(кислая среда) щелочная среда
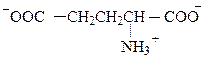 |
В связи с тем, что в зависимости от строения в молекуле могут преобладать либо кислотные свойства карбоксила, либо основные свойства аминогруппы, в водных растворах аминокислот рН среды отличается от нейтральной. Но на кривой титрования аминокислоты имеется значение рН,при котором количество групп NH3+ оказывается точно равным количеству групп -СОО-. Следовательно, при этом рН в условиях электрофореза переноса заряженных частиц не будет. Такое значение рН называют изоэлектрической точкой (рНi). Изоэлектрическая точка глицина 6.0. Глутаминовая кислота содержит вторую карбоксильную группу, и при рН = 6 большая часть ее молекул находится в виде анионов:
Чтобы достигнуть изоэлектрической точки, некоторые из этих анионов надо протонировать, что возможно только при понижении рН. рНi глутаминовой кислоты равна 3.22.
|
|
Дата добавления: 2014-12-27; Просмотров: 936; Нарушение авторских прав?; Мы поможем в написании вашей работы!