
КАТЕГОРИИ:
Архитектура-(3434)Астрономия-(809)Биология-(7483)Биотехнологии-(1457)Военное дело-(14632)Высокие технологии-(1363)География-(913)Геология-(1438)Государство-(451)Демография-(1065)Дом-(47672)Журналистика и СМИ-(912)Изобретательство-(14524)Иностранные языки-(4268)Информатика-(17799)Искусство-(1338)История-(13644)Компьютеры-(11121)Косметика-(55)Кулинария-(373)Культура-(8427)Лингвистика-(374)Литература-(1642)Маркетинг-(23702)Математика-(16968)Машиностроение-(1700)Медицина-(12668)Менеджмент-(24684)Механика-(15423)Науковедение-(506)Образование-(11852)Охрана труда-(3308)Педагогика-(5571)Полиграфия-(1312)Политика-(7869)Право-(5454)Приборостроение-(1369)Программирование-(2801)Производство-(97182)Промышленность-(8706)Психология-(18388)Религия-(3217)Связь-(10668)Сельское хозяйство-(299)Социология-(6455)Спорт-(42831)Строительство-(4793)Торговля-(5050)Транспорт-(2929)Туризм-(1568)Физика-(3942)Философия-(17015)Финансы-(26596)Химия-(22929)Экология-(12095)Экономика-(9961)Электроника-(8441)Электротехника-(4623)Энергетика-(12629)Юриспруденция-(1492)Ядерная техника-(1748)
Температура замерзання і кипіння розбавлених розчинів
|
|
|
|
Індивідуальні речовини характеризуються певними температурами переходів з одного агрегатного стану в інший (температура кипіння, температура плавлення, або кристалізації). Так, вода під нормальним атмосферним тиском (101,325 кПа) кристалізується при температурі 00 С і кипить при 1000 С.
Наявність розчиненої речовини підвищує температуру кипіння і знижує температуру замерзання розчинника, і тим сильніше, чим більша концентрація розчину. Здебільшого з розчину кристалізується або википає тільки розчинник, внаслідок чого концентрація розчину в ході його замерзання або кипіння зростає. Отже, розчин кристалізується і кипить не при певній температурі, а в деякому температурному інтервалі. Температуру початку кристалізації і початку кипіння розчину називають його температурою кристалізації і температурою кипіння.
Різниця між температурами кипіння розчину і чистого розчинника називається підвищенням температури кипіння розчину (∆tКИП). Різниця між температурою замерзання чистого розчинника і розчину називається зниженням температури замерзання розчину (∆tЗАМ):

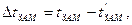
де 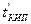 і
і  - температури кипіння і замерзання розчину; tКИП і tЗАМ - температури кипіння і замерзання чистого розчинника.
- температури кипіння і замерзання розчину; tКИП і tЗАМ - температури кипіння і замерзання чистого розчинника.
Всяка рідина починає кипіти при тій температурі, при якій тиск насиченої пари досягає величини зовнішнього тиску. Якщо розчинити у воді яку-небудь речовину, то тиск водяної тари знизиться. Щоб довести тиск пари цього розчину до атмосферного, треба його ще нагріти. Звідси випливає, що температура кипіння розчину завжди вища за температуру кипіння чистого розчинника. Аналогічно пояснюється і зниження температури замерзання розчинів.
|
|
|
Вивчаючи замерзання і кипіння розчинів, Рауль (1887 р.) вста-новив, що для розбавлених розчинів неелектролітів підвищення температури кипіння і зниження температури замерзання пропорційні концентрації розчину (ІІ закон Рауля):


де Сm - моляльна концентрація (моляльність); Е і К - ебуліоскопічна і кріоскопічна сталі, що залежать тільки від природи розчинника, але не залежать від природи розчиненої речовини. Для води кріоскопічна стала К дорівнює 1,860, а ебуліоскопічна стала Е - 0,520.
Пониження tЗАМ розчинів має велике значення для живих організмів. Клітинний сік - це розчин органічних речовин, його tЗАМ лежить нижче 00 С, тому організми виживають при низьких темпе-ратурах. Зимостійкість рослин пов'язана з концентрацією клітинного соку. Чим вища концентрація, тим нижчі температури може переносити культурна рослина. Процес перетворення більш високомолекулярних речовин в сполуки з меншою молекулярною масою (перетворення крохмалю в глюкозу) також пов’язаний з намаганням рослин підвищити концентрацію клітинного соку.
Запитання для самоконтролю
1. Характеристика дисперсних систем та їх класифікація.
2. Який розмір подрібнених частинок в істинному розчині?
3. Якою системою, гомогенною чи гетерогенною, є істинний розчин?
4. Які розчини називають ненасиченими, насиченими, перенасиченими?
5. Як виражають розчинність речовин?
6. Від чого залежить розчинність кристалічних речовин, рідин, газів?
7. Які є способи вираження складу розчинів?
8. Який процес називається осмосом?
9. Від чого залежить осмотичний тиск?
10. Яке значення має осмос для живих організмів?
11. Які розчини називають ізотонічними?
12. Чи відрізняється температура кипіння та замерзання розчинів від температури кипіння та замерзання чистого розчинника?
13. Який фізичний зміст кріоскопічної та ебуліоскопічної сталих?
|
|
|
|
|
Дата добавления: 2015-05-24; Просмотров: 3549; Нарушение авторских прав?; Мы поможем в написании вашей работы!