
КАТЕГОРИИ:
Архитектура-(3434)Астрономия-(809)Биология-(7483)Биотехнологии-(1457)Военное дело-(14632)Высокие технологии-(1363)География-(913)Геология-(1438)Государство-(451)Демография-(1065)Дом-(47672)Журналистика и СМИ-(912)Изобретательство-(14524)Иностранные языки-(4268)Информатика-(17799)Искусство-(1338)История-(13644)Компьютеры-(11121)Косметика-(55)Кулинария-(373)Культура-(8427)Лингвистика-(374)Литература-(1642)Маркетинг-(23702)Математика-(16968)Машиностроение-(1700)Медицина-(12668)Менеджмент-(24684)Механика-(15423)Науковедение-(506)Образование-(11852)Охрана труда-(3308)Педагогика-(5571)Полиграфия-(1312)Политика-(7869)Право-(5454)Приборостроение-(1369)Программирование-(2801)Производство-(97182)Промышленность-(8706)Психология-(18388)Религия-(3217)Связь-(10668)Сельское хозяйство-(299)Социология-(6455)Спорт-(42831)Строительство-(4793)Торговля-(5050)Транспорт-(2929)Туризм-(1568)Физика-(3942)Философия-(17015)Финансы-(26596)Химия-(22929)Экология-(12095)Экономика-(9961)Электроника-(8441)Электротехника-(4623)Энергетика-(12629)Юриспруденция-(1492)Ядерная техника-(1748)
Примеры решения задач. Задача 1. Для каких-элементов, имеющих электронные конфигурации
|
|
|
|
Задача 1. Для каких-элементов, имеющих электронные конфигурации
внешнего слоя атома a) 3s2р2; б) 4s2р3; в) 5s25p4; г) 6s26р3,
характерны переменная четная и переменная нечетная валентности.
Решение. При возбуждении электронов внешнего уровня в а,б,
в, г их электронные формулы таковы: а) 3s13р3;
б) 4s14р34d1; в) 5sI5p35d2; г) 6sI6p36dI.
Для "а" (кремний) валентность равна 2,4;
для "б" (мышьяк) валентность равна 3,5;
для "в" (теллур) валентность равна 2,4,6;
для "г" (висмут) валентность равна 3,5.
Задача 2. Каковы возможные валентности у атомов кислорода и серы?
Решение. Электронные формулы внешнего уровня кислорода и серы
соответственно таковы: 2s22р4 и 3s23р4. У атома серы имеется
вакантный подуровень и спаренные электроны атома серы могут
распариваться, увеличивая число неспаренных электронов, вследствие
чего валентность серы равна 2,4,6, а у атома кислорода валентность
может быть равна только 2, т.к. нет вакантного подуровня.
Задача 3. Молекула хлорида бора BCl3 имеет плоскую структуру, а
хлорида азота NCl3- пирамидальную. Чем объясняется такое
различие?
Решение - В молекуле BCl3 центральный атом В при возбуждении
имеет 3 электрона:

Непарные электроны возбужденного атома бора находятся в sp2-
гибридном состоянии, 3 гибридные орбитали атома бора расположены
под углом 1200 и связи B-Cl также направлены под углом 120, форма
молекулы плоская.

|
В молекуле NCl3 у атома азота на четыре гибридные орбитали
приходится 5 электронов:  и пара ē на 2s-
и пара ē на 2s-
орбитали является несвязывающей, она оказывает большое
отталкивающее действие, тетраэдрический угол уменьшается до
107° и форма молекулы становится пирамидальной.
Задача 4. В молекулах СН4, NH3 и H2Oвалентные орбиталиатомов
|
|
|
С,N,O находятся в состоянии sp3 - гибридизации, однако углы между
связями не равны; в CH4 - 109, в NH3-107, в H2O - 104,50. Как это
объяснить?
Решение. Причиной этого соглаcно теории валентных связей является
наличие у центрального атома несвязывающих электронных пар.
Искажение валентных углов вызывается взаимным отталкиванием
связывающих инесвязывающих электронных пар центрального
атома. Здесь нужно учесть следующее: связывающая орбиталь
(электронная пара - локализованнаямежду двумя атомами) имеет
меньшие размеры, чем орбиталь несвязывающей электронной пары.
Наиболее сильное отталкивание наблюдается между несвязывающими
парами, меньший эффект отталкивания между несвязывающей и
связывающей парой, наименьшее отталкивание проявляется между
связывающими электронными парами.
 В предложенных молекулах центральные атомы образуют химические связи за счет электронов sp3-гибридных орбиталей. В молекуле СН4 у атома углерода на четыре sр3-гибридные орбитали приходится четыре электрона: Это определяет образование 4σ-связей С-H, направленных под углом 1090.
В предложенных молекулах центральные атомы образуют химические связи за счет электронов sp3-гибридных орбиталей. В молекуле СН4 у атома углерода на четыре sр3-гибридные орбитали приходится четыре электрона: Это определяет образование 4σ-связей С-H, направленных под углом 1090.
 В молекуле NH3 в атоме азота на четыре sp3 -гибридные орбитали приходится 5 электронов: 2s-орбиталь будет несвязывающей и занимает одну одну из sp3 - гибридных орбиталей азота, направленных к вершинам тетраэдра. Несвязывающая электронная пара отталкивается от связывающих, в молекуле NH3 угол становится меньше тетраэдрического и равен HNH=107,30 (геометрическая форма – пирамидаль-
В молекуле NH3 в атоме азота на четыре sp3 -гибридные орбитали приходится 5 электронов: 2s-орбиталь будет несвязывающей и занимает одну одну из sp3 - гибридных орбиталей азота, направленных к вершинам тетраэдра. Несвязывающая электронная пара отталкивается от связывающих, в молекуле NH3 угол становится меньше тетраэдрического и равен HNH=107,30 (геометрическая форма – пирамидаль-

|
ная). Вмолекуле H2O у атома кислорода на четыре sp3- гибридные орбитали приходится 6 электронов. Здесь уже 2sp3 - гибридные орбитали занимают несвязыващие электронные пары и отталкивающее действие двух несвязывающих электронных пар проявляется в большей степени, поэтому валентный угол становится еще меньше ∟НОН=104,5° (геометрическая форма –угловая).
Задача 5. Объясните и покажите образование связей в молекулах
|
|
|
C2H4, C2H2, KHCO3.
Решение. Атом углерода в этих молекулах центральный. Электронная
формула углерода такова: ls22s22p2. При возбуждении атом углерода
имеет следующуюформулу ls22s12p3  В молекуле
В молекуле
C2H4каждый атом углерода находится в состоянии sр2 - гибридизации,а
в sр2-гибридном состоянии гибридные орбиталицентрального атома
направлены под углом 1200. Покажемперекрывание гибридных
орбиталей углерода:

При перекрывании гибридных орбиталей каждый атом углерода образует по 3σ-связи: одну σ - С-С и 2σ -связи С-Н с атомами водорода. В возбужденном атоме углерода по одному электрону от каждогоне вошли в гибридизацию и, перекрываясь, образуют по обе стороны линии σ-связи
π-связь (перпендикулярно σ -связи); каждый атом углерода образует по 3 σ- σ-связи и 1 π-связь. В молекуле С2Н2 каждый атом углерода находится в состоянии sp-гибридизации и образует по 2 σ-связи С-С и С-Н, а 2 р-электроны, не вошедшие в гибридизацию, образуют еще 2 π-связи перпендикулярно друг другу. Покажем перекрывание орбиталей в С2Н2:
| π |
| Н |
| Н |
| С |
| С |
| π |
| π |
| π |
| σ |
| σ |
| σ |
| О |
| О |
| σ |
| σ |
| К |
| π |
| π |
| σ |
| σ |
| σ |
| О |
| С |
| Н |
Задача 6. Чем объяснить устойчивость мономерных молекул N2, O2, CO, CO2 (образованы атомами элементов II периода) и склонность к полимеризации молекул Р2 (образованы атомами элементов III периода или атомами кислорода и элементов III периода)?
Решение. В молекулах N2, O2, CO, CO2 наряду с σ-связыванием наблюдается π-связывание, т.е. в этих молекулах образуются прочные кратные связи, например, в молекуле N2 проявляется 1 σ-связь и 2 π-связи. Возбужденный атом углерода в молекуле CO2 имеет 4 непарных электрона. Непарные электроны s-орбитали и р-орбитали образуют 2 sp-гибридные орбитали, расположенные под углом 180 0С. Молекула линейная и каждый из атомов кислорода объединяется с атомом углерода одной σ- и одной π-связью. Поэтому молекулы N2, O2, CO, CO2 устойчивы. Размеры атомов элементов III периода много больше
|
|
|
размеров атомов элементов II периода, поэтому для них мало
характернообразование π -связывания.Поэтому молекулы P=P,S=S,
Si=0, O=Si=O нестабильны и склонны к полимеризации, для фосфора и
серы в конденсированном состоянии характерны цепи:−S−S−; −P−Р−;
для оксидов кремния - цепи: –O−Si−O−Si−O– и
O O
| |
–O−Si−O−Si−O−
| |
O O
В молекуле SiO2 стабилизация связей Si−O достигается за счет
адативного взаимодействия O 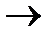 SiO с участием d-орбиталей атомов
SiO с участием d-орбиталей атомов
кремния.
Задача 7. Пользуясь значениями электроотрицательности,
предскажите, имеет ли связь в а)CaO; б)HJ; в)SiH4; г) Br2 чисто
ковалентный, чисто ионный или частично ионный характер. В случае
чисто ионной и частично ионной связей укажите ожидаемое
распределение зарядов ОЭOCa=1; ОЭOO=3,5.
Решение. а) Разность электроотрицательностей в молекуле СaО
∆ОЭО=ОЭОО – ОЭОCa = 2,5 велика, следовательно, связь CaO имеет
чисто ионный характер и может описываться структурой Са2+О2-;
б) ОЭОJ=2,5; ОЭОH = 2,1 для HJ ∆ОЭО=(ОЭОJ – ОЭОH = 0,40 связь в
этом соединении ковалентная с небольшой степенью ионности Нσ+Jσ–;
в) ОЭОSi = 1,8; ОЭОH = 2,1 SiH4 ∆ОЭО=ОЭОH – ОЭОSi =0,30, связь
ковалентная с очень небольшой степенью ионности, распределение

зарядов описывается структурой.
Ионный характер связи в этом случае мал и принято считать, что связь
Si-Н имеет чисто ковалентный характер;
г) в молекуле Вr2 ∆ОЭО=0, связь чисто ковалентная.
Задача 8. Определить тип гибридизации и форму молекулы в
соединении CdС12.
Решение. Электронная формула кадмия ls22s22p63s23p64s23d104p65s24d10.
При возбуждении электроны на 5s- подуровне
"распариваются" и один из них переходит с 5s-подуровня на
5р-подуровень. Итак, в образовании связи участвуют
электроны различных энергетических подуровней. В этом
случае они выравнивают свои энергии и образуют две
гибридные орбитали, направленные под углом 180°, которые
|
|
|



при образовании связей перекрываются р-орбиталями атома хлора. Следовательно, молекулаCdCl2 линейна.
Задача 9. Рассчитайте изменение энтальпии реакции Н— С 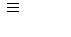 С—Н +
С—Н +

2CI—CI →, если энергии связей С-Н, С-С,
CI-СI, С-CIсоответственно равны -347,2; -823,1; -242,3;
-345,2 кДж/моль.
Решение. Образование соединения C2Н2Cl4 можно представить так:
надо разорвать тройную связь С-С и две связи CI-CI и
образовать одинарную связь С-С и четыре -Cl; изменение
энтальпии реакции (∆H0298) равно: H0298= H0298(С-Н)+
+ 4H0298(C- Cl) - H0298(C-C) 2Н0298(С-Сl) = -347,2 +(-345)·4 –
- (-823,1)-(-242,3 )· 2 = -420,4 кДж/моль.
Задача 10. Вязкость глицерина CH2OHCH(OH)CH2OH в 75 раз больше
вязкости этиленгликоля CH2OH-CH2OH. Какова причина
cтоль сильного различия вязкости?
Решение. Наличие большого числа гидроксильных групп в молекуле
глицерина увеличивает возможность образования
межмолекулярных водородных связей, что сказывается
на увеличении вязкости глицерина по сравнению с
этиленгликолем.
Задача 11. Почему в ряду HF, НСl, HBr, HJпадает прочность
химической связи и устойчивость молекул к нагреванию?
Решение. При переходе от HF к HJ уменьшается степень
перекрывания электронных облаков атомов водорода и
галогена, а область перекрывания располагается на большем
раccтоянии от ядра атома галогена и сильнее экранируется
возросшим числом промежуточных электронных слоев.
Кроме того, в ряду F-Cl-Br-Jуменьшается
электроотрицательность атома галогена. В результате этого в
молекуле HF электронное облако атома водорода смещается
в сторону атома галогена в наибольшей степени, а в
молекулах HCl, НВr, HJ это приводит к уменьшению
перекрывания облаков и к ослаблению связи между атомами.
С уменьшением прочности связи в молекулах
галогеноводородов падает их устойчивость к нагреванию.
Термическая диссоциация HF происходит лишь при очень
высоких температурах (более 3500°С), тогда как HJ
распадается в значительной степени при 300°С на йод и водород.
Задача 12. Определите энергию связи кислород-водород в молекуле
H2O, если энергия связей водород-водород и кислород-
кислород соответственно равна 435,9; 498,7 кДж/моль, а
при сгорании 2 молей водорода выделяется 483,68 кДж
теплоты.
Решение. Важнейшей характеристикой связи является энергия,
определяющая ее прочность. Образование молекулы воды
можно представить таким образом: а) разрыв связи водород-
водород и кислород-кислород в молекулах Н2O и O2 с обра-
зованием атомов Н и O; б) образовавшиеся атомы водорода и
кислорода соединяются в молекулы H2O, каждая из которых
содержит две связи кислород-водород:
4Н (г) = 2Н2(г) - 485,9 2
2О (г) = О2(г) - 498,2
2Н2(г)+О2(г)= 2Н2О(г)- 483,68
2Н(г)+2О(г) = 2Н2О(г) – 1854,18кДж
в двух молекулах H2O четыре связи кислород-водород; средняя
энергия связи кислород-водород равна 
Задача 13. Какая из следующихсвязей более полярна: а) В-Сl;
или C-Cl; б) Р-Fили P-Cl? В каждом случае укажите,
на каком атоме возникает парциальный отрицательный
заряд.
Решение. а) Разность электроотрицательностей (∆ОЭО) бора и хлора
равна ∆ОЭО B-Cl =ОЭОCl - ОЭОВ =3,2-1,8=1,4;
∆ОЭОC-Cl=ОЭOCl - ОЭОc =3,2-2,5=0,7. Следовательно, связь
B-CI должнабыть более полярной; на атоме хлора должен
находиться парциальный отрицательный заряд, поскольку он
более электроотрицателен. Поскольку бор в периодической
системе расположен слева от углерода, то можно
предсказать, что он должен слабее притягивать электроны.
Хлор, находящийся в правой части периодической таблицы,
должен сильнее притягивать электроны.Наиболее полярная
связь возникает между атомами элементов, один из которых
характеризуется самой низкой способностью притягивать
электроны (бор), а другой - наибольшей способностью при-
тягивать электроны (хлор);
б) поскольку фтор находится в периодической таблице над
хлором, для него следует предсказать более высокую
электроотрицательность. Следовательно, связь Р-Р должна
иметь большуюполярность по сравнению со связью P-CI.
Подтвердим это количественным расчетом ∆ОЭОF-P = ОЭOF
– ОЭOP = 4,0-2,2 = 1,8∆ОЭOCl-P = ОЭOCl - ОЭOр = 3,2-2,2=1.
Задача 14. Почему молекулы аммиака (NH3) и трифторид азота
NF3, имеющие одинаковую пирамидальную форму и
содержащие атомы элементов с примерно одинаковым
различием в электроотрицательности,существенно
различаются по величинам дипольных моментов:
μNH3 = 1,5Дж; μNF3=0,2Д?
Решение. На величину дипольного момента молекулы сильно влияют
несвязывающие (неподеленные) электронные пары.
Молекулы NH3 и NF3 имеют одинаковую геометрическую
форму, тригоно-пирамидальную неполярность связи N-Hи
N-F одинаковы, а дипольные моменты значительно
отличаются. Это можно объяснить следующим: большая
величина μ в молекуле NH3 объясняется тем, что
направление дипольного момента отдельных связей N-H,
имеющих отрицательный конец у атома азота и
неcвязывающей электронной пары совпадает и при
векторном сложении обуcловливaeт большой дипольный
момент молекулы: μNH3 = 1,5Д


В молекуле же NF3 дипольные моменты отдельных связей
N-F с положительным концом у атома азота и
неподеленной электронной пары направлены в
противоположные стороны, поэтому при векторном
сложении они компенсируются и μ сильно уменьшается и
μNF3 равно 0,2Д.
|
|
|
|
|
Дата добавления: 2015-05-26; Просмотров: 4278; Нарушение авторских прав?; Мы поможем в написании вашей работы!