
КАТЕГОРИИ:
Архитектура-(3434)Астрономия-(809)Биология-(7483)Биотехнологии-(1457)Военное дело-(14632)Высокие технологии-(1363)География-(913)Геология-(1438)Государство-(451)Демография-(1065)Дом-(47672)Журналистика и СМИ-(912)Изобретательство-(14524)Иностранные языки-(4268)Информатика-(17799)Искусство-(1338)История-(13644)Компьютеры-(11121)Косметика-(55)Кулинария-(373)Культура-(8427)Лингвистика-(374)Литература-(1642)Маркетинг-(23702)Математика-(16968)Машиностроение-(1700)Медицина-(12668)Менеджмент-(24684)Механика-(15423)Науковедение-(506)Образование-(11852)Охрана труда-(3308)Педагогика-(5571)Полиграфия-(1312)Политика-(7869)Право-(5454)Приборостроение-(1369)Программирование-(2801)Производство-(97182)Промышленность-(8706)Психология-(18388)Религия-(3217)Связь-(10668)Сельское хозяйство-(299)Социология-(6455)Спорт-(42831)Строительство-(4793)Торговля-(5050)Транспорт-(2929)Туризм-(1568)Физика-(3942)Философия-(17015)Финансы-(26596)Химия-(22929)Экология-(12095)Экономика-(9961)Электроника-(8441)Электротехника-(4623)Энергетика-(12629)Юриспруденция-(1492)Ядерная техника-(1748)
Определение углеводов методом йодометрии
|
|
|
|
В пищевой промышленности
Применение методов окисления-восстановления
Цель работы -определить массовую долю лактозы в молоке, используя метод йодометрии.
Сущность работы. Метод основан на окислении редуцирующих сахаров (лактозы, глюкозы), содержащих альдегидную группу, йодом в щелочной среде. Массовую долю сахарозы определяют по разности между количеством взятого и неизрасходованного йода, который определяют титрованием тиосульфатом натрия. В качестве индикатора используют раствор крахмала, который вводят вблизи точки эквивалентности. Титрование заканчивают, когда исчезает синяя окраска раствора.
Оборудование и реактивы:весы технические; штатив; бюретка, вместимостью 25 см3 и 50 см3; мерная колба, вместимостью 500 см3; мерный цилиндр, вместимостью 10 см3 (3 шт.); мерная пипетка, вместимостью 25 и 50 см3; коническая колба, вместимостью 250-300 см3; воронка, d ~ 7-10 см; бумажные фильтры, d ~10 см; резиновые пробки. Раствор Фелинга (реактив 1): 69,26 г перекристаллизованного сульфата меди, не содержащего железа, взвешивают и растворяют в мерной колбе, вместимостью 1000 см3. Раствор йода Сэк(I2) = 0,1000 моль/дм3 (реактив 2): 20-25 г йодида калия (KI) взвешивают в стакане, вместимостью 100 см3, растворяют в небольшом количестве воды. В этот же стакан добавляют 12,7 г металлического йода. Жидкость перемешивают до полного растворения йода и количественно переносят в мерную колбу, вместимостью 1000 см3, несколько раз ополаскивая стакан дистиллированной водой. Затем раствор доводят до метки дистиллированной водой. Раствор тиосульфата натрия Сэк(Na2S2O3) = 0,1000 моль/дм3 (реактив 3): 24,8 г соли Na2S2O3 переносят в мерную колбу, вместимостью 1000 см3, растворяют, прибавляют 0,2 г безводного карбоната натрия и доводят раствор водой до метки. Для приготовления раствора тиосульфата натрия используют бидистиллированную или свежепрокипяченную дистиллированную воду. Охлаждают воду в колбе, в пробке которой проходит хлоркальциевая трубка, наполненная кусочками натронной извести. Раствор хлороводородной кислоты Сэк(HCI) = 7,3 моль/дм3 (реактив 4): 120 см3 хлороводородной кислоты, плотность которой 1,19 г/см3, добавляют 80 см3 воды; раствор гидроксида натрия, Сэк(NаОН) = 0,1 моль/дм3; раствор хлороводородной кислоты, Сэк(HCI) = 0,5 моль/дм3.
|
|
|
Методика выполнения анализа. 25 г молока с точностью до 0,01 г взвешивают в мерную колбу, вместимостью 500 см3, прибавляют до половины колбы дистиллированную воду, 10 см3 раствора Фелинга (реактив 1) и 4 см3 раствора гидроксида натрия. Жидкость перемешивают после добавления воды и каждого реактива. Доводят раствор до метки дистиллированной водой (20 оC), перемешивают и оставляют на 30 мин. Отстоявшуюся жидкость фильтруют в сухую колбу через складчатый фильтр, отбрасывая первые 10-20 см3 фильтрата.
50 см3 фильтрата, что соответствует 2,5 г молока, пипеткой переносят в коническую колбу с притертой или резиновой пробкой. Приливают мерной пипеткой или бюреткой 25,00 см3 раствора йода (реактив 2) и медленно при непрерывном перемешивании приливают из бюретки 37,50 см3 раствора гидроксида натрия. Закрыв колбу пробкой, оставляют ее на 20 минут в темном месте при температуре ~ 20оС. Затем прибавляют 8 см3 раствора хлороводородной кислоты, Сэк(HCI) = 0,5 моль/дм3, и титруют выделившийся йод тиосульфатом натрия (реактив 3) до светло-желтого цвета, затем прибавляют 1 см3 раствора крахмала и продолжают титровать до исчезновения синей окраски.
Для контрольного опыта в другую такую же колбу отмеривают пипеткой 25 см3 раствора йода, 25 см3 воды и добавляют при непрерывном перемешивании 37,50 см3 раствора гидроксида натрия, закрыв пробкой, оставляют в темном месте на 20 мин и дальше титрование проводят, как в первой колбе.
|
|
|
Массовую долю лактозы в молоке (%) рассчитывают по формуле:
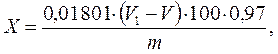 (55)
(55)
где V1 - объем раствора Na2S2O3, израсходованный на титрование контроль-ного опыта, см3;
V - объем раствора Na2S2O3, израсходованный на титрование фильтрата, см3;
m - масса молока в 50 см3 фильтрата, равна 2,5 г;
0,01801 - титр раствора йода по лактозе, Т (J2/лакт), г/см3;
0,97 - коэффициент перевода объема молока на массу.
|
|
|
|
|
Дата добавления: 2015-06-04; Просмотров: 3392; Нарушение авторских прав?; Мы поможем в написании вашей работы!