
КАТЕГОРИИ:
Архитектура-(3434)Астрономия-(809)Биология-(7483)Биотехнологии-(1457)Военное дело-(14632)Высокие технологии-(1363)География-(913)Геология-(1438)Государство-(451)Демография-(1065)Дом-(47672)Журналистика и СМИ-(912)Изобретательство-(14524)Иностранные языки-(4268)Информатика-(17799)Искусство-(1338)История-(13644)Компьютеры-(11121)Косметика-(55)Кулинария-(373)Культура-(8427)Лингвистика-(374)Литература-(1642)Маркетинг-(23702)Математика-(16968)Машиностроение-(1700)Медицина-(12668)Менеджмент-(24684)Механика-(15423)Науковедение-(506)Образование-(11852)Охрана труда-(3308)Педагогика-(5571)Полиграфия-(1312)Политика-(7869)Право-(5454)Приборостроение-(1369)Программирование-(2801)Производство-(97182)Промышленность-(8706)Психология-(18388)Религия-(3217)Связь-(10668)Сельское хозяйство-(299)Социология-(6455)Спорт-(42831)Строительство-(4793)Торговля-(5050)Транспорт-(2929)Туризм-(1568)Физика-(3942)Философия-(17015)Финансы-(26596)Химия-(22929)Экология-(12095)Экономика-(9961)Электроника-(8441)Электротехника-(4623)Энергетика-(12629)Юриспруденция-(1492)Ядерная техника-(1748)
Cl …3s 2 3p 5, O…. 2s 2 2p 4 3 страница
Принцип Ле-Шателье: если на с-му, нах в равновесии, производится внешнее воздействие (изменяются С,Т,Р), то оно благоприятствует протеканию той из двух противоположных р-ций, кот ослабляет это воздействие
1. Влияние концентраций компонентов системы.
СН4 + 2Н2О(г) = СО2 + 4Н2 ,
Если в с-му добавить метан, то равновесие нарушается, ускорится прямая р-ция,зн. увеличению СО2 и Н2 и уменьшению Н2О, равновесие смещается вправо. Процесс будет протекать до тех пор, пока не установится новое равновесие. Новое равновесие концентраций будут такими, чтобы соотношения между ними, определяемое константой равновесия, оставалось постоянным. Если в с-му ввести дополнительное количество СО2, то в соответствии с принципом Ле Шателье равновесие сместится влево.2. Влияние общего давления в системе. Если в рез-те р-ции изменяется число молей газообр в-в, то изменение Робщ в с-ме вызывает смещение равновесия. В соответствии с принципом Ле Шателье увел. Робщ в с-ме вызывает смещение равновесия в сторону уменьшения числа молей газообр в-в, т.е. в сторону уменьшения давления. 3. Влияние температуры. С увеличением Т равновесие смещается в сторону эндотерм р-ции реакций. Для рассматриваемой реакции равновесие смещается в правую сторону (DН>0), а для экзотерм р-циив левую сторону.Зависимость константы равновесия р-ции от Т может быть описана ур-ем изобары хим р-ции (изобары Вант-Гоффа):
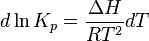
и изохоры хим р-ции (изохоры Вант-Гоффа):
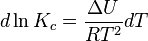
Здесь 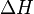 и
и 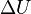 — тепловой эффект р-ции, протекающей при P,Vconst Если
— тепловой эффект р-ции, протекающей при P,Vconst Если 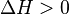 -р-ция эндотерм, то температурный коэффициент константы равновесия положителен, т.е с >>T константа равновесия эндотерм р-ции ув-ся, равновесие сдвигается вправо. 4) катализаторы не влияют на положение равновесия. Чтобы качественно определить, в какую сторону оно сместится, можно воспользоваться принципом Ле Шателье: если на систему, находящуюся в равновесии оказывается внешнее воздействие, то равновесие смещается в том направлении, которое ослабляет внешнее воздействие.
-р-ция эндотерм, то температурный коэффициент константы равновесия положителен, т.е с >>T константа равновесия эндотерм р-ции ув-ся, равновесие сдвигается вправо. 4) катализаторы не влияют на положение равновесия. Чтобы качественно определить, в какую сторону оно сместится, можно воспользоваться принципом Ле Шателье: если на систему, находящуюся в равновесии оказывается внешнее воздействие, то равновесие смещается в том направлении, которое ослабляет внешнее воздействие.
|
|
Дата добавления: 2015-06-28; Просмотров: 326; Нарушение авторских прав?; Мы поможем в написании вашей работы!