
КАТЕГОРИИ:
Архитектура-(3434)Астрономия-(809)Биология-(7483)Биотехнологии-(1457)Военное дело-(14632)Высокие технологии-(1363)География-(913)Геология-(1438)Государство-(451)Демография-(1065)Дом-(47672)Журналистика и СМИ-(912)Изобретательство-(14524)Иностранные языки-(4268)Информатика-(17799)Искусство-(1338)История-(13644)Компьютеры-(11121)Косметика-(55)Кулинария-(373)Культура-(8427)Лингвистика-(374)Литература-(1642)Маркетинг-(23702)Математика-(16968)Машиностроение-(1700)Медицина-(12668)Менеджмент-(24684)Механика-(15423)Науковедение-(506)Образование-(11852)Охрана труда-(3308)Педагогика-(5571)Полиграфия-(1312)Политика-(7869)Право-(5454)Приборостроение-(1369)Программирование-(2801)Производство-(97182)Промышленность-(8706)Психология-(18388)Религия-(3217)Связь-(10668)Сельское хозяйство-(299)Социология-(6455)Спорт-(42831)Строительство-(4793)Торговля-(5050)Транспорт-(2929)Туризм-(1568)Физика-(3942)Философия-(17015)Финансы-(26596)Химия-(22929)Экология-(12095)Экономика-(9961)Электроника-(8441)Электротехника-(4623)Энергетика-(12629)Юриспруденция-(1492)Ядерная техника-(1748)
Реактиви. Розчин нітрату ртуті(ІІ), 0,005 моль-екв/дм3: наважку 0,834 ± 0,001 г Hg(N03)2∙0,5Н20, х.ч., розчиняють у 100 см3 бідистильованої води
|
|
|
|
Розчин нітрату ртуті(ІІ), 0,005 моль-екв/дм3: наважку 0,834 ± 0,001 г Hg(N03)2∙0,5Н20, х.ч., розчиняють у 100 см3 бідистильованої води, яка містить 1,5 − 2,0 см3 концентрованої азотної кислоти, і розбавляють бідистильованою водою до 1 дм3 у мірній колбі.
Точну концентрацію розчину Hg(N03)2 встановлюють титруванням за робочим розчином NІ.
Змішаний індикатор: 0,5 г дифенілкарбазону С13Н12ON4, х.ч., і 0,05 г бромфенолового синього С19Н10О4Вr4, х.ч., розчиняють у 100 см3 96%-го етилового спирту в мірній колбі місткістю 100 см3. Розчин стійкий упродовж місяця, якщо його зберігати в пляшці з темного скла.
Розчин азотної кислоти, 0,05 моль-екв/дм3: 3,2 см3 концентрованої НN03, х.ч., розбавляють бідистильованою водою до 1 дм3 у мірній колбі.
Розчин лугу, 0,05 моль-екв/дм3: 2 г NаОН, х.ч., розчиняють у бідистильованій воді й доводять об'єм розчину до 1 дм3 у мірній колбі.
Етиловий спирт С2Н5ОН, 96%-й.
Стандартний розчин хлориду натрію, 0,01 моль-екв/дм3: 0,5844 ± 0,0005 г NaС1, попередньо прожареного при 500 − 600 °С до повного видалення вологи, розчиняють у дистильованій воді й доводять об'єм розчину до 1 дм3 у мірній колбі.
Робочий розчин хлориду натрію, 0,005 моль-екв/дм3: готують розбавлянням стандартного розчину NaСl у два рази.
Визначення концентрації розчину Hg(N03)2. У фарфорову чашку піпеткою вносять 1,0 см3 стандартного розчину NaС1 (концентрацією 0,01 моль-екв/дм3), добавляють 2 см3 етилового спирту, 0,5 см3 розчину азотної кислоти, 3−4 краплі змішаного індикатору, а далі діють за описаною методикою аналізу.
Концентрацію розчину Hg(N03)2 Сх (моль-екв/дм3) обчислюють за рівнянням
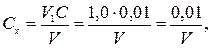
де V1 − об'єм взятого стандартного розчину NaС1, см3; С − концентрація стандартного розчину NаСІ, моль-екв/дм3; V − об'єм розчину Hg(N03)2, витрачений на титрування, см3.
|
|
|
Лабораторна робота №2
Визначення вмісту Сульфатів
Сульфати — один із компонентів сольового складу, що міститься в усіх поверхневих водах. Головними джерелами надходження сульфатів у воду є розчинення сірковмісних мінералів (в основному гіпсу), окиснення сульфідів і сірки, а також скидання шахтних і промислових стічних вод. Вміст сульфатів у поверхневих водах суходолу коливається від 5 − 10 до 60 − 80 мг S042- /дм3 і зазвичай корелює із загальною мінералізацією води.
Вміст сульфатів у природних водах визначають гравіметричним, титриметричними та турбідиметричним методами. Гравіметричний метод є найточнішим, але довготривалий і трудомісткий, тому його застосовують тільки для арбітражних аналізів. Зручними і досить точними є титриметричні методи. Найбільш чутливий і швидкий, але менш точний − турбідиметричний метод. Вміст сульфатів можна визначити також методом іонної хроматографії.
|
|
|
|
|
Дата добавления: 2014-11-06; Просмотров: 453; Нарушение авторских прав?; Мы поможем в написании вашей работы!