
КАТЕГОРИИ:
Архитектура-(3434)Астрономия-(809)Биология-(7483)Биотехнологии-(1457)Военное дело-(14632)Высокие технологии-(1363)География-(913)Геология-(1438)Государство-(451)Демография-(1065)Дом-(47672)Журналистика и СМИ-(912)Изобретательство-(14524)Иностранные языки-(4268)Информатика-(17799)Искусство-(1338)История-(13644)Компьютеры-(11121)Косметика-(55)Кулинария-(373)Культура-(8427)Лингвистика-(374)Литература-(1642)Маркетинг-(23702)Математика-(16968)Машиностроение-(1700)Медицина-(12668)Менеджмент-(24684)Механика-(15423)Науковедение-(506)Образование-(11852)Охрана труда-(3308)Педагогика-(5571)Полиграфия-(1312)Политика-(7869)Право-(5454)Приборостроение-(1369)Программирование-(2801)Производство-(97182)Промышленность-(8706)Психология-(18388)Религия-(3217)Связь-(10668)Сельское хозяйство-(299)Социология-(6455)Спорт-(42831)Строительство-(4793)Торговля-(5050)Транспорт-(2929)Туризм-(1568)Физика-(3942)Философия-(17015)Финансы-(26596)Химия-(22929)Экология-(12095)Экономика-(9961)Электроника-(8441)Электротехника-(4623)Энергетика-(12629)Юриспруденция-(1492)Ядерная техника-(1748)
Уравнения для расчета кинетических характеристик химических реакций различного порядка
|
|
|
|
(со – начальная концентрация реагента)
| Величина | Порядок химической реакции n | |||
| n = 0 | n = 1 | n = 2 | n = 3 | |
| Кинетическое уравнение | 
| 
| 
| 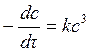
|
| Константа скорости k | 
| 
| 
| 
|
| Размерность k | 
| 
| 
| 
|
| Концентрация реагента с в момент времени τ, моль/л | 
| 
| 
| 
|
| Время полупревращения τ 1/2 | 
| 
| 
| 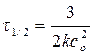
|
П р и м е р 4.2. В реакции 2-го порядка A + B → D начальные концентрации веществ A и B составляют cA,o = 2,0 моль/л, сB,o = 3,0 моль/л. При концентрации сA = 1,5 моль/л скорость реакции равна 1,2·10–3 моль/(л с). Рассчитать константу скорости этой реакции.
Р е ш е н и е
Если к определенному моменту времени концентрация вещества А стала равной 1,5 моль/л, следовательно, количество прореагировавшего числа А будет равно:
x = 2,0 – 1,5 = 0,5 моль/л.
Так как вещества А и B реагируют при мольном соотношении 1: 1, то в реакцию вступит такое же количество (0,5 моль/л) вещества B. Следовательно, концентрация вещества B к моменту, когда сA = 1,5 моль/л, будет составлять:
cB = 3,0 – 0,5 = 2,5 моль/л.
По закону действующих масс скорость связана с концентрациями реагирующих веществ уравнением (4.6). При применении этого уравнения учитываем, что по условию задачи общий порядок рассматриваемой реакции равен 2 (частные порядки равны 1):
v = k · сA · сB.
Отсюда константа скорости равна:
 л/(моль · с).
л/(моль · с).
П р и м е р 4.3. Период распада радиоактивного изотопа углерода 14С составляет 5730 лет. Каков возраст найденного при раскопках дерева, если содержание в нем 14С составляет 72 % от нормального.
Р е ш е н и е
Радиоактивный распад является реакцией первого порядка. Из формулы, приведенной в табл. 4.1 для времени полупревращения в реакциях 1-го порядка, имеем:
|
|
|
 ,
,
находим константу скорости данной реакции:
 лет –1.
лет –1.
Из формулы для расчета константы скорости реакции 1-го порядка (табл. 4.1):
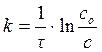 ,
,
рассчитываем время реакции, учитывая, что с = 0,72 · со:
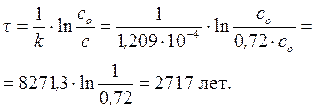
П р и м е р 4.4. Константа скорости реакции первого порядка для реакции, проходящей при температуре 323 К, составляет 0,139 мин–1. Исходная концентрация реагента 0,5 моль/л. Какая концентрация данного реагента будет достигнута через 10 минут протекания реакции при этой темпеаратуре. Чему равна степень превращения исходного вещества за это время?
Р е ш е н и е
Расчет текущей концентрации для реакции первого порядка производим по соответствующей формуле (табл. 4.1):
 ;
;
С = 0,124 моль/л;
степень превращения (x):
x = (0,5 – 0,124) / 0,5 = 0,752 (75,2 %).
П р и м е р 4.5. Окисление хлористого железа FeCl2 при помощи KClO3 в присутствии соляной кислоты – реакция третьего порядка. Константа скорости этой реакции равна 1,0 л2 ·моль-2 · мин. Вычислить концентрацию хлористого железа через 1,5 часа после начала реакции, если начальные концентрации всех реагирующих веществ равны 0,2 моль/л.
Р е ш е н и е
Концентрацию реагента в данный момент времени для реакции третьего порядка рассчитываем по соответствующему уравнению (табл.4.1):

|
|
|
|
|
Дата добавления: 2017-01-14; Просмотров: 2001; Нарушение авторских прав?; Мы поможем в написании вашей работы!