
КАТЕГОРИИ:
Архитектура-(3434)Астрономия-(809)Биология-(7483)Биотехнологии-(1457)Военное дело-(14632)Высокие технологии-(1363)География-(913)Геология-(1438)Государство-(451)Демография-(1065)Дом-(47672)Журналистика и СМИ-(912)Изобретательство-(14524)Иностранные языки-(4268)Информатика-(17799)Искусство-(1338)История-(13644)Компьютеры-(11121)Косметика-(55)Кулинария-(373)Культура-(8427)Лингвистика-(374)Литература-(1642)Маркетинг-(23702)Математика-(16968)Машиностроение-(1700)Медицина-(12668)Менеджмент-(24684)Механика-(15423)Науковедение-(506)Образование-(11852)Охрана труда-(3308)Педагогика-(5571)Полиграфия-(1312)Политика-(7869)Право-(5454)Приборостроение-(1369)Программирование-(2801)Производство-(97182)Промышленность-(8706)Психология-(18388)Религия-(3217)Связь-(10668)Сельское хозяйство-(299)Социология-(6455)Спорт-(42831)Строительство-(4793)Торговля-(5050)Транспорт-(2929)Туризм-(1568)Физика-(3942)Философия-(17015)Финансы-(26596)Химия-(22929)Экология-(12095)Экономика-(9961)Электроника-(8441)Электротехника-(4623)Энергетика-(12629)Юриспруденция-(1492)Ядерная техника-(1748)
Реакция азосочетания
Одним из важнейших превращений солей диазония, во многом определившим их широкое использование, является реакция азосочетания. Диазотирование аминов при этом обычно ведут в соляной кислоте, так как NOCl активнее N2O3, а также реакция второго порядка в соляной кислоте технологически предпочтительнее реакции третьего порядка в серной кислоте.
Азосочетание с аренами идет по механизму электрофильного замещения. Электрофилом (диазосоставляющей) является диазокатион. В качестве азосоставляющей чаще всего используют фенолы и амины, а также другие активированные арены (производные бензола, нафталина, гетероциклов и др.). Это связано с тем, что обычно диазокатион существует при 0—10 °С, поэтому реакцию азосочетания ведут при температуре 0—25 °С, а в этих условиях с диазокатионом реагируют только активированные арены.


Активность электрофильных частиц в этой реакции зависит от заместителей в ароматическом ядре в орто- и пара- положениях относительно диазогруппы и уменьшается в ряду:
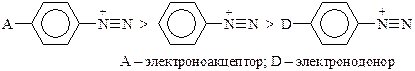
Сочетание с фенолами и нафтолами чаще всего проводят в слабощелочной среде (растворы соды, ацетата натрия), в которой они хорошо растворяются и находятся в активной фенолятной форме. Сильнощелочные растворы (растворы NaOH) неблагоприятны для азосочетания, так как переводят соли диазония в неактивные формы (диазогидрат и диазотат).
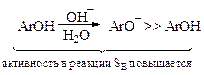

Сочетание с аминами лучше вести в слабокислой среде (разбавленная уксусная кислота). В этих условиях амины растворяются, и значительная часть их находится в активной форме, а соли диазония устойчивы.
Сильнокислая среда недопустима, т.к. группа NH3+ является акцептором электронов и дезактивирует ароматическое ядро. Соли аминов не вступают в реакцию азосочетания.
В случае первичных и вторичных аминов электрофилы атакуют и атом азота. Образующиеся при этом диазоаминосоединения (арилтриазены) в ряде случаев изомеризуются в С-азосоединения:

Направление реакции азосочетания с первичными и вторичными аминами сильно зависит от кислотности среды. Чтобы снизить образование побочных арилтриазенов реакцию проводят при рН не более 4.
Азосочетание ведут при низких температурах (0—25 °С), чтобы избежать разложения соли диазония. Реакция проходит практически нацело. Продукт реакции, как правило, нерастворим и может быть выделен из реакционной массы фильтрованием.
Примером может служить получение азорибитиламина в производстве витамина В2:
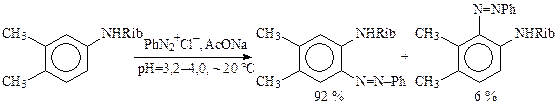

Согласованная ориентация и более благоприятные пространственные условия способствуют образованию целевого 6-азоизомера с выходом 92 %. Выход побочного — до 6 %. При значении рН > 4 в качестве побочного продукта образуется диазоаминосоединение, которое не способно к конденсации в рибофлавин.
Обычно диазосоставляющая по объему и структуре молекулы проще, чем азосоставляющая, однако бывают и обратные варианты
Образование диазоаминосоединения во многих случаях является побочной реакцией и ее стараются избежать. Однако в синтезе азидина она является целевой:
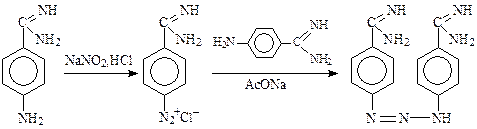
Сочетание солей диазония с алифатическими азосоставляющими. В алифатическом ряду реакция азосочетания известна лишь с соединениями общей формулы Z–CH2–Z' или Z'–CHR–Z (β-кетоэфиры, малоновый эфири т. п.), где Z и Z' ацильные, карбоксильные и др. электроноакцепторные заместители. Вероятный механизм SE1:

В этом случае первоначально образующееся соединение неустойчиво и изомеризуется в гидразон, который и является продуктом реакции. При проведении реакции с соединениями типа Z'–CHR–Z отщепляется одна из электроноакцепторных групп (особенно, если это ацил или карбоксил) и, также, как и в предыдущем случае, образуется гидразон:

При наличии в молекуле и ацильной и карбоксильной групп преимущественно отщепляется карбоксильная. При этом реакция может идти через енолизацию субстрата и электрофильное присоединение соли диазония по двойной связи с образованием p- и s- комплексов:
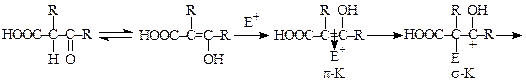
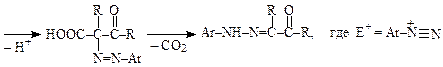
В отсутствие ацильных и карбоксильных групп в молекуле алифатического субстрата образуется азосоединение.
В синтезе индопана и серотонина азосочетание сопровождается декарбоксилированием 2-пиперидона-3-карбоновой кислоты, и азогруппа становится на место уходящей карбоксильной группы:


Другим примером использования азосоставляющей неароматического характера является одна из стадий в синтезе меркаптопурина:
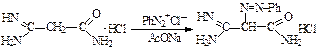
|
|
Дата добавления: 2014-10-15; Просмотров: 2576; Нарушение авторских прав?; Мы поможем в написании вашей работы!